Enraf-Nonius CD-ROM Endomed 182 Manual de usuario
- Tipo
- Manual de usuario

Page 1 of 52 EN109-1634750-40 IFU
Endomed 182
EN109-1634750-40 IFU
September 21, 2020
Instructions for use

Page 2 of 52 EN109-1634750-40 IFU
Table of contents
1 Introduction ...................................................................................................................................................... 3
2 Symbols .............................................................................................................................................................. 7
3 Device components ....................................................................................................................................... 9
4 Package contents ......................................................................................................................................... 13
5 Installation ...................................................................................................................................................... 15
6 Intended use and intended user ............................................................................................................ 16
7 Indications ...................................................................................................................................................... 17
8 Contra-indications ....................................................................................................................................... 18
9 Precautionary instructions ........................................................................................................................ 20
10 Operation ........................................................................................................................................................ 23
11 Application information............................................................................................................................. 37
12 Maintenance and troubleshooting ........................................................................................................ 44
13 Specifications ................................................................................................................................................. 48
14 Contact ............................................................................................................................................................. 51
15 Product liability ............................................................................................................................................. 51

Page 3 of 52 EN109-1634750-40 IFU
1 Introduction
Foreword
Thank you for purchasing the Endomed 182.
The Endomed 182, designed and manufactured by Enraf-Nonius B.V., offers a new dimension in
electrotherapy, made possible by advanced hardware and software design. The result is a device
with extraordinary versatility based on simplicity of operation.
This manual has been written for the owners and operators of the Endomed 182. In order to
maximize the use, efficiency and lifespan of your unit, please read this manual thoroughly and
become familiar with the controls as well as the accessories before operating the device.
Device Description
The Endomed 182 is a mains-powered electrostimulator and is equipped with a full color touch
screen. The graphic user interface allows for maximum operator comfort.
Three versions of the Endomed 182 are available:
Endomed 182 versions
Name:
Endomed 182 Type 1
Endomed 182 Type 2
Endomed 182 Type 3
Article
number:
1634903
1634901
1634902
Article
number base
unit:
1634910
1634900
1634900
Current
Wave Forms:
Direct current
TENS
• continuous biphasic pulsed
current (conventional TENS
mode)
• trains of biphasic pulsed current
(Burst TENS mode)
Interferential Current (IFC)
• 2-pole interferential
(bipolar) mode
• 4-pole interferential
(tetrapolar) mode
• 4-pole interferential
(tetrapolar) with Isoplanar Vector
TENS
• continuous biphasic pulsed
current (conventional TENS
mode)
• trains of biphasic pulsed current
(Burst TENS mode)
Interferential Current (IFC)
• 2-pole interferential
(bipolar) mode
• 4-pole interferential
(tetrapolar) mode
• 4-pole interferential
(tetrapolar) with Isoplanar Vector
Vacuum
Channels:
1
2
2
Pre-
programmed
treatment
protocols:
-
16
16

Page 4 of 52 EN109-1634750-40 IFU
The Endomed 182 Type 1 is a mains-powered single-channel electrostimulator for the application
of Percutaneous Electrolysis (PE) by means of low-intensity Direct Current (DC).
In PE, the Direct Current (also referred to as Galvanic Current) is applied through a needle that is
placed in the needle holder of a handpiece (the ‘applicator’ or cathode). The return electrode (or
anode) is a hand-held electrode (held by the patient) or another needle, depending on the treatment
to be performed.
The needle holder of the applicator (handpiece) enables the attachment of acupuncture needles
(sterile, single-use and disposable) of different length and diameter, necessary to ensure proper
placement in different areas (depending on the disorder to treat).
The handpiece is equipped with a start/stop button to begin or interrupt the flow of current manually.
The device delivers a continuous galvanic current with a maximum output of 15 mA.
The graphic user interface shows the following treatment parameters: current output level (mA), time
set for the application, actual current delivered (mC).
The user can set and adjust the output level of the current (mA) and the application time, depending
on the type of treatment.
The device does not offer any preset clinical protocol, but treatment parameters can be set and saved
as favorites (personalized settings) as a reference for future therapy sessions.
The device is a compact unit that comes with the following accessories: mains and connecting cables,
handpiece (applicator), return electrode, footswitch (optional) and product documentation.
Consumables such as disposable (acupuncture) needles are not delivered with the product.
Enraf-Nonius B.V. does not supply percutaneous electrodes or disposable acupuncture needles.
The Endomed 182 Type 2 and 3 include 16 preset clinical protocols for TENS and Interferential
currents. Individual treatment parameters can also be set manually and adjusted by the operator. All
treatment parameters can be set and saved as favorites (personalized settings) as a reference for
future therapy sessions.
The Endomed 182 Type 3, is a stacked configuration that consists of a separate vacuum suction
module and an electrostimulator Endomed 182 Type 2. The vacuum module is placed under, and
connected to, the stimulator. The purpose of the module is to generate a vacuum which enables the
therapist to quickly and (more) easily secure (fixate) the stimulation electrodes to the patient. The
fixation is achieved by means of suction cups. The suction cups have integrated stimulation surfaces
that transfer the electrostimulation via moistened sponges to the target tissue.
For Endomed 182 Type 2 and 3 the electrical stimulation can thus be applied to the skin via surface
electrodes: flexible rubber electrodes, self-adhesive electrodes or vacuum electrodes (Type 3 only),
with the objective to stimulate specific types of nerve fibers. Enraf-Nonius has various types and
sizes of electrodes (from point electrode with a surface of 0.3 cm2 to electrodes with a surface of 96
cm2) available to accommodate the size of the treatment area or the anticipated treatment goal.

Page 5 of 52 EN109-1634750-40 IFU
Current Wave Description
TENS
The asymmetrical biphasic pulsed current waveform is often used in TENS (Transcutaneous Electrical
Nerve Stimulation) applications. This waveform is characterized by variable phase duration and
variable pulse frequency. Its typical amplitude, duration, and rate of rise and decay are unequal for
each phase with respect to the baseline. The waveform is fully balanced, i.e. the phase charges of
each phase are equal. The biphasic nature of the pulse means that there is no net DC component
(zero net DC), thus minimizing any skin reactions due to the build-up of electrolytes under the
electrodes.
To prevent accommodation to stimulation or to
improve patient tolerance, the pulse frequency
can be varied through frequency modulation.
Asymmetrical biphasic waveform TENS
Burst TENS
Burst TENS is applied if Conventional TENS proves ineffective, and is particularly suitable for the
treatment of deeper lying painful regions and cases of chronic pain. Burst TENS uses a relatively
large phase duration (150-200 μs), a low burst frequency (1-5 Hz) and a high frequency.
Strong, visible contractions should occur in the muscles whose innervation corresponds with that of
the painful region.
The pain-reducing effect generally does not appear for some twenty to thirty minutes, unlike the
effect of Conventional TENS, which usually occurs fairly rapidly. However, the effect lasts for
considerably longer than that of Conventional TENS after stimulation has ended. The pain-reducing
effect of Burst TENS is due to the release of endorphins at both spinal and supraspinal level.
If Conventional or Burst TENS give no or insufficient relief, Frequent Modulation can be used.
Frequency Modulation can also prevent accommodation.
Interferential current (IFC)
With the interferential current type, a medium frequency carrier frequency is used to pass the low
frequency stimulation (beat) frequency through the skin. The relatively low resistance of the skin to
the carrier frequency contributes to the patient comfort that is often associated with this current
type. Interferential currents are all AC currents without any residual DC components. Several
variations of the interferential current type are known, of which the following are available in the
Endomed 182 Type 2 and 3: 2-pole, 4-pole and 4-pole with isoplanar vector.
The two-pole method
In this method two electrodes are used and
superimposition of the two alternating currents takes
place within the equipment. The current leaving the
equipment is a fully modulated alternating current. In
the two-pole method the modulation depth is always
100%.
Bipolar interferential therapy

Page 6 of 52 EN109-1634750-40 IFU
The four-pole method (Classic Interferential)
With this therapy method four electrodes are used and
two non-modulated currents are generated. The
frequency of one channel is fixed at the carrier
frequency, while the other channel has a variable
frequency, based on the Beat frequency and Frequency
Modulation settings. Interference occurs where the two
currents intersect in the tissue. The modulation depth
(which determines the current amplitude of the
stimulation) depends on the direction of the currents,
and can vary from 0 to 100%. 100% modulation depth
only occurs at the diagonals (and hence at the
intersection) of the two currents. This is of course a
theoretical situation, based on the assumption that the
tissue is homogeneous. In reality, the tissue is
heterogeneous, so that the current balance between
the two channels has to be used to obtain the 100%
modulation depth. The current balance can also be
used to compensate for differences in sensation
occurring under the electrodes.
In the four-pole method, the modulation
depth is only 100% at the diagonals.
The four-pole method with Isoplanar vector
With the Isoplanar vector the total area between the 4
electrodes is optimal stimulated. The electrode
positioning can be done simple and quick. The
modulation depth is 100% everywhere.
Isoplanar Interferential can be used for the treatment
of problems which are located in a large area and
which are very difficult to locate. Isoplanar Interferential
is also used as a mild pre-treatment. After this
application the treatment is continued with a focus on
a smaller, more local area.
Isoplanar vector
Direct current
A direct current (DC) or galvanic current is a continuous current that has been used in medicine for
a number of therapeutic aims. The continuous current refers to the continuous flow of electric
charge via a current conductor between two points (electrodes) with different potentials (polarity),
which does not change direction over time. In contrast to alternating currents, the electrical charges
always flow in the same direction.

Page 7 of 52 EN109-1634750-40 IFU
2 Symbols
Symbol used
Description
Follow the instructions in the Instructions for Use.
It is important that you read, understand and observe the precautionary and
operating instructions
General Prohibition Sign.
Prohibition is used to mean “You MUST NOT”
Warning or Caution:
Indicates a hazardous situation which, if not avoided, could result in:
a. Death or serious injury to the patient (or)
b. Minor to moderate injury to the patient (or)
c. Damage to the equipment
General mandatory action sign.
Mandatory action is used to mean, “You must…”
Type BF applied part complying with the specified requirements to provide a
higher degree of protection against electric shock than that provided by type B
applied parts.
Temperature Range.
Indicates acceptable temperature range.
Humidity Limits.
Indicates acceptable relative humidity.
Atmospheric Pressure.
Indicates the range of atmospheric pressure to which the medical device can
be safely exposed.
Waste electrical items that can be recycled.
Indicates that the electrical and electronic components of the device can be
recycled and have to be disposed of separately.
Keep the device dry.
Manufacturer name, address and date of manufacture.
Reference Number or Part Number.
Serial Number
Indicates the serial number so that a specific medical device can be
identified.
Alternating current

Page 8 of 52 EN109-1634750-40 IFU
Connection electrode cable electrotherapy
Connections vacuum cables electrotherapy
“ON” (power)
“OFF” (power)
CE Mark along with number indicates conformity with European Council of
Directive concerning Medical Devices and this device is under the direct
supervision of the Notified Body.

Page 9 of 52 EN109-1634750-40 IFU
3 Device components
Endomed 182 Type 1
Endomed 182 Type 2
7
8
1
9
1
2
1
3
1
1
4
1
6
1
5
1
10
11

Page 10 of 52 EN109-1634750-40 IFU
Endomed 182 Type 3
12
13
16
15
14
17
18
19
21
20

Page 11 of 52 EN109-1634750-40 IFU
Parts Description
Numbered
Part
Description
Purpose
[1]
LCD Touch Screen
Color TFT display 4.3” with touch screen. Displays
the User Interface that allows the operator to
control the device and change parameters of
treatment protocols.
[2]
Connection Electrode holder
Connection Electrode holder
[3]
Connection blank earth
electrode
Connection for DC reference cable which connects
to the blank earth electrode
[4]
Blank earth electrode
Reference electrode
[5]
DC reference cable
Return electrode connection cable
[6]
Electrode holder
Handpiece for needle holder
[7]
Connection A
Connection for Vacuum Module (Endomed 182
Type 3 / Footswitch (Endomed 182 Type 1)
[8]
Connection B
Connection for Current Module
[9]
Current Module
Current Module with connection for adhesive and
rubber electrodes.
[10]
Connection 1 Current Module
Connection channel 1 for patient cable for adhesive
or rubber electrodes on Current Module Endomed
182.
[11]
Connection 2 Current Module
Connection channel 2 for patient cable for adhesive
or rubber electrodes on Current Module Endomed
182.
[12]
Vacuum electrode holder
Holder for vacuum electrodes.
[13]
Vacuum Module
Vacuum Module integrated with Endomed 182
with connections for adhesive or rubber electrodes
and vacuum electrodes.
[14]
Vacuum Module electrode
cables
Vacuum Module electrode cables need to be
connected to the Current Module [7] and [8]
connection for the correct functioning of the
Vacuum Module connections.
[15]
Upper connections Vacuum
Module
Connections channel 1 and 2 for patient cable for
adhesive or rubber electrodes on Vacuum Module.
[16]
Lower connections Vacuum
Module
Connections channel 1 and 2 for vacuum lead hose
for vacuum electrodes on Vacuum Module.
[17]
Mains switch
To switch the unit on and off
When turning the unit off the display remains
visible for a few seconds (low-energy method).
[18]
Reference label
Provides information of the device, such as type
and serial number.
[19]
Connector for Mains cable
Connect supplied Mains Cable here to power the
device.
[20]
Air outlet
Air outlet for Vacuum Module.

Page 12 of 52 EN109-1634750-40 IFU
Parts Description
Numbered
Part
Description
Purpose
[21]
Connection for water reservoir
This connection is used for connecting the water
reservoir. No vacuum can be created unless the
water reservoir is connected. The water reservoir
ensures that any excess water from the sponges is
collected, and cannot be blown out through the
pump. The reservoir should be emptied daily.
Please refer to the section on Maintenance.

Page 13 of 52 EN109-1634750-40 IFU
4 Package contents
Device
The package contents depend on the device ordered. The following models are available:
Article number
Description
1634903
Endomed 182 Type 1
1634901
Endomed 182 Type 2
1634902
Endomed 182 Type 3 (includes integrated Vacuum Module)
Standard accessories Endomed 182 Type 1
1634750
CD-ROM with Instructions For Use (PDF on CD-ROM)
1634751
Information Booklet
3444357
Power cord 250V/2.5 A, L=2.5 m, black
3444080
Electrode holder
3444582
Blank earth electrode
3444677
DC reference cable
Standard accessories Endomed 182 Type 2 and Endomed 182 Type 3
1634750
CD-ROM with Instructions For Use (PDF on CD-ROM)
1634751
Information Booklet
3444357
Power cord 250V/2.5 A, L=2.5 m, black
3444021
Strap 250x3 cm
3444020
Strap 100x3 cm
3444129
(2x) Rubber electrodes 6x8 cm, 2 mm female, set of 2
1460266
Moist pads for rubber electrodes 6x8 cm, set of 4
3444211
(2x) Patient cable 2-core & 2 mm male plugs – black, with color clips
Additional standard accessories Endomed 182 Type 3
3444503
(2x) Vacuum electrodes Ø 60 mm, set of 2
3444505
Sponges Ø 65 mm, set of 4 (for vacuum electrodes Ø 60 mm)
3444507
(2x) Vacuum lead hose red
3444508
(2x) Vacuum lead hose black
Optional accessories Endomed 182 Type 1
1634810
Foot switch
Optional accessories Endomed 182 Type 2 and Endomed 182 Type 3
Adhesive electrodes
3444056
EN-Trode Ø 3,2 cm, 2 mm female,10 sheets of 4
3444135
EN-Trode Ø 5,0 cm, 2 mm female, 10 sheets of 4
3444057
EN-Trode 5x5 cm, 2 mm female, 10 sheets of 4
3444058
EN-Trode 5x9 cm, 2 mm female, 10 sheets of 4
3444222
Adhesive electrodes Ø 2,2 cm, 2 mm female, 10 sheets of 8
Rubber electrodes
3444128
Rubber electrodes 4x6 cm, 2 mm female, set of 2
3444129
Rubber electrodes 6x8 cm, 2 mm female, set of 2
3444130
Rubber electrodes 8x12 cm, 2 mm female, set of 2
3444380
Silicon electrode 5x5 cm

Page 14 of 52 EN109-1634750-40 IFU
Moist pads for rubber electrodes
1460273
Moist pads for rubber electrodes 4x6 cm, set of 4
1460266
Moist pads for rubber electrodes 6x8 cm, set of 4
1460275
Moist pads for rubber electrodes 8x12 cm, set of 4
Fixation straps
3444020
Strap 100x3 cm
3444021
Strap 250x3 cm
3444022
Strap 100x5 cm
3444023
Strap 250x5 cm
Point electrodes
3444180
Point electrode, 5 mm Ø, 2 mm female, pen model, incl. 10 conductive rubber
caps
Adapters
2523523
Adapter plug, 2 mm female, 4 mm male, black
2523524
Adapter plug, 2 mm female, 4 mm male, red
Patient cables
3444211
Patient cable 2-core & 2 mm male plug – black, with colored clips
Additional optional accessories Endomed 182 Type 3
Vacuum electrodes
3444503
Vacuum electrodes Ø 60 mm, set of 2
3444504
Vacuum electrodes Ø 90 mm, set of 2
3444509
Vacuum electrodes Ø 30 mm, set of 2
Sponges
3444505
Sponges Ø 65 mm, set of 4 (for vacuum electrodes Ø 60 mm)
3444506
Sponges Ø 95 mm, set of 4 (for vacuum electrodes Ø 90 mm)
3444516
Sponges Ø 30 mm, set of 4 (for vacuum electrodes Ø 30 mm)
Vacuum lead hoses
3444507
Vacuum lead hose, red
3444508
Vacuum lead hose, black
Ordering information
For the ordering data of the Endomed 182 and accessories we refer to the website
www.enraf-nonius.com.

Page 15 of 52 EN109-1634750-40 IFU
5 Installation
Inspection
In case any damage is noticed after unpacking the device, please immediately contact your
local distributor. DO NOT USE the device!
The unit should be installed in such a way, that its warmth can be passed on to the
surroundings.
Immediately upon unpacking the device, perform the following steps:
• Verify the delivery documents to make sure that the delivery is complete.
• Verify that the packaging contains all the items listed in the standard accessories list
(Refer to chapter 4 - Package contents in this manual).
• Check the external components and accessories for possible damage due to transport.
Unpacking
The Endomed 182 is specially packaged for transport in a single pack complete with filling which
has been specifically designed for safe transportation and storage.
• To remove the equipment from the pack, place the box on a smooth, flat surface.
• Open the top of the box and remove the polystyrene filling.
• Be very careful when removing the contents of the pack.
Device setup
Endomed 182 Type 2:
• Connect the cable from the Current Module [9] to Connector B [8].
Endomed 182 Type 3:
• Connect the cable from the Current Module [9] to Connector B [8].
• Connect the cable from the Vacuum Module [13] to Connector A [7].
Refer to chapter 3 – Device components in this manual.
Connection to mains supply
Use of any other cable other than the supplied cable is strictly PROHIBITED as it
affects patient safety and the proper function of the device.
Before connection of this unit to the mains supply, check that the mains voltage and frequency
stated on the identification plate of this apparatus corresponds with that of the mains supply.
To avoid the risk of electric shock, this equipment must only be connected to a supply mains
with protected earth.
Plug in the device to a wall socket using the mains cable.
• Insert the mains cable into cable socket [19] and connect it to a wall socket.
Disconnection of mains supply
• When you have finished treatment, turn the device off by setting the mains switch to Off. The
device is now disconnected from the mains supply.
• Disconnect the mains cable from the wall socket.
• Disconnect the mains cable from socket [19].

Page 16 of 52 EN109-1634750-40 IFU
6 Intended use and intended user
Intended use
Endomed 182 Type 1
The Endomed 182 Type 1 is a single-channel electrostimulator, intended and designed for use by
health professionals to perform Percutaneous Electrolysis (PE) by means of low-intensity Direct
Current (DC).
Endomed 182 Type 2 and 3
The Endomed 182 Type 2 and 3 are 2 channel electrostimulators, intended and designed for use by
health professionals to perform Pain Management with IFC (Interferential current) and TENS
current.
Pain Management by means of electrostimulation refers to:
- Symptomatic relief of chronic, intractable pain
- Management of pain associated with post-traumatic or postoperative conditions
- Relief of pain associated with arthritis
The electrical stimulation is applied to the skin via surface electrodes with the objective to stimulate
specific types of nerve fibers. Pain relief (pain modulation) can be achieved by:
1. blocking the information travelling along the nociceptive fibers (i.e. those that produce pain)
through stimulation of the large diameter afferent A fibers
2. through the release of the body’s endogenous opioids by stimulation of the small diameter
afferent and motor fibers
Intended user
The Endomed 182 is intended to be used, and shall only be used, by or under the supervision of
professional users in the field of physical medicine and rehabilitation at professional healthcare
facilities.
Additionally for Endomed 182 Type 1:
If a health professional (physiotherapist, physician) is allowed and trained to use ultrasound-guided
galvanic electrolysis therapy, the health professional is allowed and trained to:
-> to perform needle punctures on a patient;
-> to use ultrasonography;
-> to use galvanic electrolysis therapy.

Page 17 of 52 EN109-1634750-40 IFU
7 Indications
Indications Endomed 182 Type 1
Percutaneous Electrolysis
Percutaneous Electrolysis (PE) can be used for the treatment of the following conditions:
• Patellar tendinopathy / patellar tendonitis (‘jumper’s knee’)
• Lateral elbow tendinopathy (tennis elbow)
• Medial elbow tendinopathy (golfer’s elbow)
• Myofascial Pain Syndrome / Triggerpoints
• Acute whiplash syndrome (AWS)
• Shoulder disorders (rotator cuff tendinopathies, Subacromial Pain Syndrome)
• Pubalgia (groin pain)
• Hamstring tendinopathy
• Achilles tendinopathy
• Fasciitis Plantaris / Heel Pain
Indications Endomed 182 Type 2 and 3
TENS
Relief of acute pain
• Postoperative pain
o Abdominal
o Thoracic
o p.o. orthopedic pain
• Labour pain and post-labour pain
• Dysmenorrhea
• Orofacial pain, including dental procedures
• Physical trauma, including fractured ribs and minor medical procedures
Relief of chronic pain
• Low back pain
• Arthritic pain, including osteoarthritis, rheumatoid arthritis
• Muscle pain, including myofascial pain, muscle tension, post-exercise soreness
• Neuropathic pain, including post amputation (phantom pain), post-herpetic, trigeminal
neuralgia
• Cancer pain, including metastatic bone pain
• Complex Regional Pain Syndrome
Interferential Current (IFC)
Relief of acute and chronic pain, such as:
• Postoperative pain /orthopedic pain
• Low back pain
• Neck pain
• Shoulder pain
• Arthritic pain, including osteoarthritis, rheumatoid arthritis
• Muscle pain, including myofascial pain, muscle tension, post-exercise soreness, and
fibromyalgia
Muscle Stimulation
• Muscle strengthening (in general)
• Faecal and urinary incontinence
Bowel Dysfunction
Increase local (cutaneous) blood flow

Page 18 of 52 EN109-1634750-40 IFU
8 Contra-indications
The Endomed 182 MUST NOT be used for the below mentioned symptoms or medical
conditions.
Contraindications Endomed 182 Type 1
Contraindications for use
• Infectious arthritis
• Heart disease / cardiac arrhythmia
• Pregnancy
• Skin ulcers and other skin infections
• Endoprosthesis and/or osteosynthesis
• Pacemakers
• Oncological processes
• Thrombophlebitis / history of vascular insufficiency in the legs
• Coagulopathy / anticoagulation drugs
• Blood dyscrasia
• Menstruation
• Needle phobia
• Fear of electrical stimulation
• Endocrine glands
• Patients with impaired sensitivity
• Patients with central and peripheral neurological disorders
• Patients with neurovegetative disorders
• Paediatric patients
• Complicated medical conditions
• Cognitive impairment
• Drug or alcohol abuse
Points where treatments should not be applied:
• Blood vessels
• Endocrine glands
• Organs
• Peripheral nerves (endoneurium)
• Head, eyes, neck and thorax or upper part of the back traversing the heart
Precautions Percutaneous Electrolysis
Regions that require special caution:
• Abdominal region
• Intercostal region (precaution against pneumothorax)
• Thoracic region (precaution against pneumothorax)
• Thoracic outlet (precaution against pneumothorax)
• Inguinal region, popliteal hollow (precaution against damaging neurovascular bundles)

Page 19 of 52 EN109-1634750-40 IFU
Contraindications Endomed 182 Type 2 and 3
Absolute contraindications:
• Undiagnosed pain
• Active implants (incl. cardiac pacemakers and implantable cardioverter defibrillators - ICDs)
• Tissue bleeding (haemorrhage)
• Patients who do not comprehend the practitioner’s / physical therapist’s instructions or who are
unable to co-operate
Relative contraindications (= local contraindications):
• Pregnancy (do not apply anywhere over abdomen/pelvic region)
• Malignancy (do not apply over active malignancy)
• Epilepsy (do not apply on neck or head)
• Cardiac disturbances such as dysrhythmias (do not apply through the chest)
• Electrode placement around the eyes
• Electrode placement over the anterior aspect of the neck or carotid sinus
• Electrode placement through the chest (i.e. anterior and posterior electrode positions)
• Electrode placement over testes
• Electrode placement over active epiphyseal regions in children
• Electrode placement over damaged skin or open wounds
• Electrode placement over dermatological lesions e.g. dermatitis, eczema or on frail skin
• Electrode position over areas where there is ischaemic tissue and/or thrombosis
Note: There are no known adverse effects of administering IFC / TENS on skin over or close to metal
implants. TENS / IFC can be used on the intact skin overlying implants containing metal, plastic, or
cement. Persons with joint replacements that include metal components have been treated with
electrostimulation with benefit and without adverse reactions.
Precautions TENS and IFC
Caution and precaution should be taken in case of:
• Areas with abnormal skin sensation (dysaesthesia)
o hypereasthesia (allodynia / hyperalgesia)
o hypoeasthesia
• Contact dermatitis
• Pregnant women
• Patients sensitive to autonomic reactions of TENS (e.g. nausea, light-headedness and fainting)
Potential adverse effects
Skin irritation and etching beneath the electrodes have been reported with the use of therapeutic
electrical stimulation.
Isolated cases of skin irritation may occur in patients with particularly sensitive skin. In case of an
allergic reaction to the electrode gel, suspend the treatment and contact a specialist. If during the
treatment signs of tachycardia and extrasystole appear, suspend the treatment and contact your
physician.

Page 20 of 52 EN109-1634750-40 IFU
9 Precautionary instructions
If the use of this device may have caused or contributed to an undesirable event such as
death or serious injury to the user, the manufacturer AND the competent authority of the
Member State MUST be notified immediately!
This device should be kept out of the reach of children.
The patient and the device must be in sight of the therapist at all times.
The device is not intended for use in so-called "wet rooms" (hydrotherapy rooms).
This equipment is not suitable for use in the presence of flammable anesthetics mixture with
air, oxygen, or nitrous oxide.
Do not expose the device to direct sunlight, heat radiated from a heat radiator, excessive
amounts of dust, moisture, vibrations and mechanical shocks.
This device should be used only under the continued supervision of a physician or licensed
practitioner.
In case any damage is noticed after unpacking the device, please immediately contact your
local distributor. DO NOT USE the device!
The unit should be installed in such a way, that its warmth can be passed on to the
surroundings.
Use of any other cable other than the supplied cable is strictly PROHIBITED as it
affects patient safety and the proper function of the device.
Before connection of this unit to the mains supply, check that the mains voltage and frequency
stated on the identification plate of this apparatus corresponds with that of the mains supply.
To avoid the risk of electric shock, this equipment must only be connected to a supply mains
with protected earth.
Do not use the device after extreme temperature fluctuations!
Before starting the treatment please make sure: you have read and understood the content of
this manual
Before starting the treatment please make sure: you strictly follow the WARNINGS and
CAUTIONS mentioned under precautionary instructions
Before starting the treatment please make sure: you have checked the patient for any possible
contra-indications.
Connection of accessories other than the ones supplied by the manufacturer can adversely
affect the safety of the patient and correct functioning of the equipment, and is therefore not
permitted.
To prevent infection, electrodes and sponge pads should not be used on broken skin.
During treatment, the patient may not feel unpleasant sensations amounting to pain. A mild
sensation of excitation is permissible.
If, as result of treatment, headache, vertigo, fatigue and/or other (autonomic nervous)
reactions develop, subsequent treatment should be given at a lower intensity.
It is recommended that diathermy machines (such as shortwave and microwave devices) are
kept at least one metre away from electrostimulation devices as the output of
electrostimulation devices can be affected by close proximity to an operating (pulsed)
shortwave or microwave machine.
Stimulation should not be applied across or through the head, directly on the eyes, covering
the mouth, on the front of the neck (especially the carotid sinus), or from electrodes placed
on the chest and the upper back or crossing the heart.
Application of electrodes near the thorax may increase the risk of cardiac fibrillation.
Simultaneous connection of a patient to a high frequency surgical medical electrical
equipment may result in burns at the site of the stimulator electrodes and possible damage
to the stimulator.

Page 21 of 52 EN109-1634750-40 IFU
Any electrodes that have current densities exceeding 2 mA/cm² may require the special
attention of the operator.
Repeated use of pre-gelled electrodes leads to rapid loss of conductivity and deteriorating
adhesiveness.
The loss of adhesion and drying of the gel will cause the edges to begin lifting which can
dramatically increase current density; cause uneven distribution of current across the
electrode surface, increasing the risk of burn; and potentially result in electrode movement.
Changes that occur in self-adhesive electrodes over time result in an unsafe situation where
skin irritation and patient discomfort can occur.
Self-adhesive electrodes should never be shared between patients.
Clean the device and its accessories regularly to maintain hygienic safety.
Before performing any user maintenance, switch off the device and disconnect the plug from
the mains supply.
Do not spray the cleaning agent directly on the glass panel.
Do not use cleaning agents that contain strong alkalis, lye, acid, detergents with fluoride or
detergents with ammonia.
Do not allow any liquids to penetrate the device or its accessories while cleaning and
disinfecting!
Dry all sockets and connectors that have become wet before any further use!
Mechanical shocks /or vibrations MUST be avoided while cleaning the device
Do not drop the device.
The device should not be used when mechanical damage is noticed. This includes damaged
cable insulation.
In the event that an error message or warning appears, immediately stop all use of the device.
Shutdown and restart the device. If the problem persists contact the supplier or Enraf-Nonius
B.V. for service. Errors and warnings indicate an internal problem with the device that must be
tested by a field service technician certified by Enraf-Nonius B.V before any further operation
or use of the system.
Use of a device that indicates an error or warning may pose a risk of injury to the patient,
user, or extensive internal damage to the system.
In case of display failure or other obvious defects, unplug the device immediately and notify a
certified service technician.
In the case of ingress of liquids, unplug the device from the Mains supply and have it checked
by an authorized person.
Opening of the equipment by unauthorized agencies is not allowed and will terminate any
claim to warranty.
The manufacturer will not be held responsible for the results of maintenance or repairs by
unauthorized persons!
Only service Technicians authorized by Enraf-Nonius can perform maintenance or modify this
equipment according to Service Information.
Maintenance shall not be performed on the equipment when equipment is in use or
connected to a patient.
It is recommended to have the Endomed 182 checked yearly by authorized personnel of
Enraf-Nonius or by its authorized distributor.
Medical electrical devices such as the Endomed 182 are subject to special precautions with
regard to electromagnetic compatibility (EMC) and must be installed and commissioned in
accordance with the EMC advice given in the instructions for use.
Use of this equipment adjacent to or stacked with other equipment should be avoided because
it could result in improper operation. If such use is necessary, this equipment and the other
equipment should be observed to verify that they are operating normally.

Page 22 of 52 EN109-1634750-40 IFU
Use of accessories, transducers and cables other than those specified or provided by the
manufacturer of this equipment could result in increased electromagnetic emissions or
decreased electromagnetic immunity of this equipment and result in improper operation.
Portable RF communications equipment (including peripherals such as antenna cables and
external antennas) should be used no closer than 30 cm to any part of the Endomed 182,
including cables specified by the manufacturer. Otherwise degradation of the performance of
this equipment could result.
The Endomed 182 should only be operated with the original power cable specified in the list
of contents delivered. Operating the device with any other power cable can lead to increased
emissions or reduced interference immunity of the device.

Page 23 of 52 EN109-1634750-40 IFU
10 Operation
Set up
Do not use the device after extreme temperature fluctuations!
Frequently Used Functions
Selecting the Clinical Protocols (only applies to Endomed 182 Type 2 and 3), Favorite and Manual
Operation buttons in the touch screen.
Switch On
• Switch the unit On by pushing the On/Off Button at the back of the unit.
• After switching on the device, a welcome screen will be displayed while the device performs a
self-test.
• At the end of the self-test the device enters the Home Menu and is ready for use.
When the unit is switched on all vital functions are controlled via an internal microprocessor. During
the functioning of the unit the actual output of the current is measured continuously and compared
to the requested output. Whenever a faulty situation is detected the unit will switch off the current
immediately.
Navigation
Home Menu
The Home menu gives access to all functions of the unit. The Home menu provides a structured
access to all therapies available within the unit, with appropriate parameter defaults. The Endomed
182 is equipped with touch screen technology. Just select a menu item by touching the button to
navigate to the next screen. You can navigate back to the previous screen by touching the back
button at the top of the screen.
• Select “Clinical Protocols”
to start working with
preset protocols. This does
not apply to Endomed 182
Type 1.
• Select “Favorites” to use a
manually saved protocol
• Select “Manual Operation”
to set all parameters
manually
• Select “System Settings” to
enter the settings menu
Endomed 182 Type 1 home
menu
Endomed 182 Type 2 and 3
home menu

Page 24 of 52 EN109-1634750-40 IFU
System Settings
Select System Settings in the Home Menu, to adjust various settings, check the software version or
restore the device to factory defaults. The options Acoustic Feedback, Buzzer Tone and Buzzer
Duration are only available in the Endomed 182 Type 2 and 3.
Set Language
1) Select “System Settings”
2) Select “Language”
3) Select the preferred
language with the
buttons.
4) Push OK to confirm and to
return to the previous menu
Set Brightness
To change the Brightness of
the screen:
1) Select “Brightness”
2) Adjust the brightness via
the buttons.
Range: 10 – 100%
3) Push OK to confirm and to
return to the previous menu

Page 25 of 52 EN109-1634750-40 IFU
System Info
1) Select “System Info”
In the next screen information
about the unit can be found.
The currently installed
software version is shown.
2) Push BACK to return to the
previous menu
Acoustic Feedback
Endomed 182 Type 2 and 3:
Select this option to turn on
or off audio signals at the end
of treatment.
1) Select “Acoustic Feedback”
2) Turn Acoustic Feedback On
or Off
3) Push BACK to return to the
previous menu

Page 26 of 52 EN109-1634750-40 IFU
Buzzer Tone and Buzzer Duration
Endomed 182 Type 2 and 3:
1) Select “Buzzer Tone” or
“Buzzer Duration”
Buzzer Tone provides access to
7 different tunes to signal the
end of a treatment.
Buzzer Duration provides
access to 7 different intervals
to signal the end of a
treatment.
Maintenance
Restore Factory Defaults will
delete any favorites stored on
the device and clear any
system settings, returning the
device in its original factory
state.
The Service menu is intended
for Enraf-Nonius qualified
service organizations and can
only be entered with an
access code.
Tank Cleaning will activate the
pump. See chapter 12
Maintenance and
troubleshooting. (Applies only
to Endomed 182 Type 3.)
1) Select “Maintenance”
(Applicable for Endomed 182
Type 2 and 3)

Page 27 of 52 EN109-1634750-40 IFU
Manual Operation Endomed 182 Type 1
The Endomed 182 Type 1 has one output channel. See chapter 11 for connection of electrodes.
1) Select “Manual Operation” in
the Home Screen
Select (K) to set treatment time
Select (L) to set intensity
2) Set treatment time
Option: 3 s / 10 s / 60 s
Or via the buttons
3) Set intensity
Option: 1 mA / 3 mA / 5 mA
Or via the buttons
4) Press the Start button (or the
foot switch when connected) to
start treatment
5) Press the Stop button (or the
foot switch when connected) to
stop treatment.
Treatment stops automatically
when the treatment time has
elapsed.
K
L

Page 28 of 52 EN109-1634750-40 IFU
Clinical Protocols
For the Endomed 182 Type 2 and 3 a list of common electrotherapy treatments can be found under
Clinical Protocols. These evidence-based protocols have been created by professional and expert
operators after years of experience in the field.
The pre-set clinical protocols are adjustable and rewritable. See chapter 11 for connection of
electrodes.
1) Select “Clinical Protocols” in
the Home screen to activate
the list
2) Select the button to
scroll through the list.
3) Select icon for more
information about the
protocol
4) Select the chosen Clinical
Protocol to go to the
Parameter Screen
Protocol information screen
5) Touch the button to
scroll through the pages
6) Select OK to go to the
parameter screen or BACK to
return to the Clinical
Protocols menu

Page 29 of 52 EN109-1634750-40 IFU
7) The parameter screen shows
all parameters at a glance
8) The pre-set clinical protocol
parameters can be adjusted
9) Push the channel tab 1 or 2
at the bottom of the screen to
change the intensity level
10) Adjust the intensity level via
the buttons
11) Push OK to confirm and
return to the previous screen
12) The protocol will start after
setting the intensity level
13) The protocol can be
stopped by pressing the stop
icon (A) on the touchscreen.
The protocol stops
automatically when the
treatment time has elapsed.
A

Page 30 of 52 EN109-1634750-40 IFU
Manual Operation Endomed 182 Type 2 and Type 3
With Manual Operation personal parameter settings can be defined for electrotherapy.
The Endomed 182 Type 2 and 3 has two independent output channels. To select the output
channel, touch the channel tab on the bottom of the screen. See chapter 11 for connection of
electrodes.
1) Select “Manual Operation” in
the Home Screen
2) Select the desired Current
Wave Form; the parameter
screen will appear
3) Depending on the selected
Current Wave Form various
parameters can be set.
Setting Parameters: Frequency
1) Select Frequency (B)
2) Adjust Frequency via the
buttons
Range: 1 Hz – 200 Hz
3) Push OK to confirm and
return to the parameter
screen
B

Page 31 of 52 EN109-1634750-40 IFU
Setting Parameters: Burst Frequency
1) Select Burst Frequency (C)
2) Set Burst Frequency
Option: 1 Hz / 2 Hz / 4 Hz
3) Push OK to confirm and
return to the parameter
screen
Setting Parameters: Modulation Frequency
1) Select Modulation
Frequency (D)
2) Adjust Modulation
Frequency via the
buttons
Range: 1 Hz- 180 Hz
3) Push OK to confirm and
return to the parameter
screen
D
C

Page 32 of 52 EN109-1634750-40 IFU
Setting Parameters: Modulation Time
1) Select Modulation Time (E)
2) Set Modulation Time
Option:
1-1 seconds
6-6 seconds
1-30 seconds
3) Push OK to confirm and
return to the parameter
screen
Setting Parameters: Treatment Time
1) Select Treatment Time (F)
2) Set treatment time via the
buttons
Range: 0 to 60 minutes
3) Push OK to confirm and
return to the parameter
screen
E
F

Page 33 of 52 EN109-1634750-40 IFU
Setting Parameters: Vacuum Module
With the Endomed 182 Type 3
it is possible to use vacuum
electrodes
1) Select Vacuum (G)
2) Set vacuum parameters
Option: pulsed mode 1 Hz /
pulsed mode 2 Hz /
continuous
3) Adjust the pressure of the
vacuum cups via the
buttons
The vacuum cups are
automatically selected when
the pump starts to run
Setting Parameters: Intensity
1) Push the channel tab 1 or 2
(H) at the bottom of the screen
to set the intensity level (after
setting the treatment time)
2) Adjust the intensity level via
the buttons
3) Push OK to confirm and
return to the previous screen
4) The program will start after
setting the intensity level
5) The program can be stopped
by pressing the stop icon on
the touchscreen. The program
stops automatically when the
treatment time has elapsed.
G
H

Page 34 of 52 EN109-1634750-40 IFU
Setting Parameters: Balance Control
For 4P Interferential the
balance control option is
available after Intensity has
been set.
With balance control the
intensity of Channel 1 relative
to Channel 2 can be increased
or decreased. An increase of
the intensity of Channel 1 will
automatically decrease the
intensity of Channel 2 and vice
versa.
1) Select Balance Control (I)
2) Set Balance Control
parameters
3) Push OK to confirm and
return to the parameter screen
Setting Parameters: Vector View
For 4P Isoplanar Vector a
vector view screen is available
after treatment has started.
1) Select Vector View (J)
In this screen an animation of
rhythmic shrinking and
swelling rings can be seen as
well as the remaining
treatment time and intensity
level.
I
J

Page 35 of 52 EN109-1634750-40 IFU
Favorites
Prior to the execution of a modified clinical protocol or manual setting, it can be saved for later use
under favorites.
When all parameters in the treatment screen are completely set as required, you can choose to save
the settings as favorites by pressing the store button.
Favorites can be stored as long as treatment has not been started.
1) Push Store (M) to save the
program settings
2) Select the program number
via the buttons
20 store locations are available
for the Endomed 182
3) Push OK to confirm
4) Enter a name for your
favorite
5) Push OK to save the favorite
M

Page 36 of 52 EN109-1634750-40 IFU
Loading and Deleting Favorites
1) Select “Favorites” in the
Home menu
2) To load a program select a
Favorite via the buttons
The parameter screen will
appear
3) To delete a Favorite press
the delete button (N) and
select the Favorite to be
removed via the buttons
4) Press OK to permanently
delete the Favorite
N

Page 37 of 52 EN109-1634750-40 IFU
11 Application information
Before starting the treatment please make sure: you have read and understood the content of
this manual.
Before starting the treatment please make sure: you strictly follow the WARNINGS and
CAUTIONS mentioned under precautionary instructions.
Before starting the treatment please make sure: you have checked the patient for any possible
contra-indications.
Connection of accessories other than the ones supplied by the manufacturer can adversely
affect the safety of the patient and correct functioning of the equipment, and is therefore not
permitted.
To prevent infection, electrodes and sponge pads should not be used on broken skin.
During treatment, the patient may not feel unpleasant sensations amounting to pain. A mild
sensation of excitation is permissible.
If, as result of treatment, headache, vertigo, fatigue and/or other (autonomic nervous)
reactions develop, subsequent treatment should be given at a lower intensity.
It is recommended that diathermy machines (such as shortwave and microwave devices) are
kept at least one metre away from electrostimulation devices as the output of
electrostimulation devices can be affected by close proximity to an operating (pulsed)
shortwave or microwave machine.
Stimulation should not be applied across or through the head, directly on the eyes, covering
the mouth, on the front of the neck (especially the carotid sinus), or from electrodes placed
on the chest and the upper back or crossing the heart.
Application of electrodes near the thorax may increase the risk of cardiac fibrillation.
Simultaneous connection of a patient to a high frequency surgical medical electrical
equipment may result in burns at the site of the stimulator electrodes and possible damage
to the stimulator.
Any electrodes that have current densities exceeding 2 mA/cm² may require the special
attention of the operator.
Connection of electrodes
See chapter 3 for description of numbered parts.
Endomed 182 Type 1
• Connect the DC reference [5] cable to connection [3]
• Connect the blank earth electrode [4] to the DC reference cable [5]
• Use of blank earth electrode: during treatment the patient needs to hold the blank earth
electrode by hand
• Connect the electrode holder [6] cable to connection [2]
• Attach the needle (not supplied) to the electrode holder through the thread system, which
allows the electrode holder to be opened, the needle to be inserted and the electrode holder to
be closed
• The needle holder is equipped with a start/stop button to begin or interrupt the flow of current
manually.

Page 38 of 52 EN109-1634750-40 IFU
Endomed 182 Type 2
• Connect the patient cables to connection 1 [10] and/or connection 2 [11] on the Current
Module [9] (red plug into red connection, black plug into black connection).
• Connect the electrodes to the patient cable.
Endomed 182 Type 3
• For use of adhesive or rubber electrodes: connect the patient cables to the upper connections
[15] on the Vacuum Module [13] and connect the electrodes to the patient cables (red plug into
red connection, black plug into black connection).
• For use of vacuum electrodes: connect the vacuum lead hoses to the lower connections [16] on
the Vacuum Module [13] and connect the vacuum electrodes to the vacuum lead hoses (red
plug into red connection, black plug into black connection).
Treatment
Before treatment
• The skin of the area in question is cleaned (removal of grease) with soap or 70 % alcohol
• Shaving hairy skin is recommended
• Test the sensitivity of the treatment area
• Position the electrodes and/or sponges (do not forget to moisten)
• Follow the operating instructions in chapter 10 on how to adjust the settings and start and stop
the treatment
During treatment
• Intensity is set at the desired level
• The patient is regularly asked to report any sensations felt. If necessary, the treatment is
modified.
Ending treatment
• Treatment can be stopped by pressing the stop icon on the touchscreen. Treatment stops
automatically when the treatment time has elapsed.
After treatment
• Remove the electrodes and/or sponges
• Clean the patient’s skin with a towel or tissue
• The expected effects are checked (e.g. pain, circulation, and mobility)
• The patient is asked to comment subsequently on any reactions that may occur
Endomed 182 Type 1:
Percutaneous Electrolysis
Percutaneous Electrolysis (PE) is a non-pharmacologic, minimally-invasive treatment technique for
chronic tendinopathies and has few side effects compared to pharmaceutical intervention. PE is
generally well tolerated by most patients, and complications and adverse events are extremely rare.
However, patients should be informed of the potential risks associated with the application of
Percutaneous Electrolysis:
• The treatment might produce mild pain that normally lasts 48 to 72 hours
one of the most common intervention-related side effect is discomfort in the treatment area, caused
by the insertion of the needle. During the applications of galvanic current, the patients may
experience moderate to strong pain (depending on intensity used. Anesthetics are usually not locally
injected before percutaneous electrolysis, since the procedure is generally well-tolerated by patients
(the galvanic current application can be stopped at any time if the pain is not bearable). Besides, the

Page 39 of 52 EN109-1634750-40 IFU
use of syringes to introduce the anesthetics would substantially increase the overall invasiveness of
the intervention. However, the use of anesthetics remains a considerable option.
• Vasovagal reactions during and immediately after the intervention
Percutaneous Electrolysis affects the autonomous nervous system. As in any procedure involving
needling, vagal reactions (such as paleness, sweating, piloerection, and coldness in the skin) have
been reported during PE. There are several studies that include information on the potential risk of
possible vasovagal reactions. These reactions may be widely justified by the effect of needling and
not only by that of the current.
• Bleeding in area of needle insertion
After the treatment, a compressive bandage may be applied but this is normally not necessary.
The use of ice or intake of any anti-inflammatory drugs (NSAIDs) 72 hours after treatment is not
recommended as this would counter the anticipated therapeutic effect (initiate a controlled
inflammatory process).
Acupuncture needle
The use of high-quality, single-use, sterile acupuncture needles that have medical CE approval,
including the Notified Body number, is recommended. Enraf-Nonius does not supply any needles.
The needle should be compatible with the application of ultrasound guided electrolysis. For as far
as it concerns needle dimensions, always be sure to select the correct needle thickness and length
for the type of injury to treat.
• Needle diameter: 0.30 mm – 0.35 mm
• Handle outer diameter: 1.25 mm – 1.45 mm
• Needle body length: 20 mm – 100 mm
• Handle length: 25 mm – 30 mm
Foot switch
The Endomed 182 Type 1 has an optional foot switch which can be connected to connection A [7]
(see chapter 3).
Place the footswitch so that it can be reached easily during
treatment. The footswitch control unit is multi-directional so it is
not necessary to align the footswitch exactly.
To avoid damage, please note that only slight pressure needs to
be exerted on the switch. Use the front part of your foot, not the
heel to operate the footswitch.
Press the footswitch once to activate treatment. Press the
footswitch again to stop treatment.

Page 40 of 52 EN109-1634750-40 IFU
Endomed 182 Type 2 and 3:
TENS / IFC
Protocol for the safe application of TENS / IFC
• Check contraindications with patient
• Test skin for normal sensation using blunt/sharp test
• Device should be switched off and electric leads disconnected
• Set electrical characteristics of TENS / IFC while device is switched off
• Connect electrodes to pins on lead wire and position electrodes on patient’s skin
• Ensure device is still switched off and connect the electrode wire to the device
• Switch the device on
• Gradually (slowly) increase the intensity further until the patient experiences a strong but
comfortable tingling sensation
• This intensity should not be painful or cause muscle contraction
Protocol for the safe termination of TENS / IFC
• Gradually (slowly) decrease the intensity until patient experiences no tingling sensation
• Switch the device off
• Disconnect the electrode from the device
• Disconnect electrodes from the pins on lead wire
• Remove the electrodes from the patient’s skin
Endomed 182 Type 2 and 3:
Flexible rubber electrodes
We recommend using the flexible rubber electrodes in combination with the supplied sponge pads.
When properly moistened, the sponge pads ensure low impedance between the skin and the
stimulator during treatment and they are easily cleaned afterwards. Follow the guidelines below
when using these electrodes.
• Prior to initial use thoroughly rinse the sponge pads in warm tap water to remove the
impregnating agent.
• Before application, saturate the sponge pads with tap water. Preferred is to use a saline solution
instead because of the improved electrical conduction.
• The supplied sponge pads have three layers. With AC currents, apply one sponge layer between
the skin and the electrode for minimum resistance.
• Fix the electrode/sponge pad assembly to the patient using the supplied fixation straps.
Depending on the electrode size, use two or three wraps to maximize the contact surface. See
the illustrations below.
Wrong application of fixation straps, resulting
in poor electrical conductivity.
Correct application of fixation straps, resulting in good
electrical conductivity.

Page 41 of 52 EN109-1634750-40 IFU
• It is important that electrodes remain in complete contact without edges lifting throughout the
treatment.
• The Endomed 182 output mode is Constant Current (CC). This will maintain the set current
amplitude, even when the impedance of the sponge pads increases during treatment caused by
water evaporation.
• Keep the sponge pads well moistened (close to dripping when lightly squeezed) during
treatment. Remoisten when treatment exceeds 10 minutes.
• After use clean the sponge pads as described under “cleaning and disinfection”.
Endomed 182 Type 2 and 3:
Self-adhesive electrodes
Repeated use of pre-gelled electrodes leads to rapid loss of conductivity and deteriorating
adhesiveness.
The loss of adhesion and drying of the gel will cause the edges to begin lifting which can
dramatically increase current density; cause uneven distribution of current across the
electrode surface, increasing the risk of burn; and potentially result in electrode movement.
Changes that occur in self-adhesive electrodes over time result in an unsafe situation where
skin irritation and patient discomfort can occur.
Self-adhesive electrodes should never be shared between patients.
Self-adhesive electrodes have higher series impedance than flexible rubber electrodes. This can
cause the stimulator to terminate treatment at higher current amplitudes. When this occurs, it is
recommended to continue the treatment with flexible rubber electrodes, combined with properly
moistened sponge pads.

Page 42 of 52 EN109-1634750-40 IFU
Endomed 182 Type 3:
Vacuum electrodes
There is a choice of large, medium and small electrodes. The areas of the electrodes correspond to
those of the 4 x 6 cm, 6 x 8 cm and 8 x 12 cm flexible rubber electrodes. The vacuum electrodes are
sufficiently flexible to ensure optimum contact with the skin, but rigid enough to prevent any
changes in the contour of the part being treated, allowing full advantage to be taken of the
massage effect of the pulsed vacuum.
The massage effect resulting from the pulsed vacuum ensures a good blood flow through the skin
under the electrodes. This reduces the resistance of the skin and increases he effectiveness of the
stimulation current.
• Choose the appropriate electrode size for the body part to be treated
• Dampen the sponges. Squeeze them slightly to remove excess water, and place them in the
vacuum electrodes
• Select constant vacuum, this will ease the positioning of the electrodes
• Place the vacuum electrodes on a smooth surface (e.g. on a table)
• Turn the vacuum intensity up a little, so as to create a vacuum in the electrodes
• Now move the electrodes one by one from the smooth surface to the body of the patient
• Set the vacuum intensity to the desired value
• Follow the operating instructions in chapter 10 on how to adjust the settings and start and stop
the treatment
• Correct the vacuum intensity if necessary; a low vacuum is sufficient
• If required, select pulsed vacuum
Keep the sponge pads well moistened (close to dripping when lightly squeezed) during treatment.
Remoisten when treatment exceeds 10 minutes. After use clean the sponge pads as described
under Cleaning and Disinfection.
• When you use only one vacuum channel, close the other channel with one of the vacuum
cables not in use.
Continuous or pulsed vacuum
When a continuous vacuum is used, the vacuum pulse switches off as soon as the selected vacuum
pressure is reached, making the Vacuum Module virtually silent in operation. A control system
ensures that the vacuum remains constant. The pump switches on for short intervals during the
treatment to maintain the vacuum.
When pulsed vacuum is used, the pump is switched on and off intermittently. The pulsating rhythm
of the vacuum massage is continuously or pulsating (two possibilities) adjustable. Pulsating vacuum
is very useful for patients who are sensitive to the electric current, as the sensation of the current
tends to be suppressed.

Page 43 of 52 EN109-1634750-40 IFU
Current density
In the particular standard for Electrical Nerve and Muscle Stimulators, IEC 60601-2-10, it is
recommended not to exceed a current density of 2 mA r.m.s. / cm², otherwise skin irritations or
etching can occur.
To find the maximum recommended current amplitude in mA for the Interferential current
waveforms, multiply the electrode surface in cm² by two. For all other current waveforms, the
stimulator output current can never exceed 50 mA r.m.s. This implies that with an electrode surface
of 25 cm² the current density can never exceed 2 mA r.m.s. / cm². As a rule of thumb for smaller
electrodes, such as the 3.2 mm self-adhesives, the maximum current setting available on the
stimulator for a given current waveform should proportionally be reduced.
For a precise calculation of the r.m.s. value of a pulsed current waveform the following formula can
be used:
Note that electrodes should be placed with care, ensuring good electrical contact over the entire
electrode surface, and that the use of small electrodes in combination with high intensities may
cause skin irritations or etching.
Connection and disconnection reactions
Constant Current (CC) output characteristics may cause unpleasant connection and disconnection
reactions if the electrodes are not securely placed or lose contact with the skin. Make sure the
current amplitude is set to 0 mA when you apply or remove the electrodes.

Page 44 of 52 EN109-1634750-40 IFU
12 Maintenance and troubleshooting
Cleaning and Disinfection
Clean the device and its accessories regularly to maintain hygienic safety.
Before performing any user maintenance, switch off the device and disconnect the plug from
the mains supply.
Do not spray the cleaning agent directly on the glass panel.
Do not use cleaning agents that contain strong alkalis, lye, acid, detergents with fluoride or
detergents with ammonia.
Do not allow any liquids to penetrate the device or its accessories while cleaning and
disinfecting!
Dry all sockets and connectors that have become wet before any further use!
Mechanical shocks /or vibrations MUST be avoided while cleaning the device
Do not drop the device.
Device
To clean the unit, turn it off and unplug the power supply. Clean the unit with a
damp cloth. Do not use abrasive cleaners. A small amount of mild household
cleaning agent may be used, if needed.
Display Panel
The display panel contains an anti-reflective coating, which needs special care
when cleaned. Use a soft and dry cotton cloth or micro fiber tissue to clean the
panel. To remove fingerprints or grease, use a non-abrasive glass cleaning
agent. Apply a small amount of the cleaning agent to a soft cotton cloth and
then carefully clean the panel.
Electrodes,
electrode holder,
sponges and
accessories
Between patient uses, the rubber electrodes should be cleaned with lukewarm
water. To disinfect the electrodes or to remove stubborn stains of dirt, use a 70%
alcohol solution. The alcohol solution can cause the black color of the rubber
electrodes to be stained, but this does not affect the operation of the electrodes.
Between patient uses, the sponge pads should be washed in running tap water,
thoroughly drained and then dried. Damaged sponge pads should be replaced.
It is recommended that a sufficient amount of sponges be available to enable
complete drying before re-use – this will limit growth of water-borne bacteria.
When the electrodes are not being used, the sponge pads should be removed.
This increases the operational life of the rubber electrodes. We advise that you
keep an extra set of sponge pads in stock.
The blank earth electrode can be cleaned with a damp cloth. Use soap and
lukewarm water or alcohol solution.
The electrode holder can be cleaned with a damp cloth. Use lukewarm water
and a non-abrasive, non-invasive household cleaning agent or alcohol solution.
Do not put in autoclave.
Patient cable
and
DC reference
cable
Clean the patient cable with a damp cloth. Use lukewarm water and a non-
abrasive household cleaning agent. Do not use an alcohol solution. Check the
cable regularly for damages and/or bad electrical contact. We advise, keeping a
spare patient cable in stock.

Page 45 of 52 EN109-1634750-40 IFU
Vacuum
electrodes and
sponges
The vacuum electrodes and sponges should be cleaned with lukewarm water.
In the case of persistent dirt, and for disinfection, a 70% alcohol solution may
be used.
Sponges should be replaced regularly. It is recommended to keep sponges
and a spare electrode in stock.
Calcium scale can be deposited on the metal surfaces of the electrodes. This
has an insulating effect. In order to maintain optimum conductivity, these
surfaces should be regularly cleaned and polished.
Vacuum cables
Clean the vacuum cable with a damp cloth. Do not use an alcohol solution.
Check the cable regularly for damages and/or bad electrical contact. We
advise, keeping a spare vacuum cable in stock.
Cleaning the
water reservoir
and hoses
• Detach the vacuum cups from the vacuum cables.
• Place a container filled with a cleaning liquid (*) below the system.
• Place the peripheral ends of the cables in the container.
• Go to System Settings, Maintenance and select Tank Cleaning.
• The water reservoir will be filled with the cleaning liquid until the water
reservoir is full.
• Empty the water reservoir as described below (water reservoir full).
(*) The following registered products may be used for disinfecting the water reservoir:
BAKTONIL, BAKTOLAN to 5%, CHINOSOL to 1%, CHLORAMIN solution, DETTOL, ELMOCID Gamma
to 2%, PERODIN, ZEPHIROL to 5%.
Observe the application information of the corresponding manufacturer.
Troubleshooting
The device should not be used when mechanical damage is noticed. This includes damaged
cable insulation.
In the event that an error message or warning appears, immediately stop all use of the device.
Shutdown and restart the device. If the problem persists contact the supplier or Enraf-Nonius
B.V. for service. Errors and warnings indicate an internal problem with the device that must be
tested by a field service technician certified by Enraf-Nonius B.V before any further operation
or use of the system.
Use of a device that indicates an error or warning may pose a risk of injury to the patient,
user, or extensive internal damage to the system.
In case of display failure or other obvious defects, unplug the device immediately and notify a
certified service technician.
In the case of ingress of liquids, unplug the device from the Mains supply and have it checked
by an authorized person.

Page 46 of 52 EN109-1634750-40 IFU
Error messages
When the device is turned on, it will first execute a self-test. When an error is detected, both during
the self-test and during normal operation, a pop-up screen will appear on the display. When the
error is displayed, all outputs will be disabled. When this situation occurs, switch off the unit and
disconnect all accessories. Wait approximately 15 seconds and switch the unit back on.
When the error re-appears, stop using the device and contact the supplier.
Device needs to cool down before you can proceed
The temperature of the device is too high to start treatment. Remove the device from any potential
heat sources (such as direct sunlight) and let the device cool down. Restart the device to continue.
Insufficient or no output current
• Check the patient cable for breaks or poor contact.
• Ensure that the sponges are sufficiently damp.
• Clean the electrodes
• Check for poor contact
• In areas where the water is soft, it is possible that the water may conduct poorly resulting in
abnormally low currents. In this case it is possible to use a saline solution to improve the
conductivity of the water.
Water reservoir full
The water separation tank of the Vacuum Module is full. Continue the treatment with the standard
electrodes or empty the tank as follows:
• Set power line switch [17] Off (0).
• Detach the hose from the outermost hose nipple [21] and empty the reservoir.
• Reattach the hose to the hose nipple.
• Set power line switch [17] On (1).
Vacuum leak
There probably is a leak in the vacuum system. This error is usually preceded by a continuously
running pump trying to reach the set vacuum. To protect the system, the pump is automatically
stopped after a certain amount of time. Inspect the vacuum cables and electrodes, set the vacuum
back to zero and try again. If the failure persists, stop using the device and contact your supplier.

Page 47 of 52 EN109-1634750-40 IFU
It is also recommended that a service history record is maintained. In some countries, this is even
obligatory.
On request a service manual can be made available containing: spare part list, descriptions,
calibration instructions and other information which will assist the user’s qualified technical
personnel to repair those parts of the equipment which are designated by the manufacturer as
repairable.
Expected Service Life
This device will remain suitable for its intended use as long as it is subjected to yearly maintenance
by a qualified service engineer as described in the service manual.
The service engineer will decide whether the device is suitable for use according to the specifications.
End of Life
The Endomed 182 contains materials which can be recycled and/or are noxious for the environment.
Technical Maintenance
Opening of the equipment by unauthorized agencies is not allowed and will terminate any
claim to warranty.
The manufacturer will not be held responsible for the results of maintenance or repairs by
unauthorized persons!
Only service Technicians authorized by Enraf-Nonius can perform maintenance or modify this
equipment according to Service Information.
Maintenance shall not be performed on the equipment when equipment is in use or
connected to a patient.
It is recommended to have the Endomed 182 checked yearly by authorized personnel of
Enraf-Nonius or by its authorized distributor.
Please ensure that you are well informed of the local rules and regulations regarding the
removal of equipment and accessories.

Page 48 of 52 EN109-1634750-40 IFU
13 Specifications
Technical data
Electrical info
Mains voltage
100 - 240 Volt
Frequency
50/60 Hz
Max. power output
50 VA
Dimensions (width x length x height)
Endomed 182 Type 1
14.5 x 17 x 9 cm
Endomed 182 Type 2
14 x 16 x 14 cm
Endomed 182 Type 3
14 x 22.5 x 17.5 cm
These values represent the dimensions of the
housings without communication cables, electrodes
or hose.
Weight Unit
Endomed 182 Type 1
710 gram
Endomed 182 Type 2
1460 gram
Endomed 182 Type 3
2750 gram
These values represent the weight of the housings
without electrodes and power cords.
Specifications Type 1
Channels
1
Output
Constant Current
Direct Current
Polarity
Negative
Intensity
0 – 15 mA
Treatment time
0 – 300 seconds
Specifications Type 2 and 3
Channels
2
Output
Constant Current
Intensity
0 -100 mA
Timer
0 – 60 min (in steps of 1 min)
2 pole interferential
Carrier wave
4 kHz
AMF frequency
1 – 200 Hz
Modulation frequency
0 – 180 Hz
Modulation program
1-1, 6-6, 1-30 seconds
4 pole interferential and isoplanar vector
Carrier wave
4 kHz
AMF frequency
1 – 200 Hz
Modulation frequency
0 – 180 Hz
Modulation program
1-1, 6-6, 1-30 seconds

Page 49 of 52 EN109-1634750-40 IFU
Asymmetrical biphasic pulsed current (TENS)
Pulse width
150 μs
Frequency
1 – 200 Hz
Modulation frequency
0 – 180 Hz
Modulation program
1-1, 6-6, 1-30 seconds
Burst frequency
1-2-4 Hz
Technical modifications reserved
Safety and performance standards
Medical device classification
IIa; Rule 9 Annex IX of 93/42/EEC
This equipment complies with all requirements of the
Medical Device Directive (93/42/EEC).
Safety class according to IEC 60601-1
Electrical safety class I
Mode of operation
Continuous
Applied parts
Type BF Applied part for electrotherapy.
Essential Performance
The essential performance is based on the standard 60601-2-10 where the maximum output of the
current and pulse energy is specified. Considering the different therapy forms, the essential
performance is built out of five requirements:
1) The maximum TENS current rms may not exceed 50 mA.
2) The maximum Interferential current rms may not exceed 100 mA.
3) The maximum TENS pulse energy may not exceed 300 mJ.
4) The maximum Interferential pulse energy may not exceed 300 mJ.
5) The maximum Direct current rms may not exceed 80 mA
The electrotherapy outputs shall remain within 20% of the set value.
Since the device is not life supporting it is allowed to fall into a safe state (no output) requiring
operator intervention to restart.
Environmental conditions
Environmental conditions for transport and storage
Environmental temperature:
–20° to +70° C
Relative humidity:
10 to 90% (non-condensing)
Atmospheric pressure:
500 to 1060 hPa
Environmental conditions normal use
Environmental temperature:
10° to 40° C
Relative humidity:
10 to 90 % (non-condensing)
Atmospheric pressure:
800 to 1060 hPa

Page 50 of 52 EN109-1634750-40 IFU
EMC Details
Medical electrical devices such as the Endomed 182 are subject to special precautions with
regard to electromagnetic compatibility (EMC) and must be installed and commissioned in
accordance with the EMC advice given in the instructions for use.
Use of this equipment adjacent to or stacked with other equipment should be avoided because
it could result in improper operation. If such use is necessary, this equipment and the other
equipment should be observed to verify that they are operating normally.
Use of accessories, transducers and cables other than those specified or provided by the
manufacturer of this equipment could result in increased electromagnetic emissions or
decreased electromagnetic immunity of this equipment and result in improper operation.
Portable RF communications equipment (including peripherals such as antenna cables and
external antennas) should be used no closer than 30 cm to any part of the Endomed 182,
including cables specified by the manufacturer. Otherwise degradation of the performance of
this equipment could result.
The Endomed 182 should only be operated with the original power cable specified in the list
of contents delivered. Operating the device with any other power cable can lead to increased
emissions or reduced interference immunity of the device.
The Endomed 182 is classified as a Group 1, Class B device according to CISPR 11.
The Endomed 182 is suitable for use in a professional healthcare facility environment. The device
uses RF energy solely for its internal functioning. Therefore, its RF emissions are very low and are
not likely to cause any interference in nearby electronic equipment.
The Endomed 182 has been tested according to the 60601-1-2 standard by an accredited lab and
found to be compliant for each emissions and immunity standard or test.

Page 51 of 52 EN109-1634750-40 IFU
14 Contact
For assistance, please visit our website http://www.enraf-nonius.com
The latest version (in electronic or printed format) of this Instructions for Use can be obtained free
of charge from our website www.enraf-nonius.com or by contacting distributor or by calling the
telephone number: +31-(0)10-2030600. The Instructions for Use will be sent (free of charge) to you
within 7 (seven) calendar days.
15 Product liability
A law on Product Liability has become effective in many countries. This Product Liability law implies,
amongst other things, that once a period of 10 years has elapsed after a product has been brought
into circulation, the manufacturer can no longer be held responsible for possible shortcomings of
the product.
To the maximum extent permitted by applicable law, in no event will Enraf-Nonius or its suppliers
or resellers be liable for any indirect, special, incidental or consequential damages arising from the
use of or inability to use the product, including, without limitation, damages for loss of goodwill,
work and productivity, computer failure or malfunction, or any and all other commercial damages
or losses, even if advised of the possibility thereof, and regardless of the legal or equitable theory
(contract, tort or otherwise) upon which the claim is based. In any case, Enraf-Nonius entire liability
under any provision of this agreement shall not exceed in the aggregate the sum of the fees paid
for this product and fees for support of the product received by Enraf-Nonius under a separate
support agreement (if any), with the exception of death or personal injury caused by the negligence
of Enraf-Nonius to the extent applicable law prohibits the limitation of damages in such cases.
The opposing party (product’s user or its representative) shall disclaim Enraf-Nonius from all claims
arising from third parties, whatever nature or whatever relationship to the opposing party.

EN109-1634750-40
Copyright:
Enraf-Nonius B.V.
Vareseweg 127 | 3047 AT | Rotterdam | The Netherlands
Tel: +31 (0)10-20 30 600 | [email protected]

Pagina 1 van 52 NL109-1634750-40 IFU
Endomed 182
NL109-1634750-40 IFU
21 September, 2020
Gebruiksaanwijzing

Pagina 2 van 52 NL109-1634750-40 IFU
Inhoudsopgave
1 Introductie ......................................................................................................................................................... 3
2 Symbolen ........................................................................................................................................................... 7
3 Apparaatcomponenten ................................................................................................................................. 9
4 Inhoud van de verpakking ........................................................................................................................ 13
5 Installatie ......................................................................................................................................................... 15
6 Beoogd gebruik en beoogd gebruiker ................................................................................................ 16
7 Indicaties ......................................................................................................................................................... 17
8 Contra-indicaties .......................................................................................................................................... 18
9 Voorzorgsmaatregelen .............................................................................................................................. 20
10 Bediening ........................................................................................................................................................ 23
11 Toepassingsinformatie ............................................................................................................................... 37
12 Onderhoud en verhelpen van verstoringen ....................................................................................... 44
13 Specificaties .................................................................................................................................................... 48
14 Contact ............................................................................................................................................................. 51
15 Productaansprakelijkheid .......................................................................................................................... 51

Pagina 3 van 52 NL109-1634750-40 IFU
1 Introductie
Voorwoord
Dank u voor de aanschaf van de Endomed 182.
De Endomed 182, ontworpen en geproduceerd door Enraf-Nonius B.V., biedt een nieuwe dimensie
in electrotherapie, mogelijk gemaakt door geavanceerd hard- en software ontwerp. Het resultaat is
een apparaat met een buitengewone veelzijdigheid, gebaseerd op eenvoud van bediening.
Deze handleiding is geschreven voor de eigenaars en gebruikers van de Endomed 182. Om het
gebruik, de efficiëntie en de levensduur van uw apparaat te optimaliseren dient u deze handleiding
zorgvuldig door te lezen en vertrouwd te raken met de bedieningsorganen en de accessoires
voordat u het apparaat bedient.
Apparaatbeschrijving
De Endomed 182 is een op netspanning werkende elektrostimulator, uitgerust met een full-colour
aanraakscherm. De grafische gebruikersinterface zorgt voor maximaal bedieningsgemak.
De Endomed 182 is beschikbaar in drie versies:
De Endomed 182 Type 1 is een op netspanning werkende elektrostimulator met één kanaal voor de
toepassing van percutane elektrolyse (PE) door middel van gelijkstroom (DC) met lage intensiteit.
Endomed 182 versies
Naam:
Endomed 182 Type 1
Endomed 182 Type 2
Endomed 182 Type 3
Artikel nummer:
1634903
1634901
1634902
Artikel nummer
basis unit:
1634910
1634900
1634900
Stroom
golfvormen:
Gelijkstroom
TENS
• continue bifasische pulsstroom
(conventionele TENS modus)
• pulstrein van bifasische
pulsstroom (Burst TENS
modus)
Interferentie Stroom (IFC)
• 2-polig interferentie
(bipolaire) modus
• 4-polig interferentie
(tetrapolaire) modus
• 4-polig interferentie
(tetrapolair) met Isoplanaire
Vector
TENS
• continue bifasische pulsstroom
(conventionele TENS modus)
• pulstrein van bifasische
pulsstroom (Burst TENS
modus)
Interferentie Stroom (IFC)
• 2-polig interferentie
(bipolaire) modus
• 4-polig interferentie
(tetrapolaire) modus
• 4-polig interferentie
(tetrapolair) met Isoplanaire
Vector
Vacuüm
Kanalen:
1
2
2
Voorgeprogram-
meerde
behandelings-
protocollen:
-
16
16

Pagina 4 van 52 NL109-1634750-40 IFU
Bij PE wordt de gelijkstroom (ook wel Galvanische stroom genoemd) toegediend via een naald die in
de naaldhouder van een handstuk (de ‘applicator’ of kathode) is geplaatst. De retourelektrode (of
anode) is een handelektrode (vastgehouden door de patiënt) of een andere naald, afhankelijk van de
uit te voeren behandeling.
In de naaldhouder van de applicator (handstuk) kunnen acupunctuurnaalden (steriel, voor éénmalig
gebruik en weg te werpen) van verschillende lengten en diameters worden geplaatst, wat nodig is
voor goede plaatsing in de verschillende lichaamsdelen (afhankelijk van de te behandelen
aandoening).
Het handstuk is voorzien van een start/stopknop waarmee de stroom handmatig kan worden
aangezet of onderbroken.
Het instrument geeft een constante gelijkstroom af met een maximale output van 15 mA.
Op de grafische gebruikersinterface zijn de volgende behandelparameters te zien: huidig
outputniveau (mA), ingestelde tijd voor de toepassing, geleverde stroom (mC).
De gebruiker kan het outputniveau van de stroom (mA) en de toepassingstijd instellen en aanpassen,
afhankelijk van het type behandeling.
Het instrument heeft geen vooraf ingesteld klinisch protocol, maar de behandelparameters kunnen
als favorieten worden ingesteld en opgeslagen (persoonlijke instellingen), als snelle referentie voor
toekomstige therapiesessies.
Het instrument is compact en wordt geleverd met de volgende accessoires: netspanningskabel en
verbindingskabels, handstuk (applicator), retourelektrode, voetschakelaar (optioneel) en
productdocumentatie. Verbruiksmaterialen zoals wegwerpbare (acupunctuur)naalden worden niet bij
het product geleverd.
Enraf-Nonius B.V levert geen percutane elektroden of wegwerpbare acupunctuurnaalden.
De Endomed 182 Type 2 en 3 beschikken over 16 vooraf ingestelde klinische protocollen voor
TENS en interferentiestroom. De individuele behandelparameters kunnen handmatig worden
ingesteld en aangepast door de bediener. Alle behandelparameters kunnen als favorieten worden
ingesteld en opgeslagen (persoonlijke instellingen), als referentie voor toekomstige therapiesessies.
De Endomed 182 Type 3 is een samengestelde configuratie die bestaat uit een afzonderlijke,
gestapelde, vacuümzuigmodule en een elektrostimulator Endomed 182 Type 2. De vacuümmodule
wordt onder de stimulator geplaatst en hiermee verbonden. Doel van de module is het creëren van
een vacuüm waardoor de behandelaar de stimulatie-elektroden sneller en eenvoudiger op de
patiënt kan bevestigen. De bevestiging geschiedt door middel van zuignappen. De zuignappen
hebben geïntegreerde stimulatie-oppervlakken die de elektrostimulatie via vochtige sponzen
overbrengen op het doelweefsel.
Voor de Endomed 182 Type 2 en 3 kan de elektrische prikkeling op de huid worden toegepast met
behulp van oppervlakte-elektroden: flexibele, rubberen elektroden, zelfklevende elektroden of
vacuümelektroden (alleen type 3), met als doel de stimulatie van specifieke soorten zenuwvezels.
Enraf-Nonius biedt verschillende soorten en maten elektroden (van puntelektroden met een
oppervlak van 0,3 cm2 tot elektroden met een oppervlak van 96 cm2), passend bij de afmeting van
het te behandelen gebied of het verwachte behandeldoel.

Pagina 5 van 52 NL109-1634750-40 IFU
Beschrijving stroomvormen
TENS
De asymmetrische bifasische pulsvorm wordt vaak gebruikt bij TENS (transcutane elektrische
zenuwstimulatie). Deze golfvorm wordt gekenmerkt door variabele faseduur en variabele
pulsfrequentie. De typische amplitude, duur en stijg- en slinksnelheid van deze golfvorm zijn ten
opzichte van de basislijn voor elke fase ongelijk. De golfvorm is volledig gebalanceerd, m.a.w. de
lading van elke fase is gelijk. De bifasische aard van de puls betekent dat er geen netto-
gelijkspanningscomponent (nul netto-gelijkstroom) is, waardoor eventuele huidreacties als gevolg
van de opbouw van elektrolyten onder de elektroden tot een minimum worden beperkt.
Om gewenning aan stimulatie te voorkomen of
om de tolerantie van de
patiënt te verbeteren kan de pulsfrequentie via
frequentiemodulatie worden gevarieerd.
Asymmetrische bifasische stroomvorm TENS
Burst TENS
Burst TENS wordt toegepast als conventionele TENS niet effectief blijkt; dit is vooral geschikt voor
de behandeling van dieperliggende pijnlijke gebieden of bij chronische pijn. Burst TENS gebruikt
een relatief grote faseduur (150-200 μs), een lage burstfrequentie (1-5 Hz) en een hoge frequentie.
Krachtige, zichtbare contracties moeten optreden in de spieren waarvan de innervatie
correspondeert met die van het pijnlijke gebied.
Het verminderend effect op pijn treedt gewoonlijk pas na twintig tot dertig minuten op, in
tegenstelling tot het effect van conventionele TENS, dat meestal vrij snel optreedt. De effecten
houden echter aanzienlijk langer aan dan die van conventionele TENS nadat de stimulatie is
beëindigd. Het verminderend effect op pijn van burst TENS wordt veroorzaakt door de afgifte van
endorfinen op zowel spinaal als supraspinaal niveau.
Indien conventionele of Burst TENS geen of onvoldoende verlichting geeft, kan frequentiemodulatie
worden gebruikt. Frequentiemodulatie kan bovendien accommodatie voorkomen.
Interferentiestroom (IFC)
Bij het interferentiële stroomtype wordt een draaggolffrequentie van het middengebied gebruikt
om de laagfrequente prikkelfrequentie door de huid te sturen. De relatief lage weerstand van de
huid t.o.v. de draaggolffrequentie draagt bij aan het comfort voor de patiënt dat bij dit stroomtype
vaak wordt ervaren. Interferentiestromen zijn alle wisselspanningsstromen zonder
gelijkspanningscomponenten. Er zijn verschillende varianten van het interferentiële stroomtype
bekend, waarvan de volgende beschikbaar zijn bij de Endomed 182 Type 2 en 3: bipoliar,
tetrapolair, tetrapolair met isoplanaire vector.
Bipolaire methode
Bij deze methode worden twee elektroden gebruikt en
vindt de overlapping van de twee wisselstromen plaats
binnen het apparaat. De stroom die het apparaat
verlaat is een volledig gemoduleerde wisselstroom. Bij
de tweepolige methode is de modulatiediepte altijd
100%.
Bipolaire interferentie

Pagina 6 van 52 NL109-1634750-40 IFU
Tetrapolaire methode (Klassieke Interferentie)
Bij deze behandelingsmethode worden vier elektrodes
gebruikt en worden twee niet-gemoduleerde
stromen gegenereerd. De frequentie van het ene
kanaal is vastgesteld op de draaggolffrequentie terwijl
het andere kanaal een variabele frequentie heeft die is
gebaseerd op de instellingen voor
prikkelfrequentie en frequentiemodulatie. Interferentie
treedt daar op waar de twee stromen elkaar in het
weefsel kruisen. De modulatiediepte (die de
stroomamplitude van de stimulatie bepaalt) hangt af
van de richting van de stromen en kan variëren van 0
tot 100%. 100% modulatiediepte komt alleen voor bij
de diagonalen (en dus bij het kruispunt) van de twee
stromen. Dit is natuurlijk een theoretische situatie, die
is gebaseerd op de aanname dat het weefsel
homogeen is. In werkelijkheid is het weefsel echter
heterogeen, zodat de stroombalans tussen de twee
kanalen moet worden gebruikt om de 100%
modulatiediepte te verkrijgen. De stroombalans kan
ook worden gebruikt om verschillen in sensatie te
compenseren die onder de elektrodeparen optreden.
Bij de tetrapolaire methode, is de
modulatiediepte alleen 100% bij de
diagonalen.
Tetrapolaire methode met Isoplanaire vector
Met de Isoplanaire vector wordt de totale oppervlakte
tussen de 4 elektroden optimaal gestimuleerd. De
plaatsing van de elektroden kan eenvoudig en snel
gebeuren. De modulatiediepte is overal 100%.
Isoplanar Interferential kan gebruikt worden voor de
behandeling van problemen die zich in een groot
gebied bevinden en die zeer moeilijk te lokaliseren zijn.
Isoplanaire Interferentie wordt ook gebruikt als een
milde voorbehandeling. Na deze toepassing wordt de
behandeling voortgezet met een focus op een kleiner,
meer lokaal gebied.
Isoplanaire vector
Gelijkstroom
Gelijkstroom (DC) is een constante stroom die voor verschillende therapeutische doeleinden wordt
gebruikt binnen de geneeskunde. Met constante stroom wordt bedoeld dat de elektrische lading
via een stroomgeleider onafgebroken tussen twee punten (elektroden) met verschillende
potentialen (polariteit) stroomt, zonder dat deze van richting wisselt. In tegenstelling tot bij
wisselstroom stroomt de elektrische lading altijd in dezelfde richting.

Pagina 7 van 52 NL109-1634750-40 IFU
2 Symbolen
Symbolen
Beschrijving
Volg de instructies in de gebruiksaanwijzing.
Het is belangrijk dat u de preventieve veiligheids- en gebruiksinstructies
aandachtig doorleest en toepast.
Algemeen Verbodsteken.
Verbod betekent: "U MAG NIET ..."
Waarschuwing of Let op:
Geeft een gevaarlijke situatie aan welke, indien deze niet voorkomen wordt,
kan leiden tot:
a. Overlijden of ernstig letsel van de patiënt (of)
b. Klein tot middelgroot letsel van de patiënt (of)
c. Schade aan de apparatuur
Algemeen Verplichtsteken.
Verplichte actie betekent: "U moet ..."
Type BF toegepast onderdeel dat voldoet aan de gespecificeerde eisen om een
hogere mate van bescherming tegen elektrische schokken te bieden dan type
B toegepaste onderdelen.
Geeft de temperatuurlimieten aan waaraan het medische hulpmiddel veilig kan
worden blootgesteld.
Geeft de luchtvochtigheid aan waaraan het medische hulpmiddel veilig kan
worden blootgesteld.
Geeft de luchtvochtigheid aan waaraan het medische hulpmiddel veilig kan
worden blootgesteld.
Elektronisch afval – kan worden hergebruikt.
Geeft de elektrische en elektronische onderdelen van het apparaat aan die
kunnen worden gerecycled en die apart moeten worden afgevoerd.
Zorg dat het apparaat droog blijft.
Naam en adres van fabrikant en de productiedatum.
Referentie- of modelnummer.
Serienummer, gebruikt voor identificatie van het apparaat.
Wisselstroom

Pagina 8 van 52 NL109-1634750-40 IFU
Verbinding electrodekabel elektrotherapie
Verbindingen vacuümkabels elektrotherapie
“AAN” (stroom)
“UIT” (stroom)
Het CE-merkteken in combinatie met een nummer geeft aan dat deze in
overeenstemming is met de richtlijn van de Europese Raad aangaande
medische apparatuur en dat dit apparaat/hulpmiddel onder direct toezicht
staat van de aangemelde instantie.

Pagina 9 van 52 NL109-1634750-40 IFU
3 Apparaatcomponenten
Endomed 182 Type 1
Endomed 182 Type 2
7
8
1
9
1
2
1
3
1
1
4
1
6
1
5
1
10
11

Pagina 10 van 52 NL109-1634750-40 IFU
Endomed 182 Type 3
12
13
16
15
14
17
18
19
21
20

Pagina 11 van 52 NL109-1634750-40 IFU
Onderdelen Beschrijving
Genummerd
Onderdeel
Beschrijving
Doel
[1]
LCD Touch Screen
Kleuren display 4.3” met touchscreen.
Geeft de gebruikersinterface weer waarmee de
operator het apparaat kan bedienen en de
parameters van de behandelingsprotocollen kan
wijzigen.
[2]
Connectie Elektrodehouder
Connectie Elektrodehouder
[3]
Connectie blanke
aardelektrode
Aansluiting voor DC referentiekabel die aansluit
op de blanke aardelektrode
[4]
Blanke aardelektrode
Referentie electrode
[5]
DC referentiekabel
Retour elektrode aansluitkabel
[6]
Elektrodehouder
Handstuk voor naaldhouder
[7]
Aansluiting A
Aansluiting voor Vacuümmodule (Endomed 182
Type 3 / Voetschakelaar (Endomed 182 Type 1)
[8]
Aansluiting B
Aansluiting voor stroommodule
[9]
Stroommodule
Stroommodule met aansluiting voor kleef- en
rubberelektroden.
[10]
Aansluiting 1 Stroommodule
Aansluitkanaal 1 voor patiëntkabel voor kleef- en
rubberelektroden op Stroommodule Endomed
182.
[11]
Aansluiting 2 Stroommodule
Aansluitkanaal 2 voor patiëntkabel voor kleef- en
rubberelektroden op Stroommodule Endomed
182.
[12]
Vacuüm elektrodehouder
Houder voor vacuümelektroden.
[13]
Vacuümmodule
Vacuümmodule geïntegreerd met Endomed 182
met aansluitingen voor kleef- of rubberelektroden
en vacuümelektroden.
[14]
Vacuümmodule elektrode
kabels
Voor de juiste werking van de aansluitingen van
de Vacuümmodule moeten de elektrodekabels
van de Vacuümmodule worden aangesloten op
de Stroommodule [7] en [8] aansluiting.
[15]
Bovenste aansluting
Vacuümmodule
Aansluitingen kanaal 1 en 2 voor patiëntkabel
voor zelfklevende of rubberen elektroden op
Vacuümmodule.
[16]
Onderste aansluiting
Vacuümmodule
Aansluitingen kanaal 1 en 2 voor vacuümleiding
voor vacuümelektroden op Vacuümmodule.
[17]
Hoofdschakelaar
Om het apparaat aan of uit te zetten.
Bij uitzetten blijft het display no enige tijd
zichtbaar (energiezuinige methode).
[18]
Type label
Geeft informatie over het apparaat, zoals type en
serienummer.
[19]
Aansluiting voor netsnoer
Sluit hier de meegeleverde netsnoer aan om het
apparaat van stroom te voorzien.
[20]
Luchtuitlaat
Luchtuitlaat voor Vacuümmodule

Pagina 12 van 52 NL109-1634750-40 IFU
Onderdelen Beschrijving
Genummerd
Onderdeel
Beschrijving
Doel
[21]
Aansluiting voor waterreservoir
Deze aansluiting wordt gebruikt voor de
aansluiting van het waterreservoir. Er kan geen
vacuüm worden gecreëerd tenzij het
waterreservoir is aangesloten. Het waterreservoir
zorgt ervoor dat het overtollige water uit de
sponzen wordt opgevangen en niet via de pomp
kan worden weggeblazen. Het reservoir moet
dagelijks worden geleegd. Zie het hoofdstuk over
Onderhoud.

Pagina 13 van 52 NL109-1634750-40 IFU
4 Inhoud van de verpakking
Apparaat
De inhoud van het pakket is afhankelijk van het bestelde model. De volgende zijn beschikbaar:
Artikelnummer
Omschrijving
1634903
Endomed 182 Type 1
1634901
Endomed 182 Type 2
1634902
Endomed 182 Type 3 (bevat geïntegreerde vacuümmodule)
Standaard accessoires Endomed 182 Type 1
1634750
CD-ROM met Gebruiksaanwijzing (PDF op CD-ROM)
1634751
Informatieboekje
3444357
Netsnoer 250V/2,5A, 2,5 meter zwart
3444080
Electrodehouder
3444582
Blanke aardelektrode
3444677
DC referentiekabel
Standaard accessoires Endomed 182 Type 2 en Endomed 182 Type 3
1634750
CD-ROM met Gebruiksaanwijzing (PDF op CD-ROM)
1634751
Informatieboekje
3444357
Netsnoer 250V/2,5A, 2,5 meter zwart
3444021
Fixatieband 250x3 cm
3444020
Fixatieband 100x3 cm
3444129
(2x) Rubberelektrode 6x8 cm, 2 mm bus, set van 2 st.
1460266
Sponshoes voor rubberelektrode 6x8 cm, set van 4 st.
3444211
(2x) Patiëntenkabel, 2-aderig, 2 mm stekker - zwart, met gekleurde clips
Additionele standaard accessoires Endomed 182 Type 3
3444503
(2x) Vacuümelektroden Ø 60 mm, set van 2 st.
3444505
Sponsjes Ø 65 mm, set van 4 st. (voor vacuümelektrode Ø 60 mm)
3444507
(2x) Vacuümelektrodekabel rood
3444508
(2x) Vacuümelektrodekabel zwart
Optionele accessoires Endomed 182 Type 1
1634810
Voetschakelaar
Optionele accessoires Endomed 182 Type 2 en Endomed 182 Type 3
Kleefelektroden
3444056
EN-Trode Ø 3,2 cm, 2 mm bus, set van 10x4 st.
3444135
EN-Trode Ø 5,0 cm, 2 mm bus, set van 10x4 st.
3444057
EN-Trode 5x5 cm, 2 mm bus, set van 10x4 st.
3444058
EN-Trode 5x9 cm, 2 mm bus, set van 10x4 st.
3444222
Kleefelektroden Ø 2,0 cm, 2 mm bus, set van 10x8 st.
Rubber elektroden
3444128
Rubberelektrode 4x6 cm, 2 mm bus, set van 2 st.
3444129
Rubberelektrode 6x8 cm, 2 mm bus, set van 2 st.
3444130
Rubberelektrode 8x12 cm, 2 mm bus, set van 2 st.
3444380
Siliconen elektrode 5x5 cm

Pagina 14 van 52 NL109-1634750-40 IFU
Sponshoezen voor rubberelektroden
1460273
Sponshoes voor rubberelektrode 4x6 cm, set van 4 st.
1460266
Sponshoes voor rubberelektrode 6x8 cm, set van 4 st.
1460275
Sponshoes voor rubberelektrode 8x12 cm, set van 4 st.
Fixatiebanden
3444020
Fixatieband 100x3 cm
3444021
Fixatieband 250x3 cm
3444022
Fixatieband 100x5 cm
3444023
Fixatieband 250x5 cm
Puntelektroden
3444180
Puntelektrode (pen model), Ø 5 mm, aansluiting vrouwelijk 2 mm, incl 10
geleidende rubberen doppen
Adapters
2523523
Adapter van 2 mm bus naar 4 mm stekker, zwart
2523524
Adapter van 2 mm bus naar 4 mm stekker, rood
Patiëntenkabel
3444211
Patiëntenkabel, 2-aderig, 2 mm stekker - zwart, met gekleurde clips
Additionele optionele accessoires Endomed 182 Type 3
Vacuüm electrodes
3444503
Vacuum electrodes Ø 60 mm, set of 2
3444504
Vacuum electrodes Ø 90 mm, set of 2
3444509
Vacuum electrodes Ø 30 mm, set of 2
Sponsjes
3444505
Sponsjes Ø 65 mm, set van 4 st. (voor vacuümelektrode Ø 60 mm)
3444506
Sponsjes Ø 95 mm, set van 4 st. (voor vacuümelektrode Ø 90 mm)
3444516
Sponsjes Ø 30 mm, set van 4 st. (voor vacuümelektrode Ø 30 mm)
Vacuümelektrodekabel
3444507
Vacuümelektrodekabel rood
3444508
Vacuümelektrodekabel zwart
Bestelinformatie
Kijk voor bestelinformatie, standaardaccessoires en aanvullende accessoires voor de Endomed 182
en accessoires op de website www.enraf-nonius.com.

Pagina 15 van 52 NL109-1634750-40 IFU
5 Installatie
Inspectie
Als u transportschade constateert, neem dan onmiddellijk contact op met uw leverancier.
Gebruik het apparaat NIET!
Het apparaat moet zodanig worden geplaatst dat de warmte kan worden afgegeven aan de
omgeving.
Voer de volgende stappen meteen bij het uitpakken van het apparaat uit:
• Controleer de leveringsdocumenten om er zeker van te zijn dat de levering compleet is.
• Controleer of de verpakking alle artikelen bevat die worden vermeld in de lijst met
standaardtoebehoren (zie hoofdstuk 4 “Inhoud van de verpakking”).
• Controleer de externe onderdelen en accessoires op mogelijke schade door transport.
Uitpakken
De Endomed 182 wordt voor transport verpakt in één verpakking met vulling die speciaal
ontworpen is voor veilig vervoer en veilige opslag.
• Plaats de doos op een vlak oppervlak om het instrument uit de verpakking te verwijderen.
• Doe de bovenkant van de doos open en verwijder de polystyreenvulling.
• Wees voorzichtig bij het verwijderen van de inhoud uit de verpakking.
Apparaat setup
Endomed 182 Type 2:
• Sluit de kabel van de Stroommodule [9] aan op Aansluiting B [8].
Endomed 182 Type 3:
• Sluit de kabel van de Stroommodule [9] aan op Aansluiting B [8].
• Sluit de kabel van de Vacuümmodule [13] aan op Aansluiting A [7].
Zie hoofdstuk 3 - Apparaatcomponenten in deze handleiding.
Aansluiting op het lichtnet
Het gebruik van een andere kabel dan de meegeleverde kabel is strikt verboden, aangezien
deze invloed heeft op de veiligheid van de patiënt en de goede werking van het apparaat.
Controleer voor het aansluiten van het apparaat op het plaatselijke elektriciteitsnet of de op
het identificatieplaatje van het apparaat vermelde netspanning en -frequentie overeenkomen
met die van het plaatselijke elektriciteitsnet.
Om het risico van een elektrische schok te vermijden, mag deze apparatuur alleen worden
aangesloten op een stroomnet met beschermde aarde.
Sluit het apparaat aan op een stopcontact met behulp van de netkabel.
• Steek de netkabel in het aansluitpunt [19] en sluit deze aan op een stopcontact.
Ontkoppelen van het lichtnet
• Wanneer u klaar bent met de behandeling, schakelt u het apparaat uit door de aan-
/uitschakelaar op Uit te zetten.
• Haal de netkabel uit de stopcontact.
• Koppel de netkabel los van het aansluitpunt [19].

Pagina 16 van 52 NL109-1634750-40 IFU
6 Beoogd gebruik en beoogd gebruiker
Beoogd gebruik
Endomed 182 Type 1
De Endomed 182 Type 1 is een op netspanning werkende elektrostimulator met één kanaal, bedoeld
en ontworpen voor gebruik door zorgprofessionals voor de toepassing van percutane elektrolyse
(PE) door middel van gelijkstroom (DC) met lage intensiteit.
Endomed 182 Type 2 en 3
De Endomed 182 Type 2 en 3 zijn elektrostimulatoren met twee kanalen, bedoeld en ontworpen
voor gebruik door zorgprofessionals voor het uitoefenen van pijnbestrijding met IFC
(interferentiestroom) en TENS-stroom.
Met pijnbestrijding door middel van elektrostimulatie wordt bedoeld:
- Symptomatische verlichting van chronische, hardnekkige pijn
- Beheersing van pijn door posttraumatische of postoperatieve aandoeningen
- Verlichting van pijn door artritis
De elektrische prikkeling wordt op de huid toegediend met behulp van oppervlakte-elektroden met
als doel de stimulatie van specifieke soorten zenuwvezels. Pijnverlichting (pijnmodulatie) kan
worden bereikt door:
1. blokkeren van de informatie die zich verplaatst via de nociceptieve vezels (de vezels die een
pijnsensatie produceren) door stimulering van de afferente A-vezels met grote diameter;
2. afgifte van lichaamseigen opioïden door stimulatie van de afferente en motorische vezel met
kleine diameter.
Beoogd gebruiker
De Endomed 182 is bedoeld om te worden gebruikt, en mag uitsluitend worden gebruikt door of
onder toezicht van professionele gebruikers op het gebied van fysieke geneeskunde en revalidatie
in professionele zorginstellingen.
Aanvullend voor Endomed 182 Type 1:
Indien een zorgprofessional (fysiotherapeut, arts) bevoegd en bekwaam is in het gebruik van
gelijkstroom elektrolysetherapie met echogeleiding, dan is die zorgprofessional ook bevoegd en
bekwaam in:
-> het uitvoeren van naaldprikken op een patiënt;
-> het gebruik van echografie;
-> het gebruik van gelijkstroom elektrolysetherapie.

Pagina 17 van 52 NL109-1634750-40 IFU
7 Indicaties
Indicaties Endomed 182 Type 1
Percutane elektrolyse
Percutane elektrolyse (PE) kan worden toegepast voor de behandeling van de volgende
aandoeningen:
• Patellatendinopatie/patellapeestendinitis (‘springersknie’)
• Epicondylitis lateralis (tenniselleboog)
• Epicondylitis medialis (golferselleboog)
• Myofasciaal pijnsyndroom/triggerpoints
• Acuut whiplash-syndroom (AWS)
• Schouderaandoeningen (tendinopathieën van de rotatorenmanchet, subacromiaal
pijnsyndroom)
• Pubalgie (liespijn)
• Hamstringtendinopathie
• Achillespeestendinopathie
• Fasciitis plantaris/hielpijn
Indicaties Endomed 182 Type 2 en 3
TENS
Verlichting van acute pijn
• Postoperatieve pijn
o Abdominaal
o Thoracaal
o p.o. orthopedische pijn
• Bevallingspijn en pijn na de bevalling
• Dysmenorroe
• Orofaciale pijn, inclusief tandheelkundige ingrepen
• Fysiek trauma, inclusief gebroken ribben en kleine medische ingrepen
Verlichting van chronische pijn
• Onderrug pijn
• Artritische pijn, waaronder osteoartritis, reumatoïde artritis
• Spierpijn, inclusief myofasciale pijn, spierspanning, pijn na inspanning
• Neuropathische pijn, inclusief postamputatie (fantoompijn), postherpetische,
trigeminusneuralgie
• Kankerpijn, inclusief metastatische botpijn
• Complex regionaal pijnsyndroom
Interferentie stroom (IFC)
Verlichting van acute en chronische pijn, zoals:
• Postoperatieve pijn / orthopedische pijn
• Onderrug pijn
• Nekpijn
• Schouderpijn
• Artritische pijn, waaronder osteoartritis, reumatoïde artritis
• Spierpijn, inclusief myofasciale pijn, spierspanning, pijn na inspanning, en fibromyalgie
Spierstimulatie
• Versterking van spieren (in het algemeen)
• Fecale en urine-incontinentie
Darmstoornis
Verhoging lokale (cutane) doorstroming

Pagina 18 van 52 NL109-1634750-40 IFU
8 Contra-indicaties
De Endomed 182 MAG NIET worden gebruikt voor de onderstaande symptomen of
medische aandoeningen.
Contra-indicaties Endomed 182 Type 1
Contra-indicaties voor gebruik
• Infectieuze artritis
• Hartaandoeningen/hartritmestoornis
• Zwangerschap
• Huidzweren en andere huidinfecties
• Endoprothesen en/of osteosynthese
• Pacemakers
• Oncologische processen
• Tromboflebitis/voorgeschiedenis van veneuze insufficiëntie in de benen
• Stollingsstoornis/antistollingsmiddelen
• Bloedaandoeningen
• Menstruatie
• Naaldfobie
• Angst voor elektrische stimulatie
• Endocriene klieren
• Patiënten met verminderde gevoeligheid
• Patiënten met neurologische stoornissen van het centrale en perifere zenuwstelsel
• Patiënten met neurovegetatieve stoornissen
• Pediatrische patiënten
• Gecompliceerde medische aandoeningen
• Cognitieve beperking
• Drugs of alcoholmisbruik
Gebieden waar de behandeling niet moet worden toegepast:
• Bloedvaten
• Endocriene klieren
• Organen
• Perifere zenuwen (endoneurium)
• Hoofd, ogen, nek en thorax of bovenrug ter hoogte van het hart
Voorzorgsmaatregelen percutane elektrolyse
Gebieden die extra aandacht vereisen:
• Abdominaal gebied
• Intercostaal gebied (voorzorg tegen pneumothorax)
• Thoracaal gebied (voorzorg tegen pneumothorax)
• Thoracic outlet-gebied (voorzorg tegen pneumothorax)
• Inguinaal gebied, knieholte (voorzorg tegen beschadiging van neurovasculaire bundels)

Pagina 19 van 52 NL109-1634750-40 IFU
Contra-indicaties Endomed 182 Type 2 en 3
Absolute contra-indicaties:
• Ongediagnosticeerde pijn
• Actieve implantaten (incl. pacemakers en implanteerbare cardioverter-defibrillatoren - ICD's)
• Patiënten die de instructies van de behandelaar / fysiotherapeut niet begrijpen of die niet in
staat zijn om mee te werken
Relatieve contra-indicatiens (= locale contra-indicaties):
• Zwangerschap (niet toepassen op buik/bekkengebied)
• Maligniteit (niet toepassen op actieve maligniteit)
• Epilepsie (niet toepassen op de nek of hoofd)
• Hartaandoeningen zoals hartritmestoornissen (niet toepassen door de borst)
• Plaatsing van de elektroden rond de ogen
• Plaatsing van de elektrode over het anterieure aspect van de nek of sinus carotis
• Elektrodeplaatsing door de borst (d.w.z. anterieure en posterieure elektrodeposities)
• Plaatsing van de elektroden over de testikels
• Plaatsing van de elektroden over actieve epifysegebieden bij kinderen
• Plaatsing van de elektroden over beschadigde huid of open wonden
• Plaatsing van de elektroden over dermatologische laesies zoals dermatitis, eczeem of op een
tere huid
• Elektrodepositie over gebieden waar sprake is van ischemisch weefsel en/of trombose
Opmerking: Er zijn geen bekende nadelige effecten van het toedienen van IFC / TENS op de huid
over of in de buurt van metalen implantaten. TENS / IFC kan worden toegepast op de intacte huid
boven metaal, plastic of cement bevattende implantaten. Mensen met gewrichtsvervangingen met
metalen onderdelen zijn met gunstig gevolg en zonder bijwerkingen behandeld met
elektrostimulatie.
Voorzorgsmaatregelen TENS en IFC
Voorzichtigheid en voorzorg zijn geboden in geval van:
• Gebieden met een abnormaal huidgevoel (dysesthesie)
o hyperasthesie (allodynie / hyperalgesie)
o hypoeasthesie
• Contactdermatitis
• Zwangere vrouwen
• Patiënten die gevoelig zijn voor autonome reacties van TENS (bijv. misselijkheid, duizeligheid
en flauwvallen)
Potentiële negatieve effecten
Huidirritatie en etsing onder de elektroden zijn gemeld bij het gebruik van therapeutische
elektrische stimulatie.
Geïsoleerde gevallen van huidirritatie kunnen voorkomen bij patiënten met een bijzonder gevoelige
huid. In geval van een allergische reactie op de elektrodengel, de behandeling opschorten en
contact opnemen met een specialist. Als er tijdens de behandeling tekenen van tachycardie en
extrasystole optreden, schort u de behandeling op en neemt u contact op met uw arts.

Pagina 20 van 52 NL109-1634750-40 IFU
9 Voorzorgsmaatregelen
Als het gebruik van dit apparaat de oorzaak is van of bijgedragen heeft aan een ongewenst
voorval zoals overlijden of ernstig letsel van de gebruiker, dan MOETEN de fabrikant en de
bevoegde autoriteit van de lidstaat daarvan onmiddellijk op de hoogte worden gesteld!
Dit apparaat dient buiten bereik van kinderen te worden gehouden.
De patiënt en het apparaat moeten te allen tijde in het zicht van de therapeut zijn.
Gebruik dit apparaat niet in zogenaamde “natte ruimtes” (ruimten voor hydrotherapie).
Deze apparatuur is niet geschikt voor gebruik bij aanwezigheid van een ontvlambaar
anesthesiemengsel met lucht, zuurstof of lachgas.
Stel de unit niet bloot aan direct zonlicht, warmte van een radiator, overmatige hoeveelheden
stof, vocht, trillingen en mechanische schokken.
Dit apparaat dient alleen te worden gebruikt onder continue supervisie
van een bevoegd arts.
Als u transportschade constateert, neem dan onmiddellijk contact op met uw leverancier.
Gebruik het apparaat NIET!
Het apparaat moet zodanig worden geplaatst dat de warmte kan worden afgegeven aan de
omgeving.
Het gebruik van een andere kabel dan de meegeleverde kabel is strikt verboden, aangezien
deze invloed heeft op de veiligheid van de patiënt en de goede werking van het apparaat.
Controleer voor het aansluiten van het apparaat op het plaatselijke elektriciteitsnet of de op
het identificatieplaatje van het apparaat vermelde netspanning en -frequentie overeenkomen
met die van het plaatselijke elektriciteitsnet.
Om het risico van een elektrische schok te vermijden, mag deze apparatuur alleen worden
aangesloten op een stroomnet met beschermde aarde.
Gebruik het apparaat niet na extreme temperatuurschommelingen!
Zorg dat u het volgende hebt uitgevoerd voordat u de behandeling start: U hebt de inhoud
van deze handleiding gelezen en begrepen.
Zorg dat u het volgende hebt uitgevoerd voordat u de behandeling start: U volgt de
vermeldingen in de veiligheidsinstructies nauwgezet op.
Zorg dat u het volgende hebt uitgevoerd voordat u de behandeling start: U heeft de patiënt
gecontroleerd op mogelijke contra-indicaties
Het aansluiten van andere dan de door de fabrikant gespecificeerde accessoires kan de
veiligheid van de patiënt en het correct functioneren van de apparatuur nadelig beïnvloeden
en is daarom niet toegestaan.
Om infectie te voorkomen, dienen elektrodes en sponsjes niet op beschadigde huid te
worden gebruikt.
Tijdens de behandeling mag de patiënt geen onaangename sensaties voelen die leiden tot
pijn. Een licht gevoel van prikkeling is toegestaan.
Indien als gevolg van de behandeling hoofdpijn, duizeligheid, vermoeidheid en/of andere
(autonome nerveuze) reacties ontstaan, dient de behandeling in een lagere intensiteit te
worden uitgevoerd.
Het wordt aanbevolen om diathermiemachines (zoals kortegolf- en microgolfapparaten) op
minstens een meter afstand te houden van elektrostimulatieapparatuur, omdat de output van
elektrostimulatieapparatuur kan worden beïnvloed door de nabijheid van een werkende
(gepulseerde) kortegolf- of microgolfapparaat.
Stimulatie dient niet te worden toegepast over of door het hoofd, direct op de ogen, over de
mond, aan de voorkant van de nek (vooral de halsslagader), of door middel van elektroden
die op de borst en de bovenrug worden geplaatst of die het hart kruisen.
Toepassing van elektroden in de buurt van de borstkas kan het risico op hartfibrilleren
verhogen.

Pagina 21 van 52 NL109-1634750-40 IFU
Gelijktijdige aansluiting van een patiënt op een hoogfrequente chirurgische medische
apparatuur kan leiden tot brandwonden op de plaats van de stimulatorelektroden en
mogelijke schade aan de stimulator.
Elektroden met een stroomdichtheid van meer dan 2 mA/cm² vragen mogelijk de speciale
aandacht van de bediener.
Herhaaldelijk gebruik van voorgegeleerde elektroden leidt tot een snel verlies van
geleidbaarheid en een verslechterende kleefkracht.
Het verlies aan hechting en het drogen van de gel zal ervoor zorgen dat de randen beginnen
te liften, wat de stroomdichtheid dramatisch kan verhogen; kan een ongelijkmatige verdeling
van de stroom over het elektrodeoppervlak veroorzaken, waardoor het risico op
brandwonden toeneemt; en mogelijk leidt tot verplaatsing van de elektrode.
Veranderingen in de zelfklevende elektroden die in de loop van de tijd optreden, leiden tot
een onveilige situatie waarin huidirritatie en ongemak voor de patiënt kunnen optreden.
Zelfklevende elektroden mogen nooit worden gedeeld tussen patiënten.
Reinig het apparaat en de accessoires regelmatig om de hygiënische veiligheid te waarborgen.
Voordat u begint met reinigen, schakel het apparaat uit en haal de stekker uit het stopcontact.
Spuit het reinigingsmiddel niet rechtstreeks op het glazen paneel.
Gebruik geen reinigingsmiddelen die sterke alkaliën, loog of zuur bevatten en geen
reinigingsmiddelen die fluoride of ammoniak bevatten.
Zorg dat er geen vloeistoffen het apparaat of de accessoires kunnen binnendringen terwijl u
bezig bent met reinigen en desinfecteren!
Maak alle aansluitingen en connectoren droog als deze nat zijn geworden voordat u het
apparaat weer gaat gebruiken!
Mechanische schokken en/of trillingen moeten worden vermeden bij het reinigen van de
ultrageluid applicator!
Laat het apparaat niet vallen.
Het apparaat mag niet worden gebruikt wanneer er mechanische schade wordt opgemerkt.
Dit geldt ook voor beschadigde kabelisolatie.
In het geval dat er een foutmelding of waarschuwing verschijnt, dient u het gebruik van het
apparaat onmiddellijk te stoppen. Schakel het apparaat uit en start het opnieuw op. Indien
het probleem aanhoudt, neem dan contact op met de leverancier of met Enraf-Nonius B.V.
voor service. Foutmeldingen en waarschuwingen duiden op een intern probleem met het
apparaat dat op locatie moet worden getest door een door Enraf-Nonius B.V gecertificeerde
onderhoudsmonteur voordat u het systeem weer kunt bedienen of gebruiken. Een apparaat
dat een fout of een waarschuwing aangeeft, kan mogelijk letsel toebrengen aan de patient,
de gebruiker, of kan mogelijk leiden tot omvangrijke interne schade aan het systeem.
In geval van weergavestoringen of andere duidelijke defecten ontkoppelt u het apparaat
meteen en neemt u contact op met een gecertificeerde onderhoudsmonteur.
Bij het binnendringen van vloeistoffen dient u de stekker uit het stopcontact te halen en het
apparaat door een bevoegd persoon te laten controleren.
Het openen van de apparatuur door onbevoegden is niet toegestaan en beëindigt elke
aanspraak op garantie.
De fabrikant is niet verantwoordelijk voor de resultaten van onderhoud of reparaties door
onbevoegden.
Alleen door Enraf-Nonius B.V. geautoriseerde servicetechnici kunnen deze apparatuur
onderhouden of aanpassen aan de hand van de actuele service-informatie.
Voer geen onderhoud uit op het instrument als het instrument wordt gebruikt of op een
patiënt is aangesloten.
Het wordt aangeraden om de Endomed 182 jaarlijks te laten controleren door geautoriseerd
personeel van Enraf-Nonius of door haar geautoriseerde distributeur.
Voor medische elektrische apparaten zoals de Endomed 182 gelden speciale
voorzorgsmaatregelen met betrekking tot elektromagnetische compatibiliteit (EMC) en deze

Pagina 22 van 52 NL109-1634750-40 IFU
moeten geplaatst en in gebruik genomen worden in overeenstemming met het EMC-advies in
de gebruiksaanwijzing.
Het apparaat mag niet worden gebruikt direct geplaatst naast, of bovenop andere apparaten.
Als het apparaat moet worden gebruikt direct naast of bovenop andere apparaten, moet het
apparaat worden gecontroleerd om ervoor te zorgen dat het zoals beschreven funktioneert.
Het gebruik van accessoires, zenders en kabels anders dan gespecificeerd of geleverd door de
fabrikant van deze apparatuur kan leiden tot verhoogde elektromagnetische emissies of
verlaagde elektromagnetische immuniteit van dit apparaat, wat kan leiden tot onjuist
functioneren.
Draagbare RF-communicatieapparatuur (met inbegrip van randapparatuur zoals antennekabels
en externe antennes) mag niet minder dan 30 cm verwijderd zijn van enig onderdeel van de
Endomed 182, inclusief de door de fabrikant gespecificeerde kabels. Anders kunnen de
prestaties van deze apparatuur afnemen.
De Endomed 182 mag alleen worden gebruikt met de originele netsnoer vermeld op de lijst
inhoud van de verpakking. Bediening van het apparaat met een ander netsnoer kan leiden tot
hogere emissies of verminderde immuniteit van het apparaat.

Pagina 23 van 52 NL109-1634750-40 IFU
10 Bediening
Klaarzetten
Gebruik het apparaat niet na extreme temperatuurschommelingen!
Veelgebruikte functies
Het selecteren van de knoppen Klinische Protocollen (alleen van toepassing op Endomed 182 Type
2 en 3), Favorieten en Handmatige Bediening in het aanraakscherm.
Aanzetten
• Schakel het apparaat in door op de aan/uit-knop aan de achterkant van het apparaat te
drukken.
• Na het inschakelen wordt het apparaat geïnitialiseerd en verschijnt er een welkomstscherm
terwijl het apparaat een zelftest uitvoert.
• Aan het einde van de zelftest komt het apparaat in het toegangscodescherm.
Als het apparaat is ingeschakeld worden alle essentiële functies aangestuurd door een interne
microprocessor. Tijdens de werking van de eenheid wordt de stroomoutput voortdurend gemeten
en vergeleken met de gevraagde output. Zodra er een fout wordt gedetecteerd, schakelt het
apparaat de stroom onmiddellijk uit.
Navigatie
Hoofdmenu
Het hoofdmenu geeft toegang tot alle functies van het apparaat. Het hoofdmenu biedt een
gestructureerde toegang tot alle beschikbare behandelingen van de eenheid, met passende
parameterstandaardinstellingen. De Endomed 182 is uitgerust met aanraakscherm-technologie.
Kies gewoon een menu-onderdeel door op de knop te drukken en navigeer naar het volgende
scherm. U kunt terug naar het vorige scherm navigeren door de toets "Terug" bovenaan het scherm
aan te raken.
• Selecteer “Klinische
Protocollen” om met
vooraf ingestelde
protocollen te werken. Dit
is niet van toepassing op
Endomed 182 Type 1.
• Selecteer "Favorieten" om
een handmatig
opgeslagen protocol te
gebruiken.
• Selecteer "Handmatige
bediening" om alle
parameters handmatig in
te stellen.
• Selecteer "Systeem-
instellingen" om het
instellingenmenu te
openen.
Endomed 182 Type 1
hoofdmenu
Endomed 182 Type 2 en 3
hoofdmenu

Pagina 24 van 52 NL109-1634750-40 IFU
Systeeminstellingen
Selecteer Systeeminstellingen in het Hoofdmenu, om verschillende instellingen aan te passen, de
softwareversie te controleren of het apparaat te herstellen naar de fabrieksinstellingen. De opties
Akoestische terugkoppeling, Zoemertoon en Zoemer duur zijn alleen beschikbaar in de Endomed
182 Type 2 en 3.
Instellen Taal
1) Selecteer “Systeem
instellingen”
2) Selecteer “Taal”
3) Selecteer de gewenste taal
met de knoppen.
4) Druk op OK om te
bevestigen en terug te keren
naar het vorige menu.
Instellen Schermhelderheid
Aanpassen van de
schermhelderheid:
1) Selecteer
“Schermhelderheid”
2) Pas de helderheid aan via
de knoppen.
Bereik: 10 – 100%
3) Druk op OK om te
bevestigen en terug te keren
naar het vorige menu.

Pagina 25 van 52 NL109-1634750-40 IFU
Systeeminformatie
1) Selecteer “Systeem Info”
In het volgende scherm vindt
u informatie over het
apparaat.
De actuele geïnstalleerde
softwareversie wordt getoond.
2) Druk op Terug om terug te
keren naar het vorige menu.
Akoestische terugkoppeling
Endomed 182 Type 2 en 3:
Selecteer deze optie om
audiosignalen aan het einde
van de behandeling in of uit
te schakelen.
1) Selecteer “Akoestische
terugkoppeling”
2) Schakel de akoestische
terugkoppeling aan of uit.
3) Druk op TERUG om terug
te keren naar het vorige
menu.

Pagina 26 van 52 NL109-1634750-40 IFU
Zoemertoon en Zoemer duur
Endomed 182 Type 2 en 3:
1) Selecteer “Zoemertoon” of
“Zoemer duur”
Met Zoemertoon zijn 7
verschillende tonen in te stellen
om het einde van een
behandeling aan te geven.
Met Zoemer duur zijn 7
verschillende intervallen in te
stellen om het einde van een
behandeling aan te geven.
Onderhoud
Herstel Fabrieksinstellingen
zal alle favorieten die op het
apparaat zijn opgeslagen
verwijderen en alle
systeeminstellingen wissen,
waardoor het apparaat weer
in de oorspronkelijke
fabrieksinstelling komt te
staan.
Het Service Menu is bedoeld
voor door Enraf-Nonius
gekwalificeerde service
organisaties en kan alleen met
een toegangscode betreden
worden.
Waterreservoir reinigen
zal de pomp activeren. Zie
hoofdstuk 12 Onderhoud en
probleemoplossing. (Alleen
van toepassing op Endomed
182 Type 3.)
1) Selecteer “Onderhoud”
(Van toepassing op Endomed
182 Type 2 en 3)

Pagina 27 van 52 NL109-1634750-40 IFU
Handmatige Bediening Endomed 182 Type 1
Endomed 182 Type 1 heeft één uitgangskanaal. Zie hoofdstuk 11 voor aansluiten van elektroden.
1) Selecteer “Hand bediening”
in het Hoofdmenu
Selecteer (K) om Behandeltijd in te
stellen
Selecteer (L) om Intensiteit in te stellen
2) Stel de Behandeltijd in
Opties: 3 s / 10 s / 60 s
Of via de toetsen
3) Stel de Intensiteit in
Opties: 1 mA / 3 mA / 5 mA
Of via de toetsen
4) Druk op de Startknop (of de
voetschakelaar als deze is
aangesloten) om de
behandeling te starten.
5) Druk op de Stop-knop (of de
voetschakelaar als deze is
aangesloten) om de
behandeling te stoppen.
De behandeling stopt
automatisch wanneer de
behandelingstijd is verstreken.
K
L

Pagina 28 van 52 NL109-1634750-40 IFU
Klinische Protocollen
Voor de Endomed 182 Type 2 en 3 is een lijst van veel voorkomende electrotherapiebehandelingen
te vinden onder Klinische Protocollen. Deze evidence-based protocollen zijn opgesteld door
professionele en deskundige operators na jarenlange ervaring in het veld.
De vooraf ingestelde klinische protocollen zijn aanpasbaar en herschrijfbaar. Zie hoofdstuk 11 voor
aansluiten van elektroden.
1) Selecteer “Klinische
Protocollen” in het
Hoofdmenu om de lijst te
activeren
2) Druk op de toesten
om door de lijst te gaan.
3) Selecteer het icoon voor
meer informatie over het
protocol
4) Selecteer het gekozen
Klinisch Protocol om naar het
Parameterscherm te gaan.
Protocol informatie scherm
5) Druk op de knoppen
om door de lijst te gaan
6) Selecteer OK om naar het
parameterscherm te gaan of
TERUG om naar het Klinische
Protocollen scherm te gaan

Pagina 29 van 52 NL109-1634750-40 IFU
7) Het behandelscherm toont
alle parameters in één
oogopslag
8) De vooraf ingestelde
klinische protocolparameters
kunnen worden aangepast
9) Druk op het kanaaltabblad 1
of 2 aan de onderkant van het
scherm om de Intensiteit te
wijzigen.
10) Pas de Intensiteit aan via de
toetsen
11) Druk op OK om te
bevestigen en terug te keren
naar het vorige scherm.
12) Het protocol start na het
instellen van de Intensiteit.
13) Het protocol kan worden
gestopt door op het stop-
icoon (A) op het
aanraakscherm te drukken. Het
protocol stopt automatisch
wanneer de behandelingstijd is
verstreken.
A

Pagina 30 van 52 NL109-1634750-40 IFU
Handmatige Bediening Endomed 182 Type 2 en Type 3
In de handmatige bediening kunnen persoonlijke parameterinstellingen worden ingesteld voor
elektrotherapie. De Endomed 182 Type 2 en 3 heeft twee onafhankelijke uitgangskanalen. Druk op
het kanaaltabblad aan de onderkant van het scherm om het uitgangskanaal te selecteren. Zie
hoofdstuk 11 voor aansluiten van elektroden.
1) Selecteer “Handmatige
bediening” in het
Hoofdscherm.
2) Selecteer de gewenste
Stroomvorm; het
behandelscherm verschijnt
3) Afhankelijk van de
geselecteerde Stroomvorm
kunnen verschillende
parameters worden ingesteld.
Instellen Parameters: Frequentie
1) Selecteer Frequentie (B)
2) Stel Frequentie in via de
toetsen
Bereik: 1 Hz – 200 Hz
3) Druk op OK om te
bevestigen en terug te keren
naar het behandelscherm
B

Pagina 31 van 52 NL109-1634750-40 IFU
Instellen Parameters: Burst Frequentie
1) Selecteer Burst Frequentie
(C)
2) Stel Burst Frequentie in
Opties: 1 Hz / 2 Hz / 4 Hz
3) Druk op OK om te
bevestigen en terug te keren
naar het behandelscherm
Instellen Parameters: Modulatie Frequentie
1) Selecteer Modulatie
Frequentie (D)
2) Stel Modulatie Frequentie
in via de toetsen
Bereik: 1 Hz- 180 Hz
3) Druk op OK om te
bevestigen en terug te keren
naar het behandelscherm
D
C

Pagina 32 van 52 NL109-1634750-40 IFU
Instellen Parameters: Modulatietijd
1) Select Modulatietijd (E)
2) Stel Modulatietijd in
Optie:
1-1 seconden
6-6 seconden
1-30 seconden
3) Druk op OK om te
bevestigen en terug te keren
naar het behandelscherm
Instellen Parameters: Behandeltijd
1) Selecteer Behandeltijd (F)
2) Stel Behandeltijd in via de
toetsen
Bereik: 0 to 60 minuten
3) Druk op OK om te
bevestigen en terug te keren
naar het behandelscherm
E
F

Pagina 33 van 52 NL109-1634750-40 IFU
Instellen Parameters: Vacuümmodule
Met de Endomed 182 Type 3
is het mogelijk om vacuüm-
elektroden te gebruiken.
1) Selecteer Vacuüm (G)
2) Stel vacuüm parameters in
Optie: gepulseerde modus 1
Hz / gepulseerde modus 2 Hz
/ continu
3) Stel de druk van de
vacuüm- zuignappen in via de
toetsen
De vacuümzuignappen
worden automatisch
geselecteerd wanneer de
pomp begint te lopen.
Instellen Parameters: Intensiteit
1) Druk op het kanaaltabblad 1
of 2 (H) aan de onderkant van
het scherm om de Intensiteit in
te stellen (na het instellen van
de behandelingstijd)
2) Stel de Intensiteit in via de
toetsen
3) Druk op OK om te
bevestigen en terug te keren
naar het behandelscherm
4) Het programma start na het
instellen van de Intensiteit
5) Het programma kan worden
gestopt door op het stop-icoon
op het aanraakscherm te
drukken. Het programma stopt
automatisch wanneer de
behandelingstijd is verstreken.
G
H

Pagina 34 van 52 NL109-1634750-40 IFU
Instellen Parameters: Balans Controle
Voor 4P Interferentie is de
Balance Controle optie
beschikbaar nadat de
Intensiteit is ingesteld.
Met de Balans Controle kan de
intensiteit van Kanaal 1 ten
opzichte van Kanaal 2 worden
verhoogd of verlaagd. Een
verhoging van de intensiteit
van Kanaal 1 zal automatisch
de intensiteit van Kanaal 2
verlagen en vice versa.
1) Selecteer Balans Controle (I)
2) Stel Balans Controle
parameters in
3) Druk op OK om te
bevestigen en terug te keren
naar het behandelscherm
Instellen Parameters: Vector View
Voor 4P Isoplanaire Vector is
een vector view scherm
beschikbaar nadat de
behandeling is gestart.
1) Selecteer Vector View (J)
In dit scherm is een animatie
te zien van ritmische
krimpende en zwellende
ringen en de resterende
behandeltijd en intensiteit.
I
J

Pagina 35 van 52 NL109-1634750-40 IFU
Favorieten
Voorafgaand aan de uitvoering van een gewijzigd klinisch protocol of handmatige instelling kan
deze worden opgeslagen voor later gebruik onder favorieten.
Wanneer alle parameters in het behandelingsscherm volledig naar wens zijn ingesteld, kunt u
ervoor kiezen om de instellingen op te slaan als favorieten door op de bewaarknop te drukken.
Favorieten kunnen worden opgeslagen zolang de behandeling niet is gestart.
1) Druk op de bewaarknop (M)
om de programma instellingen
op te slaan
2) Selecteer het programma
nummer via de toetsen
20 bewaarlocaties zijn
beschikbaar voor de Endomed
182
3) Druk op OK om te
bevestigen
4) Voer een naam in voor de
favoriet
5) Druk op OK om de favorite
op te slaan
M

Pagina 36 van 52 NL109-1634750-40 IFU
Laden en Verwijderen van Favorieten
1) Selecteer “Favorieten” in het
Hoofdmenu
2) Om een programma te
laden, selecteer een Favoriet
via de toetsen
Het behandelscherm verschijnt
3) Om een Favoriet te
verwijderen, druk op de
Verwijder knop (N) en selecteer
de te verwijderen Favoriet via
de knoppen
4) Druk op OK om de Favoriet
permanent te verwijderen
N

Pagina 37 van 52 NL109-1634750-40 IFU
11 Toepassingsinformatie
Zorg dat u het volgende hebt uitgevoerd voordat u de behandeling start: U hebt de inhoud
van deze handleiding gelezen en begrepen.
Zorg dat u het volgende hebt uitgevoerd voordat u de behandeling start: U volgt de
vermeldingen in de veiligheidsinstructies nauwgezet op.
Zorg dat u het volgende hebt uitgevoerd voordat u de behandeling start: U heeft de patiënt
gecontroleerd op mogelijke contra-indicaties
Het aansluiten van andere dan de door de fabrikant gespecificeerde accessoires kan de
veiligheid van de patiënt en het correct functioneren van de apparatuur nadelig beïnvloeden
en is daarom niet toegestaan.
Om infectie te voorkomen, dienen elektrodes en sponsjes niet op beschadigde huid te
worden gebruikt.
Tijdens de behandeling mag de patiënt geen onaangename sensaties voelen die leiden tot
pijn. Een licht gevoel van prikkeling is toegestaan.
Indien als gevolg van de behandeling hoofdpijn, duizeligheid, vermoeidheid en/of andere
(autonome nerveuze) reacties ontstaan, dient de behandeling in een lagere intensiteit te
worden uitgevoerd.
Het wordt aanbevolen om diathermiemachines (zoals kortegolf- en microgolfapparaten) op
minstens een meter afstand te houden van elektrostimulatieapparatuur, omdat de output van
elektrostimulatieapparatuur kan worden beïnvloed door de nabijheid van een werkende
(gepulseerde) kortegolf- of microgolfapparaat.
Stimulatie dient niet te worden toegepast over of door het hoofd, direct op de ogen, over de
mond, aan de voorkant van de nek (vooral de halsslagader), of door middel van elektroden
die op de borst en de bovenrug worden geplaatst of die het hart kruisen.
Toepassing van elektroden in de buurt van de borstkas kan het risico op hartfibrilleren
verhogen.
Gelijktijdige aansluiting van een patiënt op een hoogfrequente chirurgische medische
apparatuur kan leiden tot brandwonden op de plaats van de stimulatorelektroden en
mogelijke schade aan de stimulator.
Elektroden met een stroomdichtheid van meer dan 2 mA/cm² vragen mogelijk de speciale
aandacht van de bediener.
Aansluiting van de electroden
Zie hoofdstuk 3 voor een beschrijving van de genummerde onderdelen.
Endomed 182 Type 1
• Verbind de DC referentiekabel [5] met de verbindingspoort [3].
• Verbind de blanke aardelektrode [4] met de DC referentiekabel [5].
• Gebruik van de blanke aardelektrode: de patiënt moet de blanke aardelektrode tijdens de
behandeling vasthouden.

Pagina 38 van 52 NL109-1634750-40 IFU
• Verbind de kabel voor de elektrodehouder [6] met de verbindingspoort [2].
• Bevestig de naald (niet meegeleverd) aan de elektrodehouder met het draadsysteem, waarmee
de elektrodehouder kan worden geopend, de naald kan worden bevestigd, en de
elektrodehouder kan worden gesloten.
• Het naaldhouder is voorzien van een start/stopknop waarmee de stroom handmatig kan
worden aangezet of onderbroken.
Endomed 182 Type 2
• Verbind de patiëntkabels met verbindingspoort 1 [10] en/of verbindingspoort 2 [11] van de
stroommodule [9] (rode stekker in rode verbindingspoort, zwarte stekker in zwarte
verbindingspoort).
• Verbind de elektroden met de patiëntkabel.
Endomed 182 Type 3
• Bij gebruik van plakbare of rubber elektroden: verbind de patiëntkabels met de bovenste
verbindingspoorten [15] van de vacuümmodule [13] en verbind de elektroden met de
patiëntkabels (rode stekker in rode verbindingspoort, zwarte stekker in zwarte
verbindingspoort).
• Bij gebruik van vacuümelektroden: verbind de vacuümslangen met de onderste
verbindingspoorten [16] van de vacuümmodule [13] en verbind de vacuümelektroden met de
vacuümslangen (rode stekker in rode verbindingspoort, zwarte stekker in zwarte
verbindingspoort).
Behandeling
Voor de behandeling
• De huid van het betreffende gebied wordt gereinigd (verwijdering van vet) met zeep of 70 %
alcohol.
• Het scheren van een harige huid wordt aanbevolen
• Test de gevoeligheid van het behandelingsgebied
• Plaats de elektroden en/of sponzen (vergeet niet te bevochtigen)
• Volg de instructies in hoofdstuk 10 over het aanpassen van de instellingen en het starten en
stoppen van de behandeling.
Tijdens de behandeling
• De intensiteit wordt op het gewenste niveau ingesteld
• De patiënt wordt regelmatig gevraagd om de gevoelde sensaties te melden. Indien nodig wordt
de behandeling aangepast.
Beëindiging van de behandeling
• De behandeling kan worden gestopt door op het stop-icoon op het aanraakscherm te drukken.
De behandeling stopt automatisch wanneer de behandelingstijd is verstreken.
Na de behandeling
• Verwijder de elektroden en/of de sponzen
• Maak de huid van de patiënt schoon met een handdoek of tissue
• De verwachte effecten worden gecontroleerd (bijv. pijn, circulatie en mobiliteit)
• De patiënt wordt gevraagd om achteraf commentaar te geven op eventuele reacties

Pagina 39 van 52 NL109-1634750-40 IFU
Endomed 182 Type 1:
Percutane Electrolyse
Percutane elektrolyse (PE) is een niet-farmacologische, minimaal invasieve behandeltechniek voor
chronische tendinopathieën en heeft weinig bijwerkingen vergeleken met farmaceutische
interventie. PE wordt door de meeste patiënten goed verdragen, en complicaties en bijwerkingen
treden zeer zelden op. Patiënten moeten echter wel geïnformeerd worden over de mogelijke
risico’s van percutane elektrolyse.
• De behandeling kan milde pijnklachten veroorzaken die normaal gesproken 48 tot 72 uur
aanhouden
een van de meest voorkomende gevolgen van de interventie is pijn in het behandelde gebied,
veroorzaakt door de naaldpunctie. Tijdens het toedienen van de gelijkstroom kunnen patiënten
matige tot ernstige pijn ervaren (afhankelijk van de gebruikte intensiteit). Lokaal geïnjecteerde
anesthetica zijn meestal niet nodig voor percutane elektrolyse, omdat de procedure over het
algemeen goed wordt verdragen door patiënten (de toediening van gelijkstroom kan op ieder
moment worden stopgezet als de pijn onverdraaglijk is). Het gebruik van injectienaalden voor de
toediening van de anesthetica zou bovendien de interventie aanzienlijk meer invasief maken. Het
gebruik van anesthetica blijft echter een te overwegen optie.
• Vasovagale reacties tijdens en onmiddellijk na de interventie
Percutane elektrolyse is van invloed op het autonome zenuwstelsel. Zoals bij elke procedure waarbij
gebruik wordt gemaakt van naalden zijn vagale reacties (zoals bleekheid, zweten, pilo-erectie en
klamme huid) gemeld tijdens PE. Meerdere onderzoeken omvatten informatie over het mogelijk risico
van eventuele vasovagale reacties. Deze reacties kunnen over het algemeen worden verklaard door
het effect van de naald en niet alleen door dat van de stroom.
• Bloeding in gebied van punctie
Na behandeling kan een compressieverband worden aangebracht, maar dit is normaal gesproken
niet noodzakelijk.
Het gebruik van ijs of het innemen van ontstekingsremmende geneesmiddelen (NSAID’s) gedurende
72 uur na de behandeling wordt niet aangeraden aangezien dit het verwachte therapeutische effect
(het opwekken van een gecontroleerd ontstekingsproces) tenietdoet.
Acupunctuurnaald
Het gebruik van hoogwaardige, steriele acupunctuurnaalden voor eenmalig gebruik die een
medische CE-goedkeuring hebben, inclusief het Notified Body nummer, wordt aanbevolen. Enraf-
Nonius levert geen naalden. De naald moet compatibel zijn met het gebruik van echogeleide
elektrolyse. Wat de afmetingen van de naald betreft, is het belangrijk dat de juiste naalddikte en -
lengte worden gekozen voor het te behandelen letsel.
• Diameter naald: 0,30 mm – 0,35 mm
• Buitendiameter handvat: 1,25 mm – 1,45 mm
• Naaldlengte: 20 mm – 100 mm
• Handvatlengte: 25 mm – 30 mm

Pagina 40 van 52 NL109-1634750-40 IFU
Voetschakelaar
De Endomed 182 Type 1 heeft een optionele voetschakelaar die verbonden kan worden met
verbindingspoort A [7] (zie hoofdstuk 3).
Plaats de voetschakelaar zo dat deze goed te bereiken is tijdens
de behandeling. De bedieningseenheid van de voetschakelaar is
multidirectioneel, dus het is niet nodig de voetschakelaar exact
uit te lijnen.
Om beschadiging te voorkomen, dient te moeten worden
opgemerkt dat er slechts lichte druk nodig is voor de bediening
van de schakelaar. Gebruik het voorste deel van uw voet bij de
bediening van de schakelaar, niet de hak.
Druk één keer op de voetschakelaar om de behandeling te activeren. Druk nog een keer op de
voetschakelaar om de behandeling stop te zetten.
Endomed 182 Type 2 en 3:
TENS / IFC
Protocol voor de veilige toepassing van TENS / IFC
• Controleer contra-indicaties met de patiënt
• Test de huid op een normale sensatie met behulp van een stompte/scherpte test
• Het apparaat dient uitgeschakeld te zijn en de elektrische kabels dienen losgekoppeld te
worden
• Stel de elektrische parameters van TENS / IFC in terwijl het apparaat is uitgeschakeld
• Sluit de elektroden aan op de patiëntkabel en plaats de elektroden op de huid van de patiënt
• Controleer of het apparaat nog steeds is uitgeschakeld en sluit de patiëntkabel aan op het
apparaat
• Schakel het apparaat in
• Geleidelijk aan (langzaam) de intensiteit verder verhogen tot de patiënt een sterk maar
comfortabel tintelend gevoel ervaart.
• Deze intensiteit mag niet pijnlijk zijn of spiersamentrekking veroorzaken
Protocol voor de veilige beëindiging van
• Geleidelijk (langzaam) de intensiteit verminderen totdat de patiënt geen tintelend gevoel meer
ervaart
• Schakel het apparaat uit
• Maak de patiëntkabel los van het apparaat
• Maak de electroden los van de patiëntkabel
• Verwijder de elektroden van de huid van de patiënt

Pagina 41 van 52 NL109-1634750-40 IFU
Endomed 182 Type 2 en 3:
Flexibele rubberen elektrodes
U wordt aangeraden de flexibele rubberen elektrodes te gebruiken in combinatie met de
meegeleverde sponsjes. Als ze goed vochtig zijn zorgen de sponsjes voor een lage impedantie
tussen de huid en de stimulator tijdens de behandeling en ze kunnen achteraf gemakkelijk worden
schoongemaakt. Volg bij het gebruik van deze elektrodes de onderstaande richtlijnen.
• Voor het eerste gebruik moeten de sponsjes grondig worden gespoeld in warm kraanwater om
het impregneermiddel te verwijderen.
• Voordat ze worden gebruikt moeten de sponsjes met kraanwater worden doordrenkt. Bij
voorkeur een zoutoplossing gebruiken aangezien dit elektrische geleiding verbeterd.
• De meegeleverde sponsjes hebben drie lagen. Bij wisselstroom moet een sponslaag tussen
dehuid en de elektrode worden aangebracht voor minimale weerstand.
• Bevestig elektrode/sponsje op de patiënt met de meegeleverde fixatiebanden. Afhankelijk van
deelektrodegrootte moeten twee of drie omwikkelingen worden gebruikt om het
contactoppervlak zo groot mogelijk te maken. Zie onderstaande illustraties.
• Het is belangrijk dat de elektroden volledig in contact blijven zonder dat de randen omhoog
gaan tijdens de behandeling.
• De Endomed 182 uitgangsmodus is Constant Current (CC). Hierdoor zal de ingestelde
stroomamplitude worden gehandhaafd, zelfs wanneer de impedantie van de sponsjes tijdens
de behandeling toeneemt door waterverdamping.
• Houd de sponsen goed bevochtigd ( bijna druipend als ze licht worden uitgeknepen) tijdens de
behandeling. Herbevochtig wanneer de behandeling langer dan 10 minuten duurt.
• Maak na gebruik de sponsen schoon zoals beschreven onder "Reiniging en desinfectie".
Foutieve applicatie van fixatiebanden,
resulterend in slechte elektrische geleiding.
Correcte applicatie van fixatiebanden,
resulterend in goede elektrische geleiding.

Pagina 42 van 52 NL109-1634750-40 IFU
Endomed 182 Type 2 en 3:
Zelfklevende elektrodes
Herhaaldelijk gebruik van voorgegeleerde elektroden leidt tot een snel verlies van
geleidbaarheid en een verslechterende kleefkracht.
Het verlies aan hechting en het drogen van de gel zal ervoor zorgen dat de randen beginnen
te liften, wat de stroomdichtheid dramatisch kan verhogen; kan een ongelijkmatige verdeling
van de stroom over het elektrodeoppervlak veroorzaken, waardoor het risico op
brandwonden toeneemt; en mogelijk leidt tot verplaatsing van de elektrode.
Veranderingen in de zelfklevende elektroden die in de loop van de tijd optreden, leiden tot
een onveilige situatie waarin huidirritatie en ongemak voor de patiënt kunnen optreden.
Zelfklevende elektroden mogen nooit worden gedeeld tussen patiënten.
Zelfklevende elektrodes hebben een hogere serie-impedantie dan flexibele rubberen elektrodes.
Hierdoor is het mogelijk dat de stimulator de behandeling met hogere stroomamplitudes
beëindigt. Wanneer dit gebeurt, wordt aanbevolen de behandeling voort te zetten met flexibele
rubberen elektrodes, gecombineerd met goed bevochtigde sponsjes.
Endomed 182 Type 3:
Vacuümelektrodes
U hebt de keuze uit grote en kleine elektrodes. Het oppervlak van de elektrodes komt overeen met
dat van de flexibele rubberen elektrodes van 4 x 6 cm, 6 x 8 cm en 8 x 12 cm. De vacuümelektrodes
zijn flexibel genoeg om optimaal contact met de huid te verzekeren, maar stug genoeg om te
voorkomen dat de contouren van het behandelde lichaamsdeel veranderen, waardoor optimaal van
het massage-effect van het pulserende vacuüm kan worden geprofiteerd.
Het massage-effect dat het gevolg is van het pulserende vacuüm zorgt voor een goede
doorbloeding van de huid onder de elektrodes. Dit vermindert de weerstand van de huid en
verhoogt de werkzaamheid van de stimulerende stroom.
• Kies, afhankelijk van het te behandelen lichaamsdeel het elektrodeformaat.
• Maak de sponsjes nat. Knijp de sponsjes ietwat uit en plaats ze in de vacuümelektroden.
• Kies voor continu vacuüm, dit vergemakkelijkt het aanbrengen van de elektroden.
• Plaats de elektroden op een glad oppervlak (b.v. een tafel).
• Draai de vacuumintensiteit een beetje op, zodat vacuum ontstaat in de electroden.
• Verplaats de electroden nu één voor één van het gladde oppervlak naar het lichaam van de
patiënt
• Stel de vacuumintensiteit in op de gewenste waarde.
• Volg de instructies in hoofdstuk 10 over het aanpassen van de instellingen en het starten en
stoppen van de behandeling.
• Corrigeer zonodig het vacuüm; Een lage zuigkracht is voldoende.
• Kies eventueel voor pulseren.
Houd de sponsen goed bevochtigd ( bijna druipend als ze licht worden uitgeknepen) tijdens de
behandeling. Herbevochtig wanneer de behandeling langer dan 10 minuten duurt. Maak na gebruik
de sponsen schoon zoals beschreven onder "Reiniging en desinfectie".
• Wanneer u slechts één vacuümkanaal gebruikt, sluit het andere kanaal af met een van de
vacuümkabels die niet in gebruik zijn.

Pagina 43 van 52 NL109-1634750-40 IFU
Constante of pulserende zuigkracht
Zodra, bij constante zuigkracht, het ingestelde vacuüm bereikt is, schakelt de pomp zichzelf uit
waardoor de Vacuümmodule vrijwel geruisloos in bedrijf is. Een regelsysteem zorgt ervoor dat het
vacuüm constant blijft. De pomp wordt kortstondig aangezet om tijdens de behandeling het
vacuüm op peil te houden.
Bij een pulserende zuigkracht, wordt de pomp wisselend aan- en uitgeschakeld. Het pulserende
ritme voor de zuigkrachtmassage kan continue of pulserend (2 standen) ingesteld worden.
Pulserende zuigkracht is goed bruikbaar bij patiënten die gevoelig zijn voor stroom, aangezien het
de sensatie van stroom min of meer naar de achtergrond dringt.
Stroomdichtheid
In de specifieke norm voor toestellen voor het stimuleren van zenuwen en spieren, IEC 60601-2-10,
wordt aanbevolen een stroomdichtheid van 2 mA effectief per cm² niet te overschrijden, omdat
anders huidirritaties of etswonden kunnen ontstaan.
Om de maximale aanbevolen stroomamplitude in mA voor de Interferentie stroomvorm moet het
elektrodeoppervlak in cm² met twee worden vermenigvuldigd. Bij alle andere stroomvormen kan de
uitgangsstroom van de stimulator nooit 50 mA effectief overschrijden. Dit houdt in dat bij een
elektrodeoppervlak van 25 cm² de stroomdichtheid nooit meer kan zijn dan 2 mA effectief / cm².
Als vuistregel voor kleinere elektrodes, zoals de zelfklevende van 3.2 mm, dient de maximale
stroominstelling op de stimulator voor een bepaalde stroomgolfvorm proportioneel moeten
gereduceerd.
Voor een nauwkeurige berekening van de effectieve waarde (r.m.s.) van een pulserende
stroomgolfvorm kan de volgende formule worden gebruikt:
Let op dat de elektroden met zorg moeten worden geplaatst, zodat er goed elektrisch contact is
over het gehele elektrodeoppervlak, en dat het gebruik van kleine elektroden in combinatie met
hoge intensiteiten huidirritaties of etswonden kan veroorzaken.
Aansluitings- en loskoppelingsreacties
Bij een Constant Current (CC) uitgangskarakteristiek kunnen onaangename aansluitings- en
loskoppelingsreacties optreden als de elektrodes niet goed vastzitten of geheel losraken. Zorg
ervoor dat de stroomamplitude is ingesteld op 0 mA wanneer u de elektrodes aanbrengt of
verwijdert. Gebruik de Constant Voltage (CV) output modus bij dynamische elektrodetoepassingen.

Pagina 44 van 52 NL109-1634750-40 IFU
12 Onderhoud en verhelpen van verstoringen
Reinigen en Desinfecteren
Reinig het apparaat en de accessoires regelmatig om de hygiënische veiligheid te waarborgen.
Voordat u begint met reinigen, schakel het apparaat uit en haal de stekker uit het stopcontact.
Spuit het reinigingsmiddel niet rechtstreeks op het glazen paneel.
Gebruik geen reinigingsmiddelen die sterke alkaliën, loog of zuur bevatten en geen
reinigingsmiddelen die fluoride of ammoniak bevatten.
Zorg dat er geen vloeistoffen het apparaat of de accessoires kunnen binnendringen terwijl u
bezig bent met reinigen en desinfecteren!
Maak alle aansluitingen en connectoren droog als deze nat zijn geworden voordat u het
apparaat weer gaat gebruiken!
Mechanische schokken en/of trillingen moeten worden vermeden bij het reinigen van de
ultrageluid applicator!
Laat het apparaat niet vallen.
Apparaat
Als u het apparaat wilt reinigen zet u deze uit en trekt u de stekker uit het
stopcontact. Reinig de unit met een vochtige doek. Gebruik geen schurende
reinigingsmiddelen. Zo nodig kan een kleine hoeveelheid huishoudelijk
reinigingsmiddel worden gebruikt.
Display Paneel
Het displaypaneel heeft een anti-reflectie coating en moet daarom voorzichtig
worden gereinigd. Gebruik een zachte en droge katoenen doek of een
microvezeldoekje om het paneel te reinigen. Om vingerafdrukken of vetvlekken
te verwijderen gebruikt u een niet-schurend glasreinigingsmiddel. Doe een
kleine hoeveelheid reinigingsmiddel op een zachte katoenen doek en reinig
hiermee het paneel voorzichtig.
Electroden,
electrodehouder,
sponsjes en
accessoires
Tussen gebruik bij verschillende patiënten dienen de rubberen elektrodes met
lauw water te worden gereinigd. Om de elektrodes te desinfecteren of
hardnekkige vlekken of vuil te verwijderen, gebruikt u een 70%
alcoholoplossing. De rubberen elektrodes kunnen hierbij afgeven, dit is echter
niet nadelig voor de werking.
Tussen het gebruik bij patiënten door moeten de sponsen worden gewassen in
stromend leidingwater, grondig worden uitgelekt en vervolgens worden
gedroogd. Beschadigde sponsjes moeten worden vervangen.
Het wordt aanbevolen dat er voldoende sponzen beschikbaar zijn om volledig
te kunnen drogen voordat deze weer gebruikt worden - dit zal de groei van
bacteriën beperken.
Wanneer de elektroden niet worden gebruikt, moeten de sponsen worden
verwijderd. Dit verhoogt de levensduur van de rubberen elektroden. Wij
adviseren om een extra set sponsen op voorraad te houden.
De blanke aardelektrode kan worden gereinigd met een vochtige doek.
Gebruik hiervoor zeep en lauwwarm water of een alcoholoplossing.
De elektrodehouder kan worden gereinigd met een vochtige doek. Gebruik lauw
water en een niet-schurend, niet-invasief huishoudelijk reinigingsmiddel of
alcoholoplossing. Niet in een autoclaaf plaatsen.

Pagina 45 van 52 NL109-1634750-40 IFU
Patiëntkabel en
DC referentie
kabel
Reinig de patiëntkabel met een vochtige doek. Gebruik lauw water en een
niet-schurend huishoudelijk reinigingsmiddel. Gebruik geen alcoholoplossing.
Controleer de kabel regelmatig op beschadigingen
en/of slecht elektrisch contact. Aangeraden wordt een patiëntkabel in voorraad
te houden.
Vacuüm-
elektroden en
sponsjes
De vacuümelektrodes en sponzen dienen met lauw water te worden gereinigd.
In het geval van hardnekkig vuil en voor desinfectie kan een 70%
alcoholoplossing worden gebruikt.
Sponzen dienen regelmatig te worden vervangen. Aanbevolen wordt sponzen
en een elektrode in voorraad te houden.
Op de metalen oppervlakken van de elektrodes kan zich kalk afzetten. Dit
heeft een isolerend effect. Om optimale geleidingsvermogen te behouden
dienen deze oppervlakken regelmatig te worden gereinigd en gladgeschuurd.
Vacuümkabels
Reinig de vacuümkabel met een vochtige doek. Gebruik geen
alcoholoplossing. Controleer de kabel regelmatig op beschadigingen
en/of slecht elektrisch contact.
Reinigen van
waterreservoir
en slangen
• Koppel de vacuüm-zuignappen los van de vacuüm-kabels.
• Plaats een bak gevuld met een reinigingsvloeistof (*) onder het systeem.
• Plaats de uiteinden van de kabels in de bak.
• Ga naar Systeeminstellingen, Onderhoud en selecteer Waterreservoir
reinigen.
• Het waterreservoir wordt gevuld met de reinigingsvloeistof totdat het
reservoir vol is.
• Leeg het waterreservoir zoals onder beschreven (water reservoir vol).
(*) De volgende geregistreerde producten mogen worden gebruikt voor het desinfecteren van het
waterreservoir:
BAKTONIL, BAKTOLAN tot 5%, CHINOSOL tot 1%, CHLORAMIN oplossing, DETTOL, ELMOCID
Gamma tot 2%, PERODIN, ZEPHIROL tot 5%.
Neem de voorschriften van de betreffende fabrikant in acht.
Verhelpen van storingen
Het apparaat mag niet worden gebruikt wanneer er mechanische schade wordt opgemerkt.
Dit geldt ook voor beschadigde kabelisolatie.
In het geval dat er een foutmelding of waarschuwing verschijnt, dient u het gebruik van het
apparaat onmiddellijk te stoppen. Schakel het apparaat uit en start het opnieuw op. Indien
het probleem aanhoudt, neem dan contact op met de leverancier of met Enraf-Nonius B.V.
voor service. Foutmeldingen en waarschuwingen duiden op een intern probleem met het
apparaat dat op locatie moet worden getest door een door Enraf-Nonius B.V gecertificeerde
onderhoudsmonteur voordat u het systeem weer kunt bedienen of gebruiken. Een apparaat
dat een fout of een waarschuwing aangeeft, kan mogelijk letsel toebrengen aan de patient,
de gebruiker, of kan mogelijk leiden tot omvangrijke interne schade aan het systeem.
In geval van weergavestoringen of andere duidelijke defecten ontkoppelt u het apparaat
meteen en neemt u contact op met een gecertificeerde onderhoudsmonteur.
Bij het binnendringen van vloeistoffen dient u de stekker uit het stopcontact te halen en het
apparaat door een bevoegd persoon te laten controleren.

Pagina 46 van 52 NL109-1634750-40 IFU
Foutberichten
Wanneer het apparaat wordt ingeschakeld, zal het eerst een zelftest uitvoeren. Als een fout wordt
ontdekt (zowel tijdens de zelftest als tijdens normaal bedrijf) zal een pop-up venster op het display
verschijnen. Wanneer de fout wordt weergegeven, zal alle uitgangsspanning worden uitgeschakeld.
Wanneer deze situatie zcih voordoet, schakel het apparaat uit en koppel alle accessoires los. Wacht
ongeveer 15 seconden en schakel het apparaat weer in.
Wanneer de fout zich nogmaals voordoet, dient u het apparaat niet meer te gebruiken en contact
op te nemen met uw leverancier.
Het apparaat moet eerst afkoelen voordat u verder kunt gaan
De temperatuur van het apparaat is te hoog om de behandeling te starten. Verwijder het apparaat
van mogelijke warmtebronnen (zoals direct zonlicht) en laat het apparaat afkoelen. Start het
apparaat opnieuw op om verder te gaan.
Onvoldoende of geen uitgangsstroom
• Controleer de patiëntkabel op breuken of slecht contact.
• Zorg ervoor dat de sponzen voldoende vochtig zijn.
• Reinig de elektroden
• Controleer op slecht contact
• In gebieden waar het water zacht is, is het mogelijk dat het water slecht geleidt, wat kan leiden
tot abnormaal lage stromingen. In dit geval is het mogelijk om een zoutoplossing te gebruiken
om de geleidbaarheid van het water te verbeteren.
Waterreservoir vol
Het water-scheidingsreservoir van de Vacotron is vol. Vervolg de behandeling met de standaard
elektroden of leeg het reservoir als volgt:
• Zet de aan-/uitschakelaar [17] op Uit (0).
• Koppel de slang los van de bovenste slangaansluiting [21] en leeg het reservoir.
• Sluit de slang weer aan op de slangnippel.
• Zet de aan-/uitschakelaar [17] op Aan (1).
Vacuümlek
Waarschijnlijk is er een lek in het vacuümsysteem. Deze storing wordt meestal voorafgegaan door
een continu lopende pomp die probeert het ingestelde vacuüm te bereiken. Om het systeem te
beschermen, wordt de pomp na een bepaalde tijd automatisch gestopt. Inspecteer de
vacuümkabels en elektroden, zet het vacuüm terug op nul en probeer het opnieuw. Wanneer de
storing zich nogmaals voordoet, moet u het apparaat niet meer gebruiken en contact opnemen
met uw leverancier.

Pagina 47 van 52 NL109-1634750-40 IFU
Het is tevens raadzaam een dossier bij te houden van alle uitgevoerde servicewerkzaamheden. In
sommige landen is dit zelfs verplicht.
Op verzoek kan een onderhoudshandleiding beschikbaar worden gesteld met daarin:
onderdelenlijst, beschrijvingen, kalibratie-instructies en andere informatie die door het hiervoor
gekwalificeerde technisch personeel van de gebruiker kan worden gebruikt bij het repareren van
onderdelen van de apparatuur die door de fabrikant als repareerbaar zijn aangemerkt.
Verwachte Levensduur
Dit apparaat blijft geschikt voor het beoogde gebruik, mits het jaarlijks wordt onderhouden door een
gekwalificeerde onderhoudsmonteur van Enraf-Nonius B.V. of door een officiële distributeur zoals
beschreven in de servicehandleiding en de onderhoudsmonteur van mening is dat het apparaat
geschikt is voor gebruik volgens de specificaties.
Einde Levensduur
De Endomed 182 bevat materialen die hergebruikt kunnen worden en/of schadelijk zijn voor het
milieu.
Technisch Onderhoud
Het openen van de apparatuur door onbevoegden is niet toegestaan en beëindigt elke
aanspraak op garantie.
De fabrikant is niet verantwoordelijk voor de resultaten van onderhoud of reparaties door
onbevoegden.
Alleen door Enraf-Nonius B.V. geautoriseerde servicetechnici kunnen deze apparatuur
onderhouden of aanpassen aan de hand van de actuele service-informatie.
Voer geen onderhoud uit op het instrument als het instrument wordt gebruikt of op een
patiënt is aangesloten.
Het wordt aangeraden om de Endomed 182 jaarlijks te laten controleren door geautoriseerd
personeel van Enraf-Nonius of door haar geautoriseerde distributeur.
Zorg ervoor dat u goed op de hoogte bent van lokale regels en regelgevingen
betreffende het afvoeren van apparatuur en accessoires.

Pagina 48 van 52 NL109-1634750-40 IFU
13 Specificaties
Technische data
Elektrische info
Netspanning
100 - 240 Volt
Frequentie
50/60 Hz
Max. vermogen
50 VA
Dimensies (breedte x lengte x hoogte)
Endomed 182 Type 1
14,5 x 17 x 9 cm
Endomed 182 Type 2
14 x 16 x 14 cm
Endomed 182 Type 3
14 x 22,5 x 17,5 cm
Deze waarden geven de afmetingen van de
behuizingen weer zonder communicatiekabels,
elektroden of slang.
Gewicht
Endomed 182 Type 1
710 gram
Endomed 182 Type 2
1460 gram
Endomed 182 Type 3
2750 gram
Deze waarden vertegenwoordigen het gewicht van
de behuizingen zonder elektroden en netsnoeren.
Specificaties Type 1
Kanalen
1
Output
Constante Stroom
Gelijkstroom
Polariteit
Negatief
Intensiteit
0 – 15 mA
Behandeltijd
0 – 300 seconden
Specificaties Type 2 en 3
Kanalen
2
Output
Constante Stroom
Intensiteit
0 -100 mA
Behandeltijd
0 – 60 min (in stappen van 1 min)
2 polig interferentie
Draaggolf
4 kHz
AMF frequentie
1 – 200 Hz
Modulatie frequentie
0 – 180 Hz
Modulatie programma
1-1, 6-6, 1-30 seconden
4 polig interferentie en isoplanaire
vector
Draaggolf
4 kHz
AMF frequentie
1 – 200 Hz
Modulatie frequentie
0 – 180 Hz
Modulatie programma
1-1, 6-6, 1-30 seconden

Pagina 49 van 52 NL109-1634750-40 IFU
Asymmetrisch bifasische pulsstroom (TENS)
Pulsbreedte
150 μs
Frequentie
1 – 200 Hz
Modulatie frequentie
0 – 180 Hz
Modulatie programma
1-1, 6-6, 1-30 seconden
Burst frequentie
1-2-4 Hz
Technische modificaties voorbehouden
Normen met Betrekking tot Veiligheid en Prestaties
Classificatie medisch hulpmiddel
IIa; Regel 9 Annex IX van 93/42/EEC
Deze apparatuur voldoet aan alle eisen van de Richtlijn
Medische Hulpmiddelen (93/42/EEG)
Veiligheidsklasse volgens IEC 60601-1
Electrische veiligheidsklasse I
Werkingsmodus
Continu
Toegepaste onderdelen
Type BF Toegepast onderdeel voor elektrotherapie.
Essentiële Prestatie
De essentiële prestaties zijn gebaseerd op de standaard 60601-2-10 waarin de maximale output
van de stroom en de pulsenergie wordt gespecificeerd. Rekening houdend met de verschillende
therapievormen zijn de essentiële prestaties opgebouwd uit vijf vereisten:
1) De maximale TENS-stroom RMS mag niet hoger zijn dan 50 mA.
2) De maximale interferentiestroom RMS mag niet hoger zijn dan 100 mA.
3) De maximale TENS-pulsenergie mag niet hoger zijn dan 300 mJ.
4) De maximale interferentiepulsenergie mag niet hoger zijn dan 300 mJ.
5) De maximale gelijkstroom RMS mag niet hoger zijn dan 80 mA.
De elektrotherapie-outputs moeten binnen 20% van de gestelde waarde blijven.
Omdat dit een niet-levensondersteunend apparaat betreft, mag het in een veilige staat komen
(geen output) waarbij handmatige herstart vereist is.
Omgevingscondities
Omgevingscondities voor transport en opslag
Omgevingstemperatuur:
–20° tot +70° C
Relatieve vochtigheid:
10 tot 90% (niet-condenserend)
Atmosferische druk:
500 tot 1060 hPa
Omgevingscondities voor normaal gebruik
Omgevingstemperatuur:
10° tot 40° C
Relatieve vochtigheid:
10 tot 90 % (niet-condenserend)
Atmosferische druk:
800 tot 1060 hPa

Pagina 50 van 52 NL109-1634750-40 IFU
EMC Details
Voor medische elektrische apparaten zoals de Endomed 182 gelden speciale
voorzorgsmaatregelen met betrekking tot elektromagnetische compatibiliteit (EMC) en deze
moeten geplaatst en in gebruik genomen worden in overeenstemming met het EMC-advies
in de gebruiksaanwijzing.
Het apparaat mag niet worden gebruikt direct geplaatst naast, of bovenop andere apparaten.
Als het apparaat moet worden gebruikt direct naast of bovenop andere apparaten, moet het
apparaat worden gecontroleerd om ervoor te zorgen dat het zoals beschreven funktioneert.
Het gebruik van accessoires, zenders en kabels anders dan gespecificeerd of geleverd door de
fabrikant van deze apparatuur kan leiden tot verhoogde elektromagnetische emissies of
verlaagde elektromagnetische immuniteit van dit apparaat, wat kan leiden tot onjuist
functioneren.
Draagbare RF-communicatieapparatuur (met inbegrip van randapparatuur zoals
antennekabels en externe antennes) mag niet minder dan 30 cm verwijderd zijn van enig
onderdeel van de Endomed 182, inclusief de door de fabrikant gespecificeerde kabels. Anders
kunnen de prestaties van deze apparatuur afnemen.
De Endomed 182 mag alleen worden gebruikt met de originele netsnoer vermeld op de lijst
inhoud van de verpakking. Bediening van het apparaat met een ander netsnoer kan leiden tot
hogere emissies of verminderde immuniteit van het apparaat.
De Endomed 182 is geklassificeerd als een groep 1, klasse B apparaat volgens CISPR 11.
De Endomed 182 is geschikt voor gebruik in een professionele zorginstelling. Het apparaat gebruikt
RF-energie uitsluitend voor zijn interne werking. Daarom is de RF-emissie erg laag en is het
onwaarschijnlijk dat ze interferentie veroorzaken in elektronische apparatuur in de buurt.
De Endomed 182 is getest volgens de norm 60601-1-2 door een geaccrediteerd laboratorium en is
voor elke emissie- en immuniteitsnorm of -test conform bevonden.

Pagina 51 van 52 NL109-1634750-40 IFU
14 Contact
Kijk voor hulp en ondersteuning op onze website http://www.enraf-nonius.com
De laatste versie van deze gebruiksaanwijzing (in elektronische of gedrukte vorm) kan kosteloos
worden verkregen via onze website www.enraf-nonius.com of door contact op te nemen met uw
leverancier of door te bellen met nummer: +31-(0)10-2030600. De gebruiksaanwijzing zal (gratis)
binnen 7 (zeven) kalenderdagen worden opgestuurd.
15 Productaansprakelijkheid
In veel landen is wetgeving met betrekking tot productaansprakelijkheid van kracht. Dergelijke
wetgeving impliceert, onder meer, dat de fabrikant na een periode van 10 jaar nadat een product in
roulatie is gebracht, niet meer verantwoordelijk kan worden gehouden voor mogelijke
tekortkomingen van het product.
Voor zover maximaal toegestaan op grond van het toepasselijke recht zijn Enraf-Nonius of diens
leveranciers of wederverkopers in geen geval aansprakelijk voor indirecte, speciale, incidentele of
gevolgschade die voorkomt uit het gebruik of het niet kunnen gebruiken van het product, inclusief,
zonder beperkingen, schade door verlies van goodwill, werk of productiviteit, computerstoringen,
en alle andere vormen van zakelijke schade of verlies, ook indien men op de hoogte is gesteld van
de mogelijkheid van het optreden hiervan, en ongeacht de juridische of billijke theorie (contract,
onrechtmatige daad of anderszins) waarop de claim is gebaseerd. In geen enkel geval zal de totale
aansprakelijkheid van Enraf-Nonius in het kader van de bepalingen van deze overeenkomst groter
zijn dan de som van de bedragen betaald voor dit product en de bedragen voor ondersteuning van
het product, ontvangen door Enraf-Nonius in de context van een afzonderlijke
ondersteuningsovereenkomst (indien van toepassing), met uitzondering van dood of persoonlijk
letsel veroorzaakt door nalatigheid van Enraf-Nonius in de mate waarin het toepasselijk recht
beperking van aansprakelijkheid in zulke gevallen verbiedt.
De wederpartij (de gebruiker van het product of diens vertegenwoordiger) vrijwaart Enraf-Nonius
van alle claims door derden van welke aard dan ook en ongeacht de relatie met de wederpartij.

NL109-1634750-40
Copyright:
Enraf-Nonius B.V.
Vareseweg 127 | 3047 AT | Rotterdam | Nederland
Tel: +31 (0)10-20 30 600 | [email protected]

Seite 1 von 54 DE109-1634750-40 IFU
Endomed 182
DE109-1634750-40 IFU
21. September, 2020
Gebrauchsanweisung

Seite 2 von 54 DE109-1634750-40 IFU
Inhalt
1 Einführung ......................................................................................................................................................... 3
2 Symbole .............................................................................................................................................................. 8
3 Gerätekomponenten................................................................................................................................... 10
4 Verpackungsinhalt ....................................................................................................................................... 14
5 Installation ...................................................................................................................................................... 16
6 Bestimmungsgemäßer Gebrauch und vorgesehene Anwender ................................................ 17
7 Indikationen ................................................................................................................................................... 18
8 Kontraindikationen ...................................................................................................................................... 19
9 Vorsichtshinweise......................................................................................................................................... 21
10 Bedienung ....................................................................................................................................................... 24
11 Informationen zur Anwendung .............................................................................................................. 38
12 Wartung und Fehlerbehebung ............................................................................................................... 45
13 Spezifikation ................................................................................................................................................... 49
14 Kontakt ............................................................................................................................................................. 52
15 Produkthaftung ............................................................................................................................................. 52

Seite 3 von 54 DE109-1634750-40 IFU
1 Einführung
Vorwort
Wir freuen uns, dass Sie einen Endomed 182 erworben haben.
Der Endomed 182 wurde von Enraf-Nonius B.V. entwickelt und hergestellt und bietet durch ein
fortschrittliches Hard- und Software-Design eine neue Dimension in der Elektrotherapie. Das
Ergebnis ist ein Gerät mit einer außergewöhnlichen Vielseitigkeit, das auf der Einfachheit der
Bedienung basiert.
Dieses Handbuch wurde für Besitzer und Bediener des Endomed 182 verfasst. Lesen Sie dieses
Handbuch sorgfältig durch und machen Sie sich mit den Bedienelementen und dem Zubehör
vertraut, bevor Sie das Gerät in Betrieb nehmen, um die Nutzung, Effizienz und Lebensdauer Ihres
Geräts zu optimieren.
Produktbeschreibung
Das Endomed 182 ist ein netzbetriebener Elektrostimulator und verfügt über einen Vollfarb-
Touchscreen. Die grafische Benutzeroberfläche sorgt für maximalen Bedienerkomfort.
Es sind drei Versionen des Endomed 182 erhältlich:
Endomed 182 Versionen
Name:
Endomed 182 Typ 1
Endomed 182 Typ 2
Endomed 182 Typ 3
Artikelnummer:
1634903
1634901
1634902
Artikelnummer
Basisgerät
1634910
1634900
1634900
Stromforme:
Gleichstrom
TENS
• kontinuierlich biphasischer
Impulsstrom (konventioneller
TENS Modus)
• Züge von biphasischen
Impulssulsstrom (Burst-TENS
Modus)
Interferenzstrom
• 2-polig Interferenz
(bipolarer) Modus
• 4-polig Interferenz
(tetrapolarer) Modus
• 4-polig Interferenz
(tetrapolar) mit Isoplanarer
Vektor
TENS
• kontinuierlich biphasischer
Impulsstrom (konventioneller
TENS Modus)
• Züge von biphasischen
Impulssulsstrom (Burst-TENS
Modus)
Interferenzstrom
• 2-polig Interferenz
(bipolarer) Modus
• 4-polig Interferenz
(tetrapolarer) Modus
• 4-polig Interferenz
(tetrapolar) mit Isoplanarer
Vektor
Vakuum
Kanäle:
1
2
2
Vorprogrammierte
Behandlungs-
protokolle:
-
16
16

Seite 4 von 54 DE109-1634750-40 IFU
Das Endomed 182 Typ 1 ist ein netzbetriebener 1-Kanal-Elektrostimulator zur Applikation
perkutaner Elektrolyse (PE) mithilfe von Gleichstrom (DC) geringer Intensität.
Bei der PE wird der Gleichstrom (auch galvanischer Strom genannt) über eine Nadel verabreicht, die
in den Nadelhalter eines Handstücks (des „Applikators“ oder der Kathode) gesteckt wird. Die
Gegenelektrode (oder Anode) ist eine handgehaltene Elektrode (wird vom Patienten gehalten) oder
eine andere Nadel, je nach der durchzuführenden Behandlung.
Der Nadelhalter des Applikators (des Handstücks) ermöglicht das Einstecken von Akupunkturnadeln
(steril, Einwegnadeln zum Einmalgebrauch) von unterschiedlichen Längen und Durchmessern, die
notwendig sind, um eine korrekte Platzierung in verschiedenen Bereichen (je nach der zu
behandelnden Erkrankung) zu gewährleisten.
Das Handstück ist mit einem Start/Stop-Knopf versehen, mit dem der Stromfluss manuell gestartet
oder unterbrochen werden kann.
Das Gerät gibt einen kontinuierlichen galvanischen Strom mit einem maximalen Ausgangsstrom von
15 mA ab.
Die grafische Benutzeroberfläche zeigt die folgenden Behandlungsparameter: Stromausgangspegel
(mA), eingestellte Zeit für die Anwendung, tatsächlich abgegebener Strom (mC).
Der Anwender kann den Stromausgangspegel (mA) und die Anwendungszeit je nach der Art der
Behandlung einstellen und anpassen.
Das Gerät verfügt nicht über voreingestellte klinische Protokolle, aber alle Behandlungsparameter
sind verstellbar und können als Favoriten (personalisierte Einstellungen) als Referenz für zukünftige
Therapiesitzungen gespeichert werden.
Das Gerät ist eine kompakte Einheit und wird mit folgendem Zubehör geliefert: Netzkabel und
Verbindungskabel, Handstück (Applikator), Gegenelektrode, Fußschalter (optional) und
Produktdokumentation. Verbrauchsmaterialien wie Einweg-(Akupunktur-)Nadeln sind nicht im
Lieferumfang des Produkts enthalten.
Von Enraf-Nonius B.V. sind keine perkutanen Elektroden oder Einwegakupunkturnadeln erhältlich.
Das Endomed 182 Typ 2 und 3 enthält 16 voreingestellte klinische Protokolle für TENS und
Interferenzströme. Einzelne Behandlungsparameter können auch manuell eingestellt und vom
Bediener angepasst werden. Alle Behandlungsparameter sind verstellbar und können als Favoriten
(personalisierte Einstellungen) als Referenz für zukünftige Therapiesitzungen gespeichert werden.
Das Endomed 182 Typ 3 besitzt eine übereinander angeordnete Konfiguration, die aus einem
separaten Modul zur Vakuumansaugung und einem Elektrostimulator Endomed 182 Typ 2 besteht.
Das Vakuummodul befindet sich unter dem Stimulator und ist mit ihm verbunden. Der Zweck des
Moduls ist, ein Vakuum zu erzeugen; dies ermöglicht es dem Therapeuten, die
Stimulationselektroden schnell und einfach(er) am Patienten zu befestigen (zu fixieren). Die
Fixierung wird mithilfe von Saugnäpfen erreicht. Die Saugnäpfe haben integrierte
Stimulationsoberflächen, die die Elektrostimulation über befeuchtete Schwämme auf das
Zielgewebe übertragen.
Beim Endomed 182 Typ 2 und 3 kann die elektrische Stimulation daher über Oberflächenelektroden
(flexible Gummielektroden, selbstklebende Elektroden oder Vakuumelektroden (nur Typ 3)) auf der

Seite 5 von 54 DE109-1634750-40 IFU
Haut erfolgen, um bestimmte Arten von Nervenfasern zu stimulieren. Enraf-Nonius bietet
Elektroden verschiedener Arten und Größen (von Punktelektroden mit einer Oberfläche von 0,3 cm2
bis zu Elektroden mit einer Oberfläche von 96 cm2), entsprechend der Größe der Behandlungsfläche
und dem zu erwartenden Behandlungsziel.
Stromformen Beschreibung
TENS
Die Impulsform des asymmetrischen biphasischen Impulsstroms wird oft in TENS - (Transkutane
elektrische Nervenstimulation) Anwendungen benutzt. Diese Impulsform zeichnet sich durch eine
variable Phasendauer und variable Impulsfrequenz aus. Ihre typische Amplitude, Dauer und
Anstiegs- und Abstiegsrate sind in bezug auf die Ausgangslage in jeder Phase anders. Die
Impulsform ist voll ausbalanciert, d.h. die Phasenladungen sind in allen Phasen gleich. Die
Zweiphasigkeit des Impulses bedeutet, dass keine Netto-Gleichstromkomponente (Netto-
Gleichstrom Null) vorhanden ist, wodurch Hautreaktionen aufgrund der Ansammlung von
Elektrolyten unter den Elektroden minimiert werden.
Um einer Gewöhnung an die Stimulation
vorzubeugen oder die Patiententoleranz zu
verbessern, kann die Impulsfrequenz durch
Frequenzmodulation variiert werden.
Asymmetrische biphasische Wellenform TENS
Burst-TENS
Die Burst-TENS wird angewendet, wenn die konventionelle TENS sich als unwirksam erweist und ist
insbesondere zur Behandlung von tieferliegenden schmerzenden Regionen und bei chronischen
Schmerzen geeignet. Bei der Burst-TENS wird eine relativ lange Phasendauer (150–200 μs), eine
niedrige Burst-Frequenz (1–5 Hz) und eine hohe Frequenz angewendet.
In den Muskeln, deren Innervation derjenigen der schmerzenden Region entspricht, sollten starke,
sichtbare Kontraktionen auftreten.
Die schmerzlindernde Wirkung wird gewöhnlich erst nach etwa 20 bis 30 Minuten bemerkt, im
Gegensatz zur Wirkung der konventionellen TENS, die normalerweise recht schnell eintritt. Die
Wirkung hält jedoch nach dem Ende der Stimulation wesentlich länger an als bei der
konventionellen TENS. Die schmerzlindernde Wirkung der Burst-TENS beruht auf der Freisetzung
von Endorphinen auf der spinalen und supraspinalen Ebene.
Wenn mit der konventionellen oder der Burst-TENS keine oder nur eine unzureichende Linderung
erzielt wurde, kann eine Frequenzmodulation angewendet werden. Die Frequenzmodulation kann
außerdem eine Gewöhnung verhindern.

Seite 6 von 54 DE109-1634750-40 IFU
Interferenzstrom
Beim Interferenz – Stromtyp wird eine Trägerfrequenz im mittleren Bereich benutzt, um die
Stimulationsfrequenz (Reiz) im niedrigen Bereich durch die Haut zu senden. Der relativ niedrige
Widerstand der Haut gegen die Trägerfrequenz trägt zum Komfort des Patienten bei, der oft mit
diesem Stromtyp in Verbindung gebracht wird. Interferenzströme sind stets Wechselströme ohne
jegliche Gleichstromreste. Es sind mehrere Variationen von Interferenzstrom bekannt, von denen
die folgenden im Endomed 182 Typ 2 und 3 verfügbar sind 2: 2-polig, 4-polig und 4-polig mit
isoplanarer Vektor.
Die bipolare Methode
Bei diesem Methode werden zwei Elektroden
verwendet, und die Überlagerung der beiden
Wechselströme findet innerhalb der Anlage statt. Der
Strom, der das Gerät verlässt, ist ein voll modulierter
Wechselstrom. Bei der zweipoligen Methode beträgt
die Modulationstiefe immer 100%.
Bipolare Interferenz
Die tetrapolare Methode (Klassische Interferenz)
Bei dieser Therapiemethode werden vier Elektroden
verwendet und zwei nichtmodulierte Ströme werden
erzeugt. Die Frequenz des einen Kanals wird auf die
Trägerfrequenz festgelegt, während der andere Kanal
eine variable Frequenz besitzt, die auf der Reiz-
Frequenz und den Frequenzmodulierungseinstellungen
beruht. Die Interferenz erfolgt dort, wo sich die beiden
Ströme im Gewebe kreuzen. Die Modulationstiefe
(welche die Stromamplitude der Stimulation bestimmt)
hängt von der Ausrichtung der Ströme ab und kann
zwischen 0 und 100% variieren. Eine 100%ige
Modulationstiefe ergibt sich nur an den Diagonalen
(und somit an der Kreuzung) der beiden Ströme. Dies
ist freilich eine theoretische Situation, die auf der
Annahme eines homogenen Gewebes basiert. In
Wirklichkeit ist das Gewebe heterogen, so dass die
Strombalance zwischen den beiden Kanälen genutzt
werden muß, um eine 100%ige Modulationstiefe zu
erreichen. Die Strombalance kann auch benutzt
werden, um auftretende Gefühlsunterschiede unter den
Elektrodenpaaren zu kompensieren.
Bei der tetrapolaren Methode beträgt die
Modulationstiefe an den Diagonalen nur
100%.

Seite 7 von 54 DE109-1634750-40 IFU
Die tetrapolare Methode mit isoplanarer Vektor
Mit dem Isoplanaren Vektor wird die Gesamtfläche
zwischen den 4 Elektroden optimal stimuliert. Die
Elektrodenpositionierung kann einfach und schnell
durchgeführt werden. Die Modulationstiefe beträgt
überall 100%.
Die Isoplanar-Interferenz kann für die Behandlung von
Problemen verwendet werden, die in einem grossen
Gebiet liegen und die sehr schwer zu lokalisieren sind.
Isoplanar Interferential wird auch als milde
Vorbehandlung eingesetzt. Nach dieser Anwendung
wird die Behandlung mit Schwerpunkt auf einem
kleineren, lokaleren Gebiet fortgesetzt.
Isoplanare Vektor
Gleichstrom
Ein Gleichstrom (DC) oder galvanischer Strom ist ein kontinuierlicher Strom, der in der Medizin für
eine Reihe von therapeutischen Zielsetzungen verwendet wird. Kontinuierlicher Strom bedeutet
einen stetigen Fluss elektrischer Ladung durch einen Stromleiter zwischen zwei Punkten
(Elektroden) mit unterschiedlichen Potentialen (Polarität), der seine Richtung im Lauf der Zeit nicht
ändert. Im Gegensatz zu Wechselströmen fließen die elektrischen Ladungen immer in die gleiche
Richtung.

Seite 8 von 54 DE109-1634750-40 IFU
2 Symbole
Verwendete
Symbole
Beschreibung
Befolgen Sie die Anweisungen in der Gebrauchsanweisung.
Es ist wichtig, dass Sie die Vorsichtsmaßnahmen und Bedienungsanweisungen
lesen, verstehen und beachten.
Allgemeines Verbotszeichen
Ein Verbotszeichen besagt „SIE DÜRFEN NICHT“
Warnung oder Vorsicht:
Weist auf eine Gefahrensituation hin, die bei Nichtbeachtung:
a. Beim Patienten zu schwerwiegenden Verletzungen oder sogar zum
Tode führen kann (oder)
b. Beim Patienten zu mittelschweren Verletzungen führen kann (oder)
c. Zu Schäden am Gerät führen kann.
Allgemeines Obligatorische Aktionszeichen.
Eine Pflichthandlung wird benutzt, um zu sagen: "Sie müssen..."
Anwendungsteil vom Typ BF, das den festgelegten Anforderungen entspricht
und einen höheren Schutz vor Stromschlag bietet als ein Anwendungsteil vom
Typ B
Temperaturbereich
Gibt den akzeptablen Temperaturbereich an.
Feuchtigkeitsbereich
Gibt die akzeptable relative Luftfeuchtigkeit an.
Luftdruckbereich
Gibt den Bereich des Luftdrucks an, dem das medizinische Gerät sicher
ausgesetzt werden kann.
Elektrische Altgeräte, die recycelt werden können
Gibt die elektrischen und elektronischen Teile des Geräts an, die recycelt
werden können bzw. die separat entsorgt werden müssen.
Halten Sie das Gerät trocken.
Name und Anschrift des Herstellers und Herstellungsdatum.
Referenznummer oder Teilenummer
Seriennummer
Zeigt die Seriennummer des Herstellers des Geräts an, sodass ein bestimmtes
medizinisches Gerät identifiziert werden kann.

Seite 9 von 54 DE109-1634750-40 IFU
Wechselstrom
Anschluss Elektrodenkabel Elektro
Anschlüsse Vacuum Kabel Elektro
“AN” (Strom)
“AUS” (Strom)
Das CE-Zeichen zusammen mit Nummer weist auf die Einhaltung der EU-
Richtlinie zu medizinischen Geräten hin sowie darauf, dass dieses Gerät der
direkten Aufsicht der benannten Stelle unterliegt.

Seite 10 von 54 DE109-1634750-40 IFU
3 Gerätekomponenten
Endomed 182 Typ 1
Endomed 182 Typ 2
7
8
1
9
1
2
1
3
1
1
4
1
6
1
5
1
10
11

Seite 11 von 54 DE109-1634750-40 IFU
Endomed 182 Typ 3
12
13
16
15
14
17
18
19
21
20

Seite 12 von 54 DE109-1634750-40 IFU
Beschreibung der Teile
Teile-
nummer
Beschreibung
Zweck
[1]
LCD-display
4,3"-TFT-Farbdisplay mit Touchscreen.
Zeigt die Benutzeroberfläche an, die es dem
Bediener ermöglicht, das Gerät zu steuern und die
Parameter der Behandlungsprotokolle zu ändern.
[2]
Anschluss Elektrodenhalter
Anschluss für Elektrodenhalter
[3]
Anschluss Blanke
Masseelektrode
Anschluss für DC-Referenzkabel, das an die Blanke
Masseelektrode angeschlossen wird
[4]
Blanke Masseelektrode
Referenz-Elektrode
[5]
DC-Referenzkabel
Anschlusskabel für Referenz-Elektrode
[6]
Elektrodenhalter
Handstück für Nadelhalter
[7]
Anschluss A
Anschluss für Vakuummodul (Endomed 182 Typ 3 /
Fußschalter (Endomed 182 Typ 1)
[8]
Anschluss B
Anschluss für Strommodul
[9]
Strommodul
Strommodul mit Anschluss für Klebe- und
Gummielektroden.
[10]
Anschluss 1 Strommodul
Anschlusskanal 1 für Patientenkabel für Klebe- oder
Gummielektroden am Strommodul Endomed 182.
[11]
Anschluss 2 Strommodul
Anschlusskanal 2 für Patientenkabel für Klebe- oder
Gummielektroden am Strommodul Endomed 182.
[12]
Vakuumelektrodenhalter
Halter für Vakuumelektroden.
[13]
Vakuummodul
Vakuummodul integriert mit Endomed 182 mit
Anschlüssen für Klebe- oder Gummielektroden und
Vakuumelektroden.
[14]
Elektrodenkabel des
Vakuummoduls
Die Elektrodenkabel des Vakuummoduls müssen
an die Anschlüsse des Strommoduls [7] und [8]
angeschlossen werden, damit die Anschlüsse des
Vakuummoduls korrekt funktionieren.
[15]
Obere Anschlüsse
Vakuummodul
Anschlusskanal 1 und 2 für Patientenkabel für
Klebe- oder Gummielektroden am Vakuummodul.
[16]
Untere Anschlüsse
Vakuummodul
Anschlüsse Kanal 1 und 2 für
Vakuumleitungsschlauch für Vakuumelektroden am
Vakuummodul.
[17]
Netzschalter
Zum Ein- und Ausschalten der Einheit.
Beim ausschalten bleibt der Anzeige für einige
Sekunden sichtbar (energetische Methode).
[18]
Referenzlabel
Bietet Informationen zum Gerät, wie z. B. die
Typen- und Seriennummer sowie Anschlussdaten,
wie Netzspannung und maximaler Stromverbrauch.
[19]
Anschluss für das Netzkabel
Ziehen Sie das Netzkabel ab, um das Gerät vom
Netz zu trennen.
[20]
Luftauslass
Luftauslass für Vakuummodul.

Seite 13 von 54 DE109-1634750-40 IFU
Beschreibung der Teile
Teile-
nummer
Beschreibung
Zweck
[21]
Anschluss für Wasserreservoir
Dieser Anschluss dient zum Anschluss des
Wasserreservoirs. Ohne den Anschluss des
Wasserreservoirs kann kein Vakuum erzeugt
werden. Der Wasserbehälter sorgt dafür, dass
überschüssiges Wasser aus den Schwämmen
aufgefangen wird und nicht durch die Pumpe
ausgeblasen werden kann. Das Reservoir sollte
täglich entleert werden. Bitte beachten Sie den
Abschnitt über die Wartung.

Seite 14 von 54 DE109-1634750-40 IFU
4 Verpackungsinhalt
Gerät
Der Packungsinhalt hängt vom bestellten Gerätemodell ab. Es gibt die folgenden Modelle:
Artikelnummer
Beschreibung
1634903
Endomed 182 Typ 1
1634901
Endomed 182 Typ 2
1634902
Endomed 182 Typ 3 (enthält integriertes Vakuummodul)
Standardzubehör Endomed 182 Typ 1
1634750
CD-ROM mit Gebrauchsanweisung (PDF auf CD-ROM)
1634751
Informationsbroschüre
3444357
Netzkabel 250V/2,5A, 2,5 Meter schwarz
3444080
Elektrodenhalter
3444582
Blanke Masseelektrode
3444677
DC-Referenzkabel
Standardzubehör Endomed 182 Typ 2 und Endomed 182 Typ 3
1634750
CD-ROM mit Gebrauchsanweisung (PDF auf CD-ROM)
1634751
Informationsbroschüre
3444357
Netzkabel 250V/2,5A, 2,5 Meter schwarz
3444021
Fixierband 250x3 cm
3444020
Fixierband 100x3 cm
3444129
(2x) Leitgummiplattenelektroden 6x8 cm, 2 mm Buchse, 2 St.
1460266
Viskoseschwämme für Platteneletrode 6x8 cm, Satz von 4.
3444211
(2x) Patientenkabel, 2-adrig & 2 mm Stecker - Schwarz, mit farbigen Clips
Zusätzliches Standardzubehör Endomed 182 Typ 3
3444503
(2x) Vakuumelektroden Ø 60 mm, Satz von 2 St.
3444505
Schwämme Ø 65 mm, Satz von 4 St. (für Vakuumelektroden Ø 60 mm)
3444507
(2x) Saugwelle Elektrodenkabel rot
3444508
(2x) Saugwelle Elektrodenkabel schwarz
Optionales Zubehör Endomed 182 Typ 1
1634810
Fußschalter
Optionales Zubehör Endomed 182 Typ 2 und Endomed 182 Typ 3
Klebeelektroden
3444056
EN-Trode Ø 3,2 cm, 2 mm Buchse, 10x4 Sätze in einer Packung
3444135
EN-Trode Ø 5,0 cm, 2 mm Buchse, 10x4 Sätze in einer Packung
3444057
EN-Trode 5x5 cm, 2 mm Buchse, 10x4 Sätze in einer Packung
3444058
EN-Trode 5x9 cm, 2 mm Buchse, 10x4 Sätze in einer Packung
3444222
Klebeelektroden Ø 2,0 cm, 2 mm Buchse, 10x8 Sätze in einer Packung.
Leitgummiplattenele Elektroden
3444128
Leitgummiplattenelektrode 4x6 cm, 2 mm Buchse, Satz von 2
3444129
Leitgummiplattenelektrode 6x8 cm, 2 mm Buchse, Satz von 2
3444130
Leitgummiplattenelektrode 8x12 cm, 2 mm Buchse, Satz von 2
3444380
Silikon-Elektrode 5x5 cm

Seite 15 von 54 DE109-1634750-40 IFU
Viskoseschwämme für Plattenelektroden
1460273
Viskoseschwämme für Plattenelektrode 4x6 cm, Satz von 4
1460266
Viskoseschwämme für Plattenelektrode 6x8 cm, Satz von 4
1460275
Viskoseschwämme für Plattenelektrode 8x12 cm, Satz von 4
Fixierbanden
3444020
Fixierband 100x3 cm
3444021
Fixierband 250x3 cm
3444022
Fixierband 100x5 cm
3444023
Fixierband 250x5 cm
Punktelektroden
3444180
Punktelektrode (Stiftmodell), Ø 5 mm, 2 mm Buchse, inkl. 10 leitfähige
Gummikappen
Adapters
2523523
Adapter, 2 mm Buchse, 4 mm Stecker, schwarz
2523524
Adapter, 2 mm Buchse, 4 mm Stecker, rot
Patientenkabel
3444211
Patientenkabel, 2-adrig & 2 mm Stecker - Schwarz, mit farbigen Clips
Zusätzliches optionales Zubehör Endomed 182 Typ 3
Vakuumelektroden
3444503
Vakuumelektroden Ø 60 mm, Satz von 2 St.
3444504
Vakuumelektroden Ø 90 mm, Satz von 2 St.
3444509
Vakuumelektroden Ø 30 mm, Satz von 2 St.
Schwämme
3444505
Schwämme Ø 65 mm, Satz von 4 Stück (für Vakuumelektroden Ø 60 mm)
3444506
Schwämme Ø 95 mm, Satz von 4 Stück(für Vakuumelektroden Ø 90 mm)
3444516
Schwämme Ø 30 mm, Satz von 4 Stück(für Vakuumelektroden Ø 30 mm)
Saugwelle Elektrodenkabel
3444507
Saugwelle Elektrodenkabel schwarz, mit roten Steckern
3444508
Saugwelle Elektrodenkabel schwarz, mit schwarzen Steckern
Bestellinformationen
Die Bestelldaten des Endomed 182, der standardmäßigen Zubehörteile und des Sonderzubehörs
finden Sie auf unserer Website www.enraf-nonius.com.

Seite 16 von 54 DE109-1634750-40 IFU
5 Installation
Inspektion
Benachrichtigen Sie bitte Ihren Fachhändler vor Ort, falls Sie Transportschäden festgestellt
haben. Verwenden Sie in dem Fall das Gerät NICHT!
Das Gerät ist so aufzustellen, dass es seine Wärme ungehindert an die Umgebung abgeben
kann.
Gehen Sie unmittelbar nach dem Auspacken des Geräts wie folgt vor:
• Prüfen Sie anhand des Lieferscheins, ob die Lieferung komplett ist.
• Prüfen Sie, ob die Verpackung sämtliche in der Standardzubehörliste aufgeführte Teile enthält
(siehe Kapitel 4 „Verpackungsinhalt“ in dieser Gebrauchsanweisung).
• Überprüfen Sie die externen Komponenten und das Zubehör auf etwaige Transportschäden.
Auspacken
Endomed 182 ist speziell für den Transport in einer Einzelverpackung mit einem Füllmaterial
verpackt, das eigens für sicheren Transport und sichere Lagerung entwickelt wurde.
• Um das Gerät aus der Packung zu entnehmen stellen Sie den Karton auf eine glatte, ebene
Fläche.
• Öffnen Sie den Karton an der Oberseite und nehmen Sie das Polystyrol-Füllmaterial heraus.
• Seien Sie sehr vorsichtig, wenn Sie den Inhalt der Packung entnehmen.
Einrichtung des Geräts
Endomed 182 Typ 2:
• Schließen Sie das Kabel vom Strommodul [9] an Anschluss B [8] an.
Endomed 182 Typ 3:
• Schließen Sie das Kabel vom Strommodul [9] an Anschluss B [8] an.
• Schließen Sie das Kabel vom Vakuummodul [13] an Anschluss A [7] an.
Siehe Kapitel 3 - Gerätekomponenten in diesem Handbuch.
Anschluss der Netzspannung
Es darf NUR das mitgelieferte Netzkabel verwendet werden,
da sonst die Sicherheit des Patienten und der einwandfreie Betrieb des Geräts nicht
gewährleistet werden können.
Vergewissern Sie sich vor dem Anschluss dieses Geräts an den Netzstrom, dass die auf dem
Typenschild dieses Geräts angegebene Spannung und Frequenz dem verfügbaren Netzstrom
entsprechen.
Um die Gefahr eines Stromschlags zu vermeiden, darf dieses Gerät nur an ein Versorgungsnetz
mit geschützter Erde angeschlossen werden.
Stecken Sie das Netzkabel des Geräts in eine Wandsteckdose.
• Stecken Sie das Netzkabel in die Buchse [19] und schließen Sie es an eine Wandsteckdose an.
Trennung der Netzverbindung
• Wenn Sie die Behandlung beendet haben, schalten Sie das Gerät aus, indem Sie den
Netzschalter auf Aus stellen.
• Ziehen Sie das Netzkabel aus der Steckdose.
• Trennen Sie das Netzkabel von der Steckdose [19].

Seite 17 von 54 DE109-1634750-40 IFU
6 Bestimmungsgemäßer Gebrauch und vorgesehene Anwender
Bestimmungsgemäßer Gebrauch
Endomed 182 Typ 1
Das Endomed 182 Typ 1 ist ein Ein-Kanal-Elektrostimulator, es ist vorgesehen und entwickelt für den
Gebrauch durch medizinisches Fachpersonal zur Durchführung einer perkutanen Elektrolyse (PE)
mithilfe von Gleichstrom (DC) geringer Intensität.
Endomed 182 Typ 2 und 3
Endomed 182 Typ 2 und 3 sind 2-Kanal-Elektrostimulatoren, vorgesehen und entwickelt für den
Gebrauch durch medizinisches Fachpersonal zur Durchführung einer Schmerztherapie mit
Interferenzstrom (IFC) und TENS-Strom.
Die Schmerztherapie mithilfe von Elektrostimulation umfasst:
- die symptomatische Linderung chronischer hartnäckiger Schmerzen
- die Behandlung von Schmerzen im Zusammenhang mit posttraumatischen oder postoperativen
Zuständen
- die Linderung von arthritisbedingten Schmerzen
Die elektrische Stimulation erfolgt über Oberflächenelektroden auf der Haut, um bestimmte Arten
von Nervenfasern zu stimulieren. Eine Schmerzlinderung (Schmerzmodulation) kann erreicht
werden durch:
1. Blockieren der Weiterleitung von Informationen entlang der nozizeptiven Fasern (d. h. der
Schmerz produzierenden Fasern) durch Stimulierung der afferenten A-Fasern mit großem
Durchmesser
2. Freisetzung körpereigener Opioide durch Stimulation der afferenten und motorischen Fasern
mit kleinem Durchmesser
Vorgesehene Anwender
Endomed 182 ist zur Verwendung durch oder unter Aufsicht von professionellen Anwendern im
Bereich der physikalischen Medizin und Rehabilitation in professionellen Gesundheitseinrichtungen
vorgesehen und darf nur von diesen verwendet werden.
Zusätzlich für Endomed 182 Typ 1:
Wenn ein Angehöriger eines Gesundheitsberufs (Physiotherapeut, Arzt) die ultraschallgeführte
galvanische Elektrolysetherapie anwenden darf und darin geschult ist, darf er und hat gelernt:
-> Nadelpunktionen an einem Patienten durchzuführen,
-> Ultraschall anzuwenden,
-> die galvanische Elektrolysetherapie anzuwenden.

Seite 18 von 54 DE109-1634750-40 IFU
7 Indikationen
Indikationen Endomed 182 Typ 1
Perkutane Elektrolyse
Die Perkutane Elektrolyse (PE) kann zur Behandlung folgender Krankheiten verwendet werden:
• Patellaspitzensyndrom / Tendinitis der Patellarsehne („Jumper’s Knee“)
• Epicondylitis radialis humeri (Tennisellenbogen)
• Epicondylitis ulnaris humeri (Golferellenbogen)
• Myofasziales Schmerzsyndrom / Triggerpunkte
• Akutes Schleudertrauma (AWS)
• Schultererkrankungen (Tendopathien der Rotatorenmanschette, subakromiales
Schmerzsyndrom)
• Pubalgie (Schmerzen in der Leistengegend)
• Tendopathie am rückseitigen Oberschenkel
• Achillessehnenreizung
• Plantarfasziitis / Schmerzen in der Ferse
Indikationen Endomed 182 Typ 2 und 3
TENS
Linderung von akuten Schmerzen
• Postoperative Schmerzen
o Abdominal
o Thorakal
o Schmerzen nach einer orthopädischen Operation
• Wehenschmerzen und Schmerzen nach Wehentätigkeit
• Dysmenorrhö
• Orofaziale Schmerzen, einschließlich im Zusammenhang mit zahnmedizinischen Verfahren
• Physisches Trauma, einschließlich Rippenfrakturen und kleinerer medizinischer Eingriffe
Linderung chronischer Schmerzen
• Schmerzen im unteren Rücken
• Arthritisschmerzen, einschließlich Osteoarthrose, rheumatoide Arthritis
• Muskelschmerzen, einschließlich myofaszialer Schmerzen, Muskelverspannungen und
Schmerzen nach dem Training
• Neuropathische Schmerzen, einschließlich postamputativer Schmerzen
(Phantomschmerzen), postherpetischer Schmerzen, Trigeminusneuralgie
• Krebsbedingte Schmerzen, einschließlich Schmerzen aufgrund von Knochenmetastasen
• Komplexes regionales Schmerzsyndrom
Interferenzstrom
Linderung von akuten und chronischen Schmerzen, wie z.B:
• Postoperative Schmerz / orthopädischer Schmerz
• Schmerzen im unteren Rücken
• Nackenschmerzen
• Schulterschmerzen
• Arthritisschmerzen, einschließlich Osteoarthrose, rheumatoide Arthritis
• Muskelschmerzen, einschließlich myofaszialer Schmerzen, Muskelverspannungen,
Schmerzen nach dem Training und Fibromyalgie
Muskelstimulation
• Muskelkräftigung (allgemein)
• Stuhl- und Harninkontinenz
Funktionsstörungen des Darms
Erhöhung der lokalen (Haut-)Durchblutung

Seite 19 von 54 DE109-1634750-40 IFU
8 Kontraindikationen
Endomed 182 darf bei den im Folgenden genannten Symptomen oder
Gesundheitsbeschwerden NICHT verwendet werden.
Kontraindicationen Endomed 182 Typ 1
Kontraindikationen für die Anwendung
• Infektiöse Arthritis
• Herzerkrankungen / Herzrhythmusstörungen
• Schwangerschaft
• Hautgeschwüre und andere Hautinfektionen
• Endoprothesen und/oder Osteosynthesen
• Herzschrittmacher
• Onkologische Erkrankungen
• Thrombophlebitis / anamnestisch bekannte Gefäßinsuffizienz in den Beinen
• Koagulopathie / Antikoagulanzien
• Blutbildveränderung
• Menstruation
• Nadelphobie
• Angst vor Elektrostimulation
• Endokrine Drüsen
• Patienten mit eingeschränkter Sensibilität
• Patienten mit zentralen und peripheren neurologischen Erkrankungen
• Patienten mit neurovegetativen Störungen
• Pädiatrische Patienten
• Komplexe Erkrankungen
• Kognitive Störungen
• Drogen-, Medikamenten- oder Alkoholmissbrauch
Stellen, an denen keine Behandlung appliziert werden darf:
• Blutgefäße
• Endokrine Drüsen
• Organe
• Periphere Nerven (Endoneurium)
• Kopf, Augen, Hals, Thorax und der obere Teil des Rückens, der über dem Herz liegt
Vorsichtshinweise für die perkutane Elektrolyse
Regionen bei denen besondere Vorsicht geboten ist:
• Abdominalregion
• Interkostalregion (Vorsichtsmaßnahme gegen Pneumothorax)
• Thoraxregion (Vorsichtsmaßnahme gegen Pneumothorax)
• Thoraxapertur (Vorsichtsmaßnahme gegen Pneumothorax)
• Leistenregion, Kniekehle (Vorsichtsmaßnahme gegen Schädigung von Gefäß-Nerven-Strängen)

Seite 20 von 54 DE109-1634750-40 IFU
Kontraindicationen Endomed 182 Typ 2 und 3
Absolute Kontraindikationen:
• Nichtdiagnostizierte Schmerzen
• Aktive Implantate (inkl. Herzschrittmachern und implantierbarer Kardioverter-Defibrillatoren -
ICDs)
• Gewebeblutung (Hämorrhagie)
• Patienten, die nicht in der Lage sind, Anweisungen des Anwenders/Therapeuten zu verstehen
oder zu kooperieren.
Relative Kontraindikationen (= lokale Kontraindikationen):
• Schwangerschaft (nicht über dem Bauch/Beckenbereich anwenden)
• Maligne Tumoren (nicht über aktiven malignen Tumoren anwenden)
• Epilepsie (nicht an Hals oder Kopf anwenden)
• Herzstörungen wie etwa Rhythmusstörungen (nicht an der Brust anwenden)
• Elektrodenplatzierung im Augenbereich
• Elektrodenplatzierung über der vorderen Seite des Halses oder dem Karotissinus
• Elektrodenplatzierung zur Stromleitung durch den Brustkorb (d. h. Elektrodenpositionen vorne
und hinten)
• Elektrodenplatzierung an den Hoden
• Elektrodenplatzierung an aktiven Epiphysenregionen bei Kindern
• Elektrodenplatzierung an geschädigter Haut oder offenen Wunden
• Elektrodenplatzierung an dermatologischen Läsionen, z. B. Dermatitis, Ekzem oder
empfindlicher Haut
• Elektrodenplatzierung an Bereichen mit ischämischem Gewebe und/oder Thrombose
Hinweis: Es sind keine unerwünschten Auswirkungen der Anwendung einer TENS / Interferenzstrom
an der Haut über oder in der Nähe von Metallimplantaten bekannt. TENS / Interferenzstrom kann
auf intakter Haut über Implantaten, die Metall, Kunststoff oder Zement enthalten, angewendet
werden. Personen mit Gelenkersatz, der Metallkomponenten enthält, profitierten von einer
Behandlung mit Elektrostimulation und es traten keine Nebenwirkungen auf.
Vorsichtsmaßnahmen TENS und Interferenzstrom
In folgenden Fällen sind Sicherheits- und Vorsichtsmaßnahmen zu treffen:
• Bereiche mit gestörter Wahrnehmungsfähigkeit der Haut (Dysästhesie)
o Hyperästhesie (Allodynie/Hyperalgesie)
o Hypoästhesia
• Kontaktdermatitis
• Schwangerschaft
• Patienten, die empfindlich auf autonome Reaktionen bei der TENS reagieren (z. B. Übelkeit,
Benommenheit und Ohnmacht)
Potenzielle unerwünschte Wirkungen
Bei Anwendung einer therapeutischen elektrischen Stimulation wurde über Hautreizungen und
Verätzungen unter den Elektroden berichtet.
Bei Patienten mit besonders empfindlicher Haut können vereinzelt Hautreizungen auftreten. Im
Falle einer allergischen Reaktion auf das Elektrodengel ist die Behandlung abzubrechen und ein
Fachmann zu verständigen. Wenn während der Behandlung Anzeichen von Tachykardie und
Extrasystole auftreten, brechen Sie die Behandlung ab und wenden Sie sich an den zuständigen
Arzt.

Seite 21 von 54 DE109-1634750-40 IFU
9 Vorsichtshinweise
Wenn die Verwendung dieses Geräts eine unerwünschte Nebenwirkung, z. B. Tod oder eine
schwerwiegende Verletzung, verursacht oder dazu beiträgt, sind der Hersteller und die
zuständige Behörde des Mitgliedstaates UMGEHEND zu benachrichtigen!
Stellen Sie das Gerät außer Reichweite von Kindern auf.
Behalten Sie als Therapeut den Patienten und das Gerät stets im Auge.
Verwenden Sie das Gerät nicht in sogenannten Feuchträumen (Hydrotherapieräumen).
Dieses Gerät eignet sich nicht für den Betrieb in Umgebungen, in denen entflammbare
Anästhesiemischungen mit Luft, Sauerstoff oder Lachgas vorhanden sind.
Setzen Sie das Gerät nicht direktem Sonnenlicht, Hitze, die von einem Heizkörper
ausgestrahlt wird, übermäßigem Staub, Feuchtigkeit, Vibrationen und mechanischen Stößen
aus.
Das Gerät darf nur unter ständiger Aufsicht eines Arztes oder einer zugelassenen Fachperson
eingesetzt werden.
Benachrichtigen Sie bitte Ihren Fachhändler vor Ort, falls Sie Transportschäden festgestellt
haben. Verwenden Sie in dem Fall das Gerät NICHT!
Das Gerät ist so aufzustellen, dass es seine Wärme ungehindert an die Umgebung abgeben
kann.
Es darf NUR das mitgelieferte Netzkabel verwendet werden,
da sonst die Sicherheit des Patienten und der einwandfreie Betrieb des Geräts nicht
gewährleistet werden können.
Vergewissern Sie sich vor dem Anschluss dieses Geräts an den Netzstrom, dass die auf dem
Typenschild dieses Geräts angegebene Spannung und Frequenz dem verfügbaren Netzstrom
entsprechen.
Um die Gefahr eines Stromschlags zu vermeiden, darf dieses Gerät nur an ein Versorgungsnetz
mit geschützter Erde angeschlossen werden.
Verwenden Sie das Gerät nach extremen Temperaturschwankungen nicht!
Stellen Sie vor Beginn der Behandlung sicher, dass: Sie den Inhalt dieser Gebrauchsanweisung
gelesen und verstanden haben.
Stellen Sie vor Beginn der Behandlung sicher, dass: Sie sich strikt an die bei den
Vorsichtsmaßnahmen genannten WARNUNGEN und HINWEISE halten.
Stellen Sie vor Beginn der Behandlung sicher, dass: Der Patient auf mögliche Kontraindikationen
untersucht worden ist.
Der Anschlus von Zubehor, das nicht vom Hersteller vorgesehen ist, kann die Sicherheit des
Patienten und das korrekte Funktionieren des Gerates beeintrachtigen und ist daher
unzulassig.
Um Infektionen zu vermeiden, sollten Elektroden und Schwammpads nicht auf geschädigter
Haut verwendet werden.
Während der Behandlung darf der Patient keine unangenehmen Empfindungen empfinden,
die zu Schmerzen führen. Ein leichtes Erregungsempfinden ist zulässig.
Wenn infolge der Behandlung Kopfschmerzen, Schwindel, Ermüdung und/oder andere
(autonome Nerven-)Reaktionen auftreten, dann sollte die Folgebehandlung mit geringerer
Intensität erfolgen.
Es wird empfohlen, Diathermiegeräte (zum Beispiel Kurzwellen- und Mikrowellengeräte)
mindestens zwei Meter von Elektrostimulationsgeräten entfernt zu halten, da die Leistung von
Elektrostimulationsgeräten durch die unmittelbare Nähe zu einem (gepulsten) Kurzwellen-
oder Mikrowellengerät beeinträchtigt werden kann.
Die Stimulation sollte nicht über oder durch den Kopf, direkt auf den Augen, auf dem Mund,
an der Vorderseite des Halses (insbesondere am Karotissinus) oder über Elektroden auf der
Brust und dem oberen Rücken oder über das Herz erfolgen.

Seite 22 von 54 DE109-1634750-40 IFU
Das Anbringen von Elektroden in der Nähe des Thorax kann das Risiko von Herzflimmern
erhöhen.
Das gleichzeitige Anschließen eines Patienten an ein medizinisch-elektrisches
Hochfrequenzgerät kann an der Stelle der Stimulatorelektroden zu Verbrennungen und zu
einer möglichen Beschädigung des Stimulators führen.
Elektroden mit einer Stromdichte von mehr als 2 mA/cm² erfordern möglicherweise die
besondere Aufmerksamkeit des Bedieners.
Die mehrmalige Verwendung vorgelierter Elektroden führt zu einem raschen Verlust der
Leitfähigkeit und zu einer Verschlechterung des Haftvermögens.
Der Verlust der Haftung und das Austrocknen des Gels führen dazu, dass sich die Ränder
anheben, was die Stromdichte drastisch erhöhen, eine ungleichmäßige Verteilung des Stroms
über die Elektrodenfläche verursachen (Anstieg der Verbrennungsgefahr) und möglicherweise
dazu führen kann, dass sich die Elektrode verschiebt.
Veränderungen, die im Laufe der Zeit an selbstklebenden Elektroden auftreten, bergen
Risiken und können Hautreizungen und Beschwerden des Patienten hervorrufen.
Selbstklebende Elektroden sollten niemals bei mehr als jeweils einem Patienten angewendet
werden.
Reinigen Sie das Gerät und sein Zubehör regelmäßig, um die hygienische Sicherheit
aufrechtzuerhalten.
Schalten Sie das Gerät immer aus und ziehen Sie den Netzstecker aus der Steckdose, bevor Sie
mit Reinigungsarbeiten beginnen.
Reinigungsmittel nicht direkt auf die Glasplatte sprühen.
Verwenden Sie keine Reinigungsmittel, die starke Alkalien, Laugen oder Säuren enthalten und
keine fluorid- oder ammoniakhaltigen Reiniger.
Sorgen Sie dafür, dass während der Reinigung und Desinfektion keine Flüssigkeiten in das Gerät
oder das Zubehör eindringen können!
Trocknen Sie sämtliche Anschlussbuchsen und Stecker, die feucht geworden sind, sorgfältig ab,
bevor Sie das Gerät wieder benutzen!
Mechanische Stöße und/oder Vibrationen während der Reinigung des Geräts sind unter allen
Umständen zu VERMEIDEN!
Lassen Sie das Gerät nicht fallen!
Das Gerät sollte nicht verwendet werden, wenn mechanische Beschädigungen festgestellt
werden. Dazu gehört auch eine beschädigte Kabelisolierung.
Falls eine Fehlermeldung oder eine Warnmeldung erscheint, stellten Sie unmittelbar den
Betrieb des Geräts ein. Schalten Sie das Gerät aus und danach wieder ein. Wenn das Problem
bestehen bleibt, wenden Sie sich an den Lieferanten oder an Enraf-Nonius B.V.
Fehlermeldungen und Warnmeldungen weisen auf ein internes Problem im Gerät hin. In
diesem Fall muss das Gerät von einem von Enraf-Nonius B.V. zertifizierten Servicetechniker
geprüft werden, bevor das System wieder in Betrieb genommen oder benutzt werden darf.
Die Verwendung eines Geräts trotz Fehler- oder Warnmeldung kann Verletzungen des
Patienten oder des Bedieners oder Beschädigungen des Systems zur Folge haben.
Im Falle einer Fehlermeldung oder anderer offensichtlicher Defekte ziehen Sie sofort den
Netzstecker und benachrichtigen Sie einen zertifizierten Servicetechniker.
Bei Eindringen von Flüssigkeiten ziehen Sie den Netzstecker und lassen Sie das Gerät von
einer autorisierten Person überprüfen.
Öffnen der Ausrüstung durch nicht autorisierte Dienstleister ist nicht gestattet und beendet
jeglichen Garantieanspruch.
Der Hersteller haftet nicht für die Ergebnisse der Wartungsarbeiten oder Reparaturen, die
durch unbefugte Personen ausgeführt wurden!
Nur von Enraf-Nonius autorisierte Servicetechniker dürfen dieses Gerät gemäß den
Serviceinformationen warten oder modifizieren.

Seite 23 von 54 DE109-1634750-40 IFU
Das Gerät darf nicht gewartet werden, wenn es in Betrieb oder mit einem Patienten
verbunden ist.
Es wird empfohlen, Endomed 182 jährlich von autorisiertem Personal von Enraf-Nonius oder
von dessen autorisiertem Fachhändler überprüfen zu lassen.
Medizinische elektrische Geräte wie Endomed 182 unterliegen speziellen Vorsichtsmaßnahmen
hinsichtlich der elektromagnetischen Verträglichkeit (EMV) und müssen in Übereinstimmung
mit den EMV-Empfehlungen in der Gebrauchsanweisung und den Begleitdokumenten
installiert und in Betrieb genommen werden.
Die Verwendung dieses Geräts neben oder gestapelt auf anderen Geräten sollte vermieden
werden, da dies zu fehlerhaftem Betrieb führen könnte. Falls eine solche Verwendung
erforderlich ist, sollten dieses Gerät sowie die anderen Geräte beobachtet werden, um
sicherzustellen, dass sie normal funktionieren.
Die Verwendung von Zubehör, Transducern und Kabeln, die nicht aufgeführt oder nicht vom
Hersteller des Geräts zur Verfügung gestellt wurden, kann zu erhöhten elektromagnetischen
Emissionen oder zu einer reduzierten elektromagnetischen Immunität dieses Geräts und zu
einem unsachgemäßen Betrieb führen.
Tragbare HF-Kommunikationsgeräte (einschließlich Peripheriegeräten wie Antennenkabel und
externe Antennen) sollten nicht näher als 30 cm an einem Teil des Endomed 182 verwendet
werden, einschließlich der vom Hersteller angegebenen Kabel. Andernfalls kann es zu
Leistungseinbußen bei dem Gerät kommen.
Endomed 182 darf nur mit dem Original-Netzkabel betrieben werden, das in der Liste des
Lieferumfangs angegeben ist. Der Betrieb des Geräts mit einem anderen Netzkabel kann zu
stärkeren Emissionen oder einer geringeren Immunität des Geräts gegenüber Interferenzen
führen.

Seite 24 von 54 DE109-1634750-40 IFU
10 Bedienung
Konfiguration
Verwenden Sie das Gerät nach extremen Temperaturschwankungen nicht!
Häufig verwendete Funktionen
Auswahl der Schaltflächen "Klinische Protokolle" (nur gültig für Endomed 182 Typ 2 und 3),
"Favoriten" und "Manuelle Bedienung" auf dem Touchscreen.
Einschalten
• Schalten Sie das Gerät ein, indem Sie die Ein/Aus-Taste auf der Rückseite des Gerätes drücken.
• Nach dem Einschalten initialisiert sich das Gerät und es wird ein Begrüßungsbildschirm
angezeigt, während das Gerät einen Selbsttest durchführt.
• Am Ende des Selbsttests gelangt das Gerät in das Hauptmenü und ist einsatzbereit.
Wenn das Gerät eingeschaltet ist, werden alle wichtigen Funktionen über einen internen
Mikroprozessor gesteuert. Während des Betriebs des Geräts wird die tatsächliche Stromabgabe
kontinuierlich gemessen und mit der gewünschten Abgabe verglichen. Wenn eine fehlerhafte
Situation erkannt wird, schaltet das Gerät den Strom sofort aus.
Navigation
Hauptmenü
Das Hauptmenü ermöglicht den Zugriff auf alle Funktionen des Geräts. Das Hauptmenü bietet
einen strukturierten Zugriff auf alle im Gerät verfügbaren Therapien mit den entsprechenden
Standardparametern. Ein Menüpunkt wird einfach durch Berühren der Schaltfläche ausgewählt, um
so zum nächsten Bildschirm zu navigieren. Durch Berühren der Zurück-Schaltfläche am oberen
Bildschirmrand können Sie zum vorherigen Bildschirm zurück navigieren.
• Wählen Sie „Klinische
Protokolle", um mit den
voreingestellten
Protokollen zu arbeiten.
Dies gilt nicht für
Endomed 182 Typ 1
• Wählen Sie „Favoriten",
um ein manuell
gespeichertes Protokoll zu
verwenden
• Wählen Sie „Manuelle
Bedienung", um alle
Parameter manuell
einzustellen
• Wählen Sie
„Systemeinstellungen", um
das Einstellungsmenü zu
öffnen.
Endomed 182 Typ 1 Hauptmenü
Endomed 182 Type 2 und 3
Hauptmenü

Seite 25 von 54 DE109-1634750-40 IFU
Systemeinstellungen
Wählen Sie im Hauptmenü Systemeinstellungen, um verschiedene Einstellungen vorzunehmen, die
Softwareversion zu überprüfen oder das Gerät auf die Werkseinstellungen zurückzusetzen. Die
Optionen Audiosignal, Signalton und Signalton Dauer sind nur in den Endomed 182 Typ 2 und 3
verfügbar.
Sprache einstellen
1) Wählen Sie
„Systemeinstellungen"
2) Wählen Sie „Sprache"
3) Wählen Sie mit den
Tasten die gewünschte Sprache
aus.
4) Bestätigen Sie mit OK und
kehren Sie zum vorherigen
Menü zurück.
Helligkeit einstellen
So ändern Sie die Helligkeit
des Bildschirms:
1) Wählen Sie „Helligkeit"
2) Stellen Sie die Helligkeit
über die Tasten ein.
Reichweite: 10 – 100%
3) Bestätigen Sie mit OK und
kehren Sie zum vorherigen
Menü zurück.

Seite 26 von 54 DE109-1634750-40 IFU
System Info
1) Wählen Sie "System Info”
Im nächsten Bildschirm finden
Sie Informationen über das
Gerät.
Die aktuell installierte
Softwareversion wird
angezeigt.
2) Drücken Sie „Zurück”, um
zum vorherigen Menü
zurückzukehren.
Audiosignal
Endomed 182 Typ 2 und 3:
Wählen Sie diese Option, um
Audiosignale am Ende der
Behandlung ein- oder
auszuschalten.
1) Wählen Sie "Audiosignal"
2) Schalten Sie das
Audiosignal ein oder aus
3) Drücken Sie „Zurück”, um
zum vorherigen Menü
zurückzukehren.

Seite 27 von 54 DE109-1634750-40 IFU
Signalton und Signalton Dauer
Endomed 182 Typ 2 und 3:
1) Wählen Sie "Signalton" oder
"Signalton Dauer"
Signalton bietet Zugang zu 7
verschiedenen Melodien, um
das Ende einer Behandlung zu
signalisieren.
Signalton Dauer bietet Zugang
zu 7 verschiedenen Intervallen,
um das Ende einer Behandlung
zu signalisieren.
Wartung
Durch Wiederherstellen der
Werkseinstellungen werden
alle auf dem Gerät
gespeicherten Favoriten
gelöscht und alle
Systemeinstellungen gelöscht,
wodurch das Gerät wieder in
den ursprünglichen
Werkszustand versetzt wird.
Das Service-menü ist für
Enraf-Nonius-qualifizierte
Serviceorganisationen
bestimmt und kann nur mit
einem Zugangscode
aufgerufen werden.
Wasserbehälter reinigen
aktiviert die Pumpe. Siehe
Kapitel 12 Wartung und
Störungsbeseitigung. (Gilt nur
für Endomed 182 Typ 3.)
1) Wählen Sie “Wartung”
(Anwendbar auf Endomed 182
Typ 2 und 3)

Seite 28 von 54 DE109-1634750-40 IFU
Manuelle Bedienung Endomed 182 Typ 1
Endomed 182 Typ 1 hat einen Ausgangskanal. Siehe Kapitel 11 für den Anschluss der Elektroden.
1) Wählen Sie "Manuelle
Bedienung" im Hauptmenü.
Wählen Sie (K), um die
Behandlungszeit einzustellen
Wählen Sie (L), um die
Intensität einzustellen
2) Behandlungszeit einstellen
Option: 3 s / 10 s / 60 s
Oder über die Tasten
3) Intensität einstellen
Option: 1 mA / 3 mA / 5 mA
Oder über die Tasten
4) Drücken Sie die Start-Taste
(oder den Fußschalter, wenn
dieser angeschlossen ist), um
die Behandlung zu starten
5) Drücken Sie die Stopptaste
(oder den Fußschalter, wenn
dieser angeschlossen ist), um
die Behandlung zu beenden.
Die Behandlung stoppt automatisch,
wenn die Behandlungszeit abgelaufen
ist.
K
L

Seite 29 von 54 DE109-1634750-40 IFU
Klinische Protokolle
Für die Endomed 182 Typ 2 und 3 ist eine Liste der gängigen Elektrotherapie-Behandlungen unter
Klinische Protokolle zu finden. Diese evidenzbasierten Protokolle wurden von professionellen und
fachkundigen Anwendern nach jahrelanger Erfahrung auf diesem Gebiet erstellt.
Die voreingestellten klinischen Protokolle sind einstellbar und wiederbeschreibbar. Siehe Kapitel 11
für den Anschluss der Elektroden.
1) Wählen Sie „Klinische
Protokolle" im Hauptmenü,
um die Liste zu aktivieren
2) Wählen Sie die Taste,
um durch die Liste zu blättern.
3) Wählen Sie das Icon für
weitere Informationen über
die Protokoll
4) Wählen Sie das gewählte
Klinische Protokoll, um zum
Parameterbildschirm zu
gelangen
Protokoll-Informations-
bildschirm
5) Berühren Sie die
Tasten, um durch die Seiten
zu blättern
6) Wählen Sie OK, um zum
Parameterbildschirm zu
gelangen, oder Zurück, um
zum Menü Klinische
Protokolle zurückzukehren.

Seite 30 von 54 DE109-1634750-40 IFU
7) Der Parameterbildschirm
zeigt alle Parameter auf einen
Blick
8) Die voreingestellten
Parameter des klinischen
Protokolls können angepasst
werden
9) Drücken Sie die Kanal-
Registerkarte 1 oder 2 unten
auf dem Bildschirm, um den
Intensitätspegel zu ändern.
10) Stellen Sie den
Intensitätspegel mit den
Tasten
11) Bestätigen Sie mit OK und
kehren Sie zum vorherigen
Menü zurück.
12) Das Protokoll beginnt nach
Festlegung der Intensität
13) Das Protokoll kann durch
Drücken des Stopp-Symbols
(A) auf dem Touchscreen
gestoppt werden. Das Protokoll
wird automatisch gestoppt,
wenn die Behandlungszeit
abgelaufen ist.
A

Seite 31 von 54 DE109-1634750-40 IFU
Manuelle Bedienung Endomed 182 Typ 2 und Typ 3
Mit Manuelle Bedienung können persönliche Parametereinstellungen für die Elektrotherapie
definiert werden. Der Endomed 182 Typ 2 und 3 hat zwei unabhängige Ausgangskanäle. Um den
Ausgangskanal auszuwählen, berühren Sie die Kanal-Registerkarte unten auf dem Bildschirm. Siehe
Kapitel 11 für den Anschluss der Elektroden.
1) Wählen Sie "Manuelle
Bedienung" im Hauptmenü
2) Wählen Sie die gewünschte
Stromform; der
Parameterbildschirm erscheint
3) Abhängig von der gewählten
Stromform können
verschiedene Parameter
eingestellt werden.
Parameter einstellen: Frequenz
1) Wählen Sie Frequenz (B)
2) Stellen Sie die Frequenz
über die Tasten ein
Reichweite: 1 Hz – 200 Hz
3) Bestätigen Sie mit OK und
kehren Sie zum vorherigen
Menü zurück.
B

Seite 32 von 54 DE109-1634750-40 IFU
Parameter einstellen: Burstfrequenz
1) Wählen Sie Burstfrequenz
(C)
2) Stellen Sie die
Burstfrequenz ein
Option: 1 Hz / 2 Hz / 4 Hz
3) Bestätigen Sie mit OK und
kehren Sie zum vorherigen
Menü zurück.
Parameter einstellen: Modulationsfrequenz
1) Wählen Sie die
Modulationsfrequenz (D)
2) Stellen Sie die
Modulationsfrequenz über die
Tasten ein
Reichweite: 1 Hz - 180 Hz
3) Bestätigen Sie mit OK und
kehren Sie zum vorherigen
Menü zurück.
D
C

Seite 33 von 54 DE109-1634750-40 IFU
Parameter einstellen: Modulation Zeit
1) Wählen Sie
Modulationszeit (E)
2) Stellen Sie die Modulation
Zeit ein
Option:
1-1 Sekunden
6-6 Sekunden
1-30 Sekunden
3) Bestätigen Sie mit OK und
kehren Sie zum vorherigen
Menü zurück.
Parameter einstellen: Behandlungszeit
1) Wählen Sie die
Behandlungszeit (F)
2) Stellen Sie die
Behandlungszeit über die
Tasten ein
Reichweite: 0 bis 60 Minuten
3) Bestätigen Sie mit OK und
kehren Sie zum vorherigen
Menü zurück.
E
F

Seite 34 von 54 DE109-1634750-40 IFU
Parameter einstellen: Vakuummodul
Mit dem Endomed 182 Typ 3
ist es möglich, Vakuum-
elektroden zu verwenden
1) Wählen Sie Vakuum (G)
2) Stellen Sie Vakuum-
Parameter ein
Option: gepulster Modus 1 Hz
/ gepulster Modus 2 Hz /
kontinuierlich
3) Stellen Sie den Druck der
Vakuumsaugnäpfe über die
Tasten
Die Vakuumsaugnäpfe
werden automatisch
ausgewählt, wenn die Pumpe
zu laufen beginnt
Parameter einstellen: Intensität
1) Drücken Sie die Kanal-
Registerkarte 1 oder 2 (H) am
unteren Rand des Bildschirms,
um den Intensitätspegel
einzustellen (nach der
Einstellung der
Behandlungszeit)
2) Stellen Sie die Intensität mit
den Tasten
3) Bestätigen Sie mit OK und
kehren Sie zum vorherigen
Menü zurück.
4) Das Programm beginnt nach
Einstellung der Intensität
5) Das Programm kann durch
Drücken des Stopp-Symbols
auf dem Touchscreen
angehalten werden. Das
Programm stoppt automatisch,
wenn die Behandlungszeit
abgelaufen ist.
H
G

Seite 35 von 54 DE109-1634750-40 IFU
Parameter einstellen: Balance-Steuerung
Für 4P Interferenzstrom ist die
Balance-Steuerungsoption
verfügbar, nachdem die
Intensität eingestellt wurde.
Mit der Balance-Steuerung
kann die Intensität von Kanal 1
relativ zu Kanal 2 erhöht oder
verringert werden. Eine
Erhöhung der Intensität von
Kanal 1 verringert automatisch
die Intensität von Kanal 2 und
umgekehrt.
1) Wählen Sie Balance-
Steuerung (I)
2) Stellen Sie Parameter für die
Balance-Steuerung ein
3) Bestätigen Sie mit OK und
kehren Sie zum vorherigen
Menü zurück.
Parameter einstellen: Vektor-Ansicht
Für 4P Isoplanar- Vektor ist
die Vektor-Ansicht nach
Beginn der Behandlung
verfügbar.
1) Wählen Sie Vektor-Ansicht
(J)
In diesem Bildschirm ist eine
Animation der rhythmischen
Schrumpf- und
Schwellungsringe sowie der
verbleibenden
Behandlungszeit und des
Intensitätsniveaus zu sehen.
J
I

Seite 36 von 54 DE109-1634750-40 IFU
Favoriten
Vor der Durchführung eines geänderten klinischen Protokolls oder einer manuellen Einstellung
kann es zur späteren Verwendung unter Favoriten gespeichert werden.
Wenn alle Parameter im Behandlungsbildschirm vollständig wie gewünscht eingestellt sind, können
Sie die Einstellungen durch Drücken der Speichertaste als Favoriten speichern.
Die Favoriten können gespeichert werden, solange die Behandlung noch nicht gestartet wurde.
1) Drücken Sie Speichern (M),
um die Programmeinstellungen
zu speichern
2) Wählen Sie die
Programmnummer mit den
Tasten aus.
Für die Endomed 182 stehen
20 Speicherplätze zur
Verfügung.
3) Mit OK bestätigen
4) Geben Sie einen Namen für
Ihren Favoriten ein
5) Drücken Sie OK, um den
Favoriten zu speichern
M

Seite 37 von 54 DE109-1634750-40 IFU
Laden und Löschen von Favoriten
1) Wählen Sie „Favoriten" im
Hauptmenü
2) Um ein Programm zu laden,
wählen Sie einen Favoriten
über die Tasten.
Es erscheint der Parameter-
Bildschirm.
3) Um einen Favoriten zu
löschen, drücken Sie die
Löschtaste (N) und wählen den
zu löschenden Favoriten mit
den Tasten aus.
4) Drücken Sie OK, um den
Favoriten dauerhaft zu löschen.
N

Seite 38 von 54 DE109-1634750-40 IFU
11 Informationen zur Anwendung
Stellen Sie vor Beginn der Behandlung sicher, dass: Sie den Inhalt dieser Gebrauchsanweisung
gelesen und verstanden haben.
Stellen Sie vor Beginn der Behandlung sicher, dass: Sie sich strikt an die bei den
Vorsichtsmaßnahmen genannten WARNUNGEN und HINWEISE halten.
Stellen Sie vor Beginn der Behandlung sicher, dass: Der Patient auf mögliche
Kontraindikationen untersucht worden ist.
Der Anschlus von Zubehor, das nicht vom Hersteller vorgesehen ist, kann die Sicherheit des
Patienten und das korrekte Funktionieren des Gerates beeintrachtigen und ist daher
unzulassig.
Um Infektionen zu vermeiden, sollten Elektroden und Schwammpads nicht auf geschädigter
Haut verwendet werden.
Während der Behandlung darf der Patient keine unangenehmen Empfindungen empfinden,
die zu Schmerzen führen. Ein leichtes Erregungsempfinden ist zulässig.
Wenn infolge der Behandlung Kopfschmerzen, Schwindel, Ermüdung und/oder andere
(autonome Nerven-)Reaktionen auftreten, dann sollte die Folgebehandlung mit geringerer
Intensität erfolgen.
Es wird empfohlen, Diathermiegeräte (zum Beispiel Kurzwellen- und Mikrowellengeräte)
mindestens zwei Meter von Elektrostimulationsgeräten entfernt zu halten, da die Leistung von
Elektrostimulationsgeräten durch die unmittelbare Nähe zu einem (gepulsten) Kurzwellen-
oder Mikrowellengerät beeinträchtigt werden kann.
Die Stimulation sollte nicht über oder durch den Kopf, direkt auf den Augen, auf dem Mund,
an der Vorderseite des Halses (insbesondere am Karotissinus) oder über Elektroden auf der
Brust und dem oberen Rücken oder über das Herz erfolgen.
Das Anbringen von Elektroden in der Nähe des Thorax kann das Risiko von Herzflimmern
erhöhen.
Das gleichzeitige Anschließen eines Patienten an ein medizinisch-elektrisches
Hochfrequenzgerät kann an der Stelle der Stimulatorelektroden zu Verbrennungen und zu
einer möglichen Beschädigung des Stimulators führen.
Elektroden mit einer Stromdichte von mehr als 2 mA/cm² erfordern möglicherweise die
besondere Aufmerksamkeit des Bedieners.
Anschluss der Elektroden
Siehe Kapitel 3 für die Beschreibung der nummerierten Teile.
Endomed 182 Typ 1
• Stecken Sie das DC-Referenzkabel [5] in den entsprechenden Anschluss [3]
• Schließen Sie die blanke Masseelektrode [4] an das DC-Referenzkabel [5] an
• Verwendung der blanken Masseelektrode: Während der Behandlung muss der Patient die
blanke Masseelektrode in der Hand halten

Seite 39 von 54 DE109-1634750-40 IFU
• Stecken Sie das Kabel des Elektrodenhalters [6] in den entsprechenden Anschluss [2]
• Stecken Sie die Nadel (nicht mitgeliefert) mithilfe des Einfädelsystems in den Elektrodenhalter;
es ermöglicht, dass der Elektrodenhalter sich öffnet, die Nadel eingeführt wird und der
Elektrodenhalter sich wieder schließt.
• Der Nadelhalter ist mit einem Start/Stop-Knopf versehen, mit dem der Stromfluss manuell
gestartet oder unterbrochen wird.
Endomed 182 Typ 2
• Stecken Sie die Patientenkabel in Anschluss 1 [10] und/oder Anschluss 2 [11] am Strommodul
[9] (roter Stecker in den roten Anschluss, schwarzer Stecker in den schwarzen Anschluss).
• Schließen Sie die Elektroden an die Patientenkabel an.
Endomed 182 Typ 3
• Zur Anwendung von Klebeelektroden oder Gummielektroden: Stecken Sie die Patientenkabel in
die oberen Anschlüsse [15] des Vakuummoduls (13) und schließen Sie die Elektroden an die
Patientenkabel an (roter Stecker in den roten Anschluss, schwarzer Stecker in den schwarzen
Anschluss).
• Zur Anwendung von Vakuumelektroden: Schließen Sie die Vakuumleitungsschläuche an die
unteren Anschlüsse [16] des Vakuummoduls [13] an und schließen Sie die Vakuumelektroden
an die Vakuumleitungsschläuche an (roter Stecker in den roten Anschluss, schwarzer Stecker in
den schwarzen Anschluss).
Behandlung
Vor der Behandlung
• Die Haut der betroffenen Stelle wird mit Seife oder 70-prozentigem Alkohol gereinigt (zur
Entfernung von Fett)
• Es wird empfohlen, behaarte Stellen zu rasieren
• Prüfen Sie die Empfindlichkeit der Behandlungszone
• Positionieren Sie die Elektroden und/oder Schwämme (vergessen Sie nicht, diese zu befeuchten)
• Befolgen Sie die Bedienungsanleitung in Kapitel 10, wie Sie die Einstellungen anpassen und die
Behandlung starten und beenden können
Während der Behandlung
• Die Intensität muss auf den gewünschten Wert eingestellt sein.
• Der Patient wird regelmäßig gebeten, über alle Empfindungen, die er verspürt, Rückmeldung zu
geben. Gegebenenfalls wird die Behandlung modifiziert.
Ende der Behandlung
• Die Behandlung kann beendet werden, indem das Stopp-Symbol auf dem Touch-Screen
berührt oder der Timer auf Null gesetzt wird. Die Behandlung stoppt automatisch nach Ablauf
der eingestellten Behandlungsdauer.
Nach der Behandlung
• Nehmen Sie die Elektroden und/oder Schwämme ab.
• Die Haut des Patienten wird mit einem Handtuch oder Papiertaschentuch gereinigt.
• Die zu erwartenden Effekte werden geprüft (z. B. Schmerzen, Durchblutung und Mobilität).
• Der Patient wird gebeten, sich anschließend zu womöglich aufgetretenen Reaktionen zu
äußern.

Seite 40 von 54 DE109-1634750-40 IFU
Endomed 182 Typ 1:
Perkutane Electrolyse
Die perkutane Elektrolyse (PE) ist eine nicht-pharmakologische, minimalinvasive
Behandlungsmethode für chronische Tendopathien und hat im Vergleich zu pharmakologischen
Interventionen wenige Nebenwirkungen. Die PE wird gewöhnlich von den meisten Patienten gut
vertragen und Komplikationen und Nebenwirkungen sind extrem selten. Die Patienten sollten
jedoch über potenzielle Risiken im Zusammenhang mit der Anwendung der perkutanen Elektrolyse
informiert werden:
• Die Behandlung kann leichte Schmerzen hervorrufen, die normalerweise 48 bis 72 Stunden
anhalten.
Eine der häufigsten interventionsbedingten Nebenwirkungen sind Beschwerden im
Behandlungsbereich aufgrund des Einführens der Nadel. Während der Applikation des galvanischen
Stroms können mittelstarke bis starke Schmerzen (je nach der verwendeten Intensität) auftreten. Vor
der perkutanen Elektrolyse werden normalerweise keine Lokalanästhetika injiziert, da das Verfahren
allgemein von den Patienten gut vertragen wird (die Applikation des galvanischen Stroms kann
jederzeit beendet werden, wenn der Schmerz nicht erträglich ist). Außerdem würde die Anwendung
von Spritzen zur Injektion der Anästhetika die gesamte Invasivität der Intervention deutlich erhöhen.
Die Anwendung von Anästhetika bleibt jedoch eine erwägenswerte Option.
• Vasovagale Reaktionen während und unmittelbar nach der Intervention
Die perkutane Elektrolyse beeinflusst das vegetative Nervensystem. Wie bei jedem Verfahren mit
Nadelung wurden während perkutaner Elektrolysen vagale Reaktionen (wie Blässe, Schwitzen,
Piloarrektion und Kälte der Haut) beobachtet. Es gibt Informationen aus mehreren Studien über das
potenzielle Risiko vasovagaler Reaktionen. Diese Reaktionen sind weitgehend auf die Wirkung der
Nadelung und nicht nur des Stroms zurückzuführen.
• Blutung im Bereich des Nadeleinstichs
Nach der Behandlung kann ein Druckverband angelegt werden, aber dies ist normalerweise nicht
notwendig.
Die Anwendung von Eis oder Einnahme von entzündungshemmenden Arzneimitteln (NSAR)
innerhalb von 72 Stunden nach der Behandlung wird nicht empfohlen, da dies dem erwarteten
therapeutischen Effekt (einen kontrollierten Entzündungsprozess einzuleiten) entgegenwirken würde.
Akupunkturnadeln
Es wird die Verwendung von hochwertigen, sterilen Einweg-Akupunkturnadeln mit medizinischer
CE-Zulassung, einschließlich der Nummer der Benannten Stelle, empfohlen. Enraf-Nonius liefert
keine Nadeln. Die Nadel sollte mit der Applikation einer ultraschallgeführten Elektrolyse kompatibel
sein. Hinsichtlich der Abmessungen der Nadel achten Sie bitte stets darauf, die korrekte Dicke und
Länge der Nadel für die zu behandelnde Art der Verletzung zu wählen.
• Nadeldurchmesser: 0,30 mm–0,35 mm
• Äußerer Durchmesser des Griffs: 1,25 mm–1,45 mm
• Länge des Nadelkörpers: 20 mm–100 mm
• Länge des Griffs: 25 mm–30 mm

Seite 41 von 54 DE109-1634750-40 IFU
Fußschalter
Das Endomed 182 Typ 1 hat einen optionalen Fußschalter, der mit Anschluss A [7] (siehe Kapitel 3)
verbunden werden kann.
Positionieren Sie den Fußschalter so, dass er während der
Behandlung leicht erreichbar ist. Die Steuereinheit des
Fußschalters ist richtungsunabhängig, daher ist es nicht
notwendig, den Fußschalter exakt auszurichten.
Beachten Sie bitte, dass nur leichter Druck auf den Schalter
ausgeübt werden muss, um ihn nicht zu beschädigen. Benutzen
Sie zur Bedienung des Fußschalters den Vorderfuß, nicht die
Ferse.
Drücken Sie einmal auf den Fußschalter, um die Behandlung zu aktivieren. Drücken Sie den
Fußschalter erneut, um die Behandlung zu beenden.
Endomed 182 Typ 2 und 3:
TENS / Interferenzstrom
Protokoll zur sicheren Anwendung von TENS / Interferenzstrom
• Kontraindikationen auf Seiten des Patienten überprüfen.
• Die Haut mit einem stumpfen/spitzen Gegenstand auf normale Wahrnehmungsfähigkeit
prüfen.
• Das Gerät sollte ausgeschaltet und die elektrischen Leitungen getrennt sein.
• Die elektrischen Parameter für TENS / Interferenzstrom bei ausgeschaltetem Gerät einstellen.
• Die Elektroden an die Stifte des Anschlusskabels anbringen und die Elektroden auf der Haut des
Patienten positionieren.
• Sicherstellen, dass das Gerät nach wie vor ausgeschaltet ist, und das Elektrodenkabel am Gerät
anschließen.
• Das Gerät einschalten.
• Die Intensität allmählich (langsam) weiter erhöhen, bis der Patient ein starkes, aber
angenehmes „Kribbeln“ verspürt.
• Diese Intensität sollte nicht schmerzhaft sein oder Muskelkontraktionen verursachen.
Protokoll zur sicheren Beendigung der TENS / Interferenzstrom
• Die Intensität allmählich (langsam) reduzieren, bis der Patient kein Kribbeln mehr verspürt.
• Das Gerät ausschalten.
• Das Elektrodenkabel vom Gerät abziehen.
• Die Elektroden von den Stiften am Anschlusskabel lösen.
• Die Elektroden von der Haut des Patienten lösen.

Seite 42 von 54 DE109-1634750-40 IFU
Endomed 182 Typ 2 und 3:
Flexible Gummielektroden
Wir empfehlen die Verwendung der flexiblen Gummielektroden in Kombination mit den
mitgelieferten Schwammpads. Bei richtiger Befeuchtung sorgen die Schwammpads für eine
niedrige Impedanz zwischen Haut und Stimulator während der Behandlung und lassen sich
anschließend leicht reinigen. Befolgen Sie die folgenden Richtlinien, wenn Sie diese Elektroden
verwenden.
• Spülen Sie die Schwammpads vor dem ersten Gebrauch gründlich in warmem Leitungswasser
aus, um das Imprägniermittel zu entfernen.
• Lassen Sie die Schwammpolster vor dem Auftragen mit Leitungswasser vollsaugen. Aufgrund
der verbesserten elektrischen Leitung ist eine Salzlösung jedoch zu bevorzugen.
• Die mitgelieferten Schwammpads bestehen aus drei Schichten. Bei Wechselstrom eine
Schwammschicht zwischen Haut und Elektrode anbringen, um den Widerstand zu minimieren.
• Befestigen Sie die Elektroden-/Schwammpad-Einheit mit den mitgelieferten Fixierungsgurten
am Patienten. Verwenden Sie je nach Elektrodengröße zwei oder drei Umwicklungen, um die
Kontaktfläche zu maximieren. Beachten Sie die Abbildungen unten.
• Es ist wichtig, dass die Elektroden während der gesamten Behandlung in vollständigem Kontakt
bleiben, ohne dass sich die Rändern anheben.
• Der Ausgabemodus von Endomed 182 ist Konstantstrom (CC). Dadurch bleibt die eingestellte
Stromamplitude auch dann erhalten, wenn die Impedanz der Schwammpads während der
Behandlung aufgrund von Wasserverdunstung zunimmt.
• Halten Sie die Schwammpads während der Behandlung gut angefeuchtet (bei leichtem Druck
tropfnass). Befeuchten Sie diese erneut, wenn die Behandlung länger als 10 Minuten dauert.
• Reinigen Sie die Schwammpads nach Gebrauch wie unter „Reinigung und Desinfektion“
beschrieben.
Falsches Anbringen der Fixiergurte. Dies führt zu
schlechter elektrischer Leitfähigkeit.
Richtiges Anbringen der Fixiergurte. Dies führt zu guter
elektrischer Leitfähigkeit.

Seite 43 von 54 DE109-1634750-40 IFU
Endomed 182 Typ 2 und 3:
Selbstklebende Elektroden
Die mehrmalige Verwendung vorgelierter Elektroden führt zu einem raschen Verlust der
Leitfähigkeit und zu einer Verschlechterung des Haftvermögens.
Der Verlust der Haftung und das Austrocknen des Gels führen dazu, dass sich die Ränder
anheben, was die Stromdichte drastisch erhöhen, eine ungleichmäßige Verteilung des Stroms
über die Elektrodenfläche verursachen (Anstieg der Verbrennungsgefahr) und möglicherweise
dazu führen kann, dass sich die Elektrode verschiebt.
Veränderungen, die im Laufe der Zeit an selbstklebenden Elektroden auftreten, bergen
Risiken und können Hautreizungen und Beschwerden des Patienten hervorrufen.
Selbstklebende Elektroden sollten niemals bei mehr als jeweils einem Patienten angewendet
werden.
Selbstklebende Elektroden haben eine höhere Serienimpedanz als flexible Gummielektroden. Dies
kann dazu führen, dass der Stimulator die Behandlung bei höheren Stromamplituden beendet. In
diesem Fall wird empfohlen, die Behandlung mit flexiblen Gummielektroden kombiniert mit
ordnungsgemäß angefeuchteten Schwammpads fortzusetzen.
Endomed 182 Typ 3:
Vakuumelektroden
Es besteht eine Auswahl an großen und kleinen Elektroden. Die Flächen der Elektroden entsprechen
denen der flexiblen 4 x 6 cm, 6 x 8 cm und 8 x 12 cm Gummi-Elektroden. Die Vakuumelektroden
sind flexibel genug, um einen optimalen Hautkontakt zu sichern, aber fest genug, um jegliche
Änderungen im Umriß der Behandlungsfläche zu verhindern, wodurch der Massageeffekt des
Impulsvakuums voll ausgenutzt werden kann.
Die Massage, die durch die Saugkraft entsteht, sorgt dafür, daß die Haut unter den Elektroden
kräftig durchblutet wird. Dadurch sinkt der Hautwiderstand, steigt die Effektivität des
stimulierenden Stromes.
• Elektrodengröße in Abhängigkeit vom zu behan-delnden Körperteil auswählen
• Schwämmchen anfeuchten. Schwämmchen etwas ausdrücken und in die Vakuumelektroden
einführen
• Zum leichteren Anlegen der Elektroden kontinuierliches Vakuum wählen
• Stellen Sie die Vakuumelektroden auf eine glatte Oberfläche (z.B. ein Tisch)
• Drehen Sie die Vakuumintensität ein wenig auf, sodaß in den Elektroden ein Vakuum entsteht
• Plazieren Sie jetzt die Elektroden eine nach der anderen von der glatten Oberfläche auf dem
Körper des Patienten
• Stellen Sie die Vakuumintensität auf dem ge-wünschten Wert ein
• Befolgen Sie die Bedienungsanleitung in Kapitel 10, wie Sie die Einstellungen anpassen und die
Behandlung starten und beenden können
• Falls erforderlich, Saugleistung nachregeln. Es genügt bereits eine geringe Saugleistung
• Falls erforderlich, wählen Sie gepulstes Vakuum
Halten Sie die Schwammpads während der Behandlung gut angefeuchtet (bei leichtem Druck
tropfnass). Befeuchten Sie diese erneut, wenn die Behandlung länger als 10 Minuten dauert.
Reinigen Sie die Schwammpads nach Gebrauch wie unter „Reinigung und Desinfektion“
beschrieben.
• Wenn Sie nur einen Vakuumkanal verwenden, schließen Sie den anderen Kanal mit einem der
nicht verwendeten Vakuumkabel.

Seite 44 von 54 DE109-1634750-40 IFU
Continuous or pulsed vacuum Konstante oder pulsierende Saugwirkung
Sobald bei konstanter Saugwirkung das vorgewählte Vakuum erreicht ist, schaltet sich die Pumpe
selbsttätig ab. Deshalb arbeitet das Vacotron S fast ge-räuschlos. Ein Regelsystem sorgt für ein
konstantes Vakuum. Die Pumpe schaltet sich von Zeit zu Zeit kurz ein, um das Vakuum auf einem
konstanten Niveau zu halten.
Bei pulsierender Saugwirkung wird die Pumpe abwechselnd ein- und ausgeschaltet. Der
Impulsrhythmus, der eine massierende Saugwirkung zur Folge hat, läßt sich konstante oder
pulsierende (zwei Möglichkeiten) einstellen. Die pulsierende Saug-wirkung eignet sich besonders
gut für die Behandlung von Patienten mit hoher Sensibilität, da dadurch das vom Stromfluß
erzeugte Gefühl mehr oder weniger stark überlagert wird.
Stromdichte
In der Norm IEC 60601-2-10 – Besondere Festlegungen für die Sicherheit einschließlich der
wesentlichen Leistungsmerkmale von Geräten zur Stimulation von Nerven und Muskeln – wird
empfohlen, eine Stromdichte von 2 mA r.m.s./cm2 nicht zu überschreiten, da sonst Hautreizungen
oder Verätzungen auftreten können.
Um die maximale empfohlene Stromamplitude in mA für Interferenzstrom zu errechnen,
multiplizieren Sie die Elektrodenoberfläche in cm² mit zwei. Für alle anderen Stromimpulsformen
darf der Stimulator- Output- Strom niemals 50 mA r.m.s überschreiten. Dies bedeutet, dass die
Stromdichte bei einer Elektrodenoberfläche von 25 cm² niemals 2 mA r.m.s. / cm² überschreiten
kann. Als Daumenregel für kleinere Elektroden, wie die 3.2 mm selbsthaftenden, sollte die am
Stimulator für eine gegebene Stromimpulsform verfügbare maximale Stromeinstellung proportional
vermindert werden.
Für eine präzise Berechnung des r.m.s. – Wertes einer Strom-Impulsform kann die folgende Formel
verwendet werden:
Achten Sie darauf, dass die Elektroden sorgfältig platziert werden sollten, wobei ein guter
elektrischer Kontakt über die gesamte Elektrodenfläche gewährleistet sein muss, und dass die
Verwendung kleiner Elektroden in Kombination mit hohen Intensitäten Hautreizungen oder
Verätzungen verursachen kann.
Reaktionen beim Anbringen und Lösen der Elektroden
Die Charakteristika bei der Abgabe von Konstantstrom (CC) können zu unangenehmen Reaktionen
beim Anbringen und Lösen der Elektroden führen, wenn die Elektroden nicht stabil platziert sind
oder den Hautkontakt verlieren. Achten Sie darauf, dass die Stromamplitude auf 0 mA eingestellt
ist, wenn Sie die Elektroden anbringen oder entfernen.

Seite 45 von 54 DE109-1634750-40 IFU
12 Wartung und Fehlerbehebung
Reinigung und Desinfektion
Reinigen Sie das Gerät und sein Zubehör regelmäßig, um die hygienische Sicherheit
aufrechtzuerhalten.
Schalten Sie das Gerät immer aus und ziehen Sie den Netzstecker aus der Steckdose, bevor Sie
mit Reinigungsarbeiten beginnen.
Reinigungsmittel nicht direkt auf die Glasplatte sprühen.
Verwenden Sie keine Reinigungsmittel, die starke Alkalien, Laugen oder Säuren enthalten und
keine fluorid- oder ammoniakhaltigen Reiniger.
Sorgen Sie dafür, dass während der Reinigung und Desinfektion keine Flüssigkeiten in das Gerät
oder das Zubehör eindringen können!
Trocknen Sie sämtliche Anschlussbuchsen und Stecker, die feucht geworden sind, sorgfältig ab,
bevor Sie das Gerät wieder benutzen!
Mechanische Stöße und/oder Vibrationen während der Reinigung des Geräts sind unter allen
Umständen zu VERMEIDEN!
Lassen Sie das Gerät nicht fallen!
Gerät
Schalten Sie das Gerät zum Reinigen aus und ziehen Sie den Netzstecker
heraus. Reinigen Sie das Gerät mit einem feuchten Tuch. Verwenden Sie
keine Scheuermittel. Bei Bedarf kann eine kleine Menge eines milden
Haushaltswaschmittels verwendet werden.
Display
Das Display ist mit einer Antireflexfolie versehen, die mit besonderer Umsicht
gereinigt werden muss. Verwenden Sie zur Displayreinigung ein weiches und
trockenes Baumwolltuch oder ein Mikrofasertuch. Um Fingerabdrücke oder
Fett zu entfernen, verwenden Sie einen nicht scheuernden Glasreiniger. Geben
Sie eine kleine Menge Reinigungsmittel auf ein weiches Baumwolltuch und
reinigen Sie damit vorsichtig das Display.
Elektroden,
Elektrodenhalter,
Schwämme und
Zubehörteile
Zwischen den Anwendungen bei Patienten sollten die Gummielektroden mit
lauwarmem Wasser gereinigt werden. Verwenden Sie eine 70%ige
Alkohollösung, um die Elektroden zu desinfizieren oder hartnäckige
Schmutzflecken zu entfernen. Die Alkohollösung kann helle Flecken auf der
schwarzen Farbe hervorrufen, dies beeinträchtigt jedoch nicht die Funktion
der Elektroden.
Zwischen den Anwendungen bei Patienten sollten die Schwammpads unter
fließendem Leitungswasser gewaschen, gründlich abtropfen gelassen und
anschließend getrocknet werden. Beschädigte Schwammpads sollten ersetzt
werden.
Es wird empfohlen, eine ausreichende Menge an Schwämmen zur Verfügung
zu haben, damit sie vor der Wiederverwendung vollständig trocknen können.
Dadurch wird das Wachstum von Bakterien, die in dem Wasser vorhanden
sind, begrenzt.
Wenn die Elektroden nicht verwendet werden, sollten die Schwammpolster
entfernt werden. Dies erhöht die Lebensdauer der Gummielektroden. Wir
empfehlen Ihnen, einen zusätzlichen Satz Schwammpolster vorrätig zu halten.
Die blanke Masseelektrode kann mit einem feuchten Tuch gereinigt werden.
Verwenden Sie Seife und lauwarmes Wasser oder Alkohollösung.

Seite 46 von 54 DE109-1634750-40 IFU
Der Elektrodenhalter kann mit einem feuchten Tuch gereinigt werden.
Verwenden Sie lauwarmes Wasser und ein nicht scheuerndes, nicht invasives
Haushaltsreinigungsmittel oder eine Alkohollösung. Nicht in den Autoklaven
legen.
Patientenkabel
und DC-
Referenzkabel
Reinigen Sie das Patientenkabel mit einem feuchten Tuch. Verwenden Sie
lauwarmes Wasser und ein nicht scheuerndes Haushaltsreinigungsmittel.
Verwenden Sie keine alkoholische Lösung. Überprüfen Sie das Kabel
regelmäßig auf Beschädigungen und/oder mangelhaften elektrischen
Kontakt. Wir empfehlen, ein Ersatz-Patientenkabel vorrätig zu halten.
Vakuumelektroden
und Schwämme
Die Vakuumelektroden und Schwämme sollten mit lauwarmem Wasser
gereinigt werden. Wenn Schmutz zurückbleibt, ebenso wie zur Desinfektion,
kann eine 70%ige Alkohollösung verwendet werden.
Schwämme sollten regelmäßig ersetzt werden. Es wird empfohlen,
Schwämme und eine Ersatzelektrode auf Lager zu halten.
Durch Ablagerungen können auf den Metalloberflächen der Elektroden
Kalziumkrusten entstehen. Dies hat eine isolierende Wirkung. Um die
optimale Leitfähigkeit aufrechtzuerhalten, sollten diese Oberflächen
regelmäßig gereinigt und poliert werden.
Vakuumkabel
Reinigen Sie das Vakuumkabel mit einem feuchten Tuch. Verwenden Sie
keine Alkohollösung. Prüfen Sie das Kabel regelmäßig auf Schäden und/oder
schlechten elektrischen Kontakt. Wir raten Ihnen, ein Ersatzkabel vorrätig zu
halten.
Reinigen des
Wasserbehälters
und der Schläuche
• Trennen Sie die Saugnäpfe von den Vakuumkabeln.
• Stellen Sie einen mit Reinigungsflüssigkeit gefüllten Behälter (*) unter das
System.
• Entfermen Sie die Saugnäpfe von den Vakuumkabeln und legen Sie die
Peripherieenden der Kabel in den Behälen
• Gehen Sie zu „Systemeinstellungen“ und wählen Sie „Wasserbehälter
reinigen“.
• Der Wasserbehälter wird mit Reinigungsflüssigkeit gefüllt, bis der
Wasserbehälter voll ist.
• Leeren Sie den Wasserbehälter wie unter beschrieben (Wasserbehälter
voll).
(*)Die folgenden registrierten Produkte können zur Desinfektion des Wasserbehälters verwendet
werden:
BAKTONIL, BAKTOLAN zu 5%, CHINOSOL zu 1%, CHLORAMIN Lösung, DETTOL, ELMOCID Gamma
zu 2%, PERODIN, ZEPHIROL zu 5%.
Beachten Sie die Anwendungsinformationen des entsprechenden Herstellers.

Seite 47 von 54 DE109-1634750-40 IFU
Fehlermeldungen
Wenn das Gerät eingeschaltet wird, führt es zunächst einen Selbsttest durch. Wird sowohl während
des Selbsttests als auch während des normalen Betriebs ein Fehler festgestellt, erscheint ein Pop-
up-Bildschirm auf dem Display. Wenn der Fehler angezeigt wird, werden alle Ausgänge deaktiviert.
Schalten Sie in diesem Fall das Gerät aus und trennen Sie alle Zubehörteile ab. Warten Sie ca. 15
Sekunden und schalten Sie das Gerät wieder ein. Wenn der Fehler wieder auftritt, stellen Sie die
Verwendung des Geräts ein und wenden Sie sich an den Lieferanten.
Das Gerät muss abkühlen, bevor Sie fortfahren können
Die Temperatur des Gerätes ist zu hoch, um mit der Behandlung beginnen zu können. Entfernen Sie
das Gerät von eventuellen Wärmequellen (z. B. direktem Sonnenlicht) und lassen Sie es abkühlen.
Starten Sie das Gerät erneut, um fortzufahren.
Unzureichender oder kein Ausgangsstrom
• Überprüfen Sie das Patientenkabel auf Unterbrechungen oder schlechten Kontakt.
• Stellen Sie sicher, dass die Schwämme ausreichend befeuchtet sind.
• Reinigen Sie die Elektroden
• Auf schlechten Kontakt prüfen
• In Gebieten, in denen das Wasser weich ist, ist es möglich, dass das Wasser schlecht leitet, was
zu ungewöhnlich niedrigen Strömungen führt. In diesem Fall ist es möglich, eine Salzlösung zu
verwenden, um die Leitfähigkeit des Wassers zu verbessern.
Wasserbehälter voll
Der Wasserabscheidungstank des Vacotron ist voll. Setzen Sie die Behandlung mit den
Standardelektroden fort oder leeren Sie den Tank wie folgt:
• Stellen Sie den Netzschalter [17] auf Aus (0).
• Trennen Sie den Schlauch vom oberen Schlauchnippel [21] und leeren Sie den Behälter.
• Bringen Sie den Schlauch wieder am Schlauchnippel an.
• Stellen Sie den Netzschalter [17] auf Ein (1).
Fehlerbehebung
Das Gerät sollte nicht verwendet werden, wenn mechanische Beschädigungen festgestellt
werden. Dazu gehört auch eine beschädigte Kabelisolierung.
Falls eine Fehlermeldung oder eine Warnmeldung erscheint, stellten Sie unmittelbar den
Betrieb des Geräts ein. Schalten Sie das Gerät aus und danach wieder ein. Wenn das Problem
bestehen bleibt, wenden Sie sich an den Lieferanten oder an Enraf-Nonius B.V.
Fehlermeldungen und Warnmeldungen weisen auf ein internes Problem im Gerät hin. In
diesem Fall muss das Gerät von einem von Enraf-Nonius B.V. zertifizierten Servicetechniker
geprüft werden, bevor das System wieder in Betrieb genommen oder benutzt werden darf.
Die Verwendung eines Geräts trotz Fehler- oder Warnmeldung kann Verletzungen des
Patienten oder des Bedieners oder Beschädigungen des Systems zur Folge haben.
Im Falle einer Fehlermeldung oder anderer offensichtlicher Defekte ziehen Sie sofort den
Netzstecker und benachrichtigen Sie einen zertifizierten Servicetechniker.
Bei Eindringen von Flüssigkeiten ziehen Sie den Netzstecker und lassen Sie das Gerät von
einer autorisierten Person überprüfen.

Seite 48 von 54 DE109-1634750-40 IFU
Vakuumleck
Es ist wahrscheinlich ein Leck im Vakuumsystem. Vor diesem Fehler tritt normalerweise eine ständig
laufende Pumpe auf, die versucht, das eingestellte Vakuum zu erreichen. Um das System zu
schützen, wird die Pumpe nach einer gewissen Zeit automatisch gestoppt. Überprüfen Sie die
Vakuumkabel und Elektroden, stellen Sie das Vakuum wieder auf null und versuchen Sie es erneut.
Wenn der Fehler weiterhin besteht, verwenden Sie das Gerät nicht mehr und wenden Sie sich an
Ihren Lieferanten.
Es wird außerdem empfohlen, ein Protokoll über die Service-Historie zu führen. In manchen Ländern
ist dies vorgeschrieben.
Auf Anfrage kann eine Serviceanleitung zur Verfügung gestellt werden, die eine Ersatzteilliste,
Beschreibungen, Kalibrierungsanweisungen und andere Informationen enthält, die dem
qualifizierten technischen Personal des Benutzers helfen, die Teile des Geräts zu reparieren, die vom
Hersteller als reparabel eingestuft wurden.
Erwartete Lebensdauer
Sofern die jährliche Wartung von einem qualifizierten Servicetechniker gemäß Serviceanleitung
durchgeführt wird, bleibt das Gerät für den vorgesehenen Einsatz geeignet.
Der Servicetechniker entscheidet, ob das Gerät für den spezifikationsgemäßen Einsatz geeignet ist.
Ende der Lebensdauer
Endomed 182 enthält Materialien, die recycelt werden können und/oder schädlich für die Umwelt
sind.
Technische Wartung
Öffnen der Ausrüstung durch nicht autorisierte Dienstleister ist nicht gestattet und beendet
jeglichen Garantieanspruch.
Der Hersteller haftet nicht für die Ergebnisse der Wartungsarbeiten oder Reparaturen, die
durch unbefugte Personen ausgeführt wurden!
Nur von Enraf-Nonius autorisierte Servicetechniker dürfen dieses Gerät gemäß den
Serviceinformationen warten oder modifizieren.
Das Gerät darf nicht gewartet werden, wenn es in Betrieb oder mit einem Patienten
verbunden ist.
Es wird empfohlen, Endomed 182 jährlich von autorisiertem Personal von Enraf-Nonius oder
von dessen autorisiertem Fachhändler überprüfen zu lassen.
Bitte stellen Sie sicher, dass Sie die lokalen Vorschriften in Bezug auf die Entsorgung des
Geräts und Zubehörs genau kennen.

Seite 49 von 54 DE109-1634750-40 IFU
13 Spezifikation
Technische Daten
Elektrische Daten
Netzspannung
100 - 240 Volt
Frequenz
50/60 Hz
Max. Leistungsaufnahme
50 VA
Abmessungen (Breite x Länge x Höhe)
Endomed 182 Typ 1
14.5 x 17 x 9 cm
Endomed 182 Typ 2
14 x 16 x 14 cm
Endomed 182 Typ 3
14 x 22,5 x 17,5 cm
Diese Werte stellen die Abmessungen der Gehäuse
ohne Kommunikationskabel, Elektroden oder
Schläuche dar.
Gewicht
Endomed 182 Typ 1
710 Gramm
Endomed 182 Typ 2
1460 Gramm
Endomed 182 Typ 3
2750 Gramm
Diese Werte stellen das Gewicht der Gehäuse ohne
Elektroden und Netzkabel dar.
Spezifikationen Typ 1
Kanäle
1
Ausgabe
Konstanter Strom
Gleichstrom
Polarität
Negativ
Intensität
0 – 15 mA
Behandlungszeit
0 – 300 Sekunden
Spezifikationen Typ 2 und 3
Kanäle
2
Ausgabe
Konstanter Strom
Intensität
0 -100 mA
Timer
0 – 60 min (in Schritten von 1 min)
2-polig Interferenz
Trägerwelle
4 kHz
AMF-Frequenz
1 – 200 Hz
Modulationsfrequenz
0 – 180 Hz
Modulationsprogramm
1-1, 6-6, 1-30 Sekunden
4-polig Interferenz und isoplanarer Vektor
Trägerwelle
4 kHz
AMF-Frequenz
1 – 200 Hz
Modulationsfrequenz
0 – 180 Hz
Modulationsprogramm
1-1, 6-6, 1-30 Sekunden

Seite 50 von 54 DE109-1634750-40 IFU
Asymmetrischer biphasischer Impulsstrom (TENS)
Pulsbreite
150 μs
Frequenz
1 – 200 Hz
Modulationsfrequenz
0 – 180 Hz
Modulationsprogramm
1-1, 6-6, 1-30 Sekunden
Burst-Frequenz
1-2-4 Hz
Technische Änderungen vorbehalten
Sicherheits- und Leistungsstandards
Klassifikation von Medizinprodukten
IIa; Regel 9 Anhang IX der 93/42/EWG
Dieses Gerät entspricht allen Anforderungen der
Richtlinie über Medizinprodukte (93/42/EWG).
Sicherheitsklasse gemäß IEC 60601-1
Elektrische Sicherheit der Klasse I
Arbeitsweise
Kontinuierlich
Anwendungsteile
Anwendungsteil vom Typ BF für die Elektrotherapie.
Wesentliche Leistung
Die wesentlichen Leistungsmerkmale basieren auf der Norm 60601-2-10, in der der maximale
Ausgang des Stroms und der Impulsenergie angegeben ist. Angesichts der unterschiedlichen
Therapieformen beinhalten die wesentlichen Leistungsmerkmale fünf Anforderungen:
1) Der maximale TENS-Effektivstrom darf 50 mA nicht übersteigen.
2) Der maximale Interferenzstrom-Effektivwert darf 100 mA nicht übersteigen.
3) Die maximale TENS-Impulsenergie darf 300 mJ nicht übersteigen.
4) Die maximale Interferenz-Impulsenergie darf 300 mJ nicht übersteigen.
5) Der maximale Gleichstrom-Effektivwert darf 80 mA nicht übersteigen.
Die Leistungsabgabe bei der Elektrotherapie darf nicht mehr als 20 % von dem eingestellten Wert
abweichen.
Da das Gerät nicht lebenserhaltend ist, ist ein Ausfall in einen sicheren Zustand (d. h. ohne
Leistungsabgabe), der einen Neustart durch den Bediener erfordert, zulässig.
Umgebungsbedingungen
Umgebungsbedingungen für Transport und Lagerung
Umgebungstemperatur:
–20° bis +70° C
Relative Luftfeuchtigkeit:
10 bis 90% (nicht-kondensierend)
Luftdruck:
500 bis 1060 hPa
Umgebungsbedingungen bei normaler Verwendung
Umgebungstemperatur:
10° bis 40° C
Relative Luftfeuchtigkeit:
10 bis 90 % (nicht-kondensierend)
Luftdruck:
800 bis 1060 hPa

Seite 51 von 54 DE109-1634750-40 IFU
Angaben zur EMV
Medizinische elektrische Geräte wie Endomed 182 unterliegen speziellen Vorsichtsmaßnahmen
hinsichtlich der elektromagnetischen Verträglichkeit (EMV) und müssen in Übereinstimmung
mit den EMV-Empfehlungen in der Gebrauchsanweisung und den Begleitdokumenten
installiert und in Betrieb genommen werden.
Die Verwendung dieses Geräts neben oder gestapelt auf anderen Geräten sollte vermieden
werden, da dies zu fehlerhaftem Betrieb führen könnte. Falls eine solche Verwendung
erforderlich ist, sollten dieses Gerät sowie die anderen Geräte beobachtet werden, um
sicherzustellen, dass sie normal funktionieren.
Die Verwendung von Zubehör, Transducern und Kabeln, die nicht aufgeführt oder nicht vom
Hersteller des Geräts zur Verfügung gestellt wurden, kann zu erhöhten elektromagnetischen
Emissionen oder zu einer reduzierten elektromagnetischen Immunität dieses Geräts und zu
einem unsachgemäßen Betrieb führen.
Tragbare HF-Kommunikationsgeräte (einschließlich Peripheriegeräten wie Antennenkabel und
externe Antennen) sollten nicht näher als 30 cm an einem Teil des Endomed 182 verwendet
werden, einschließlich der vom Hersteller angegebenen Kabel. Andernfalls kann es zu
Leistungseinbußen bei dem Gerät kommen.
Endomed 182 darf nur mit dem Original-Netzkabel betrieben werden, das in der Liste des
Lieferumfangs angegeben ist. Der Betrieb des Geräts mit einem anderen Netzkabel kann zu
stärkeren Emissionen oder einer geringeren Immunität des Geräts gegenüber Interferenzen
führen.
Endomed 182 ist gemäß CISPR 11 als Gerät der Gruppe 1, Klasse B eingestuft.
Endomed 182 ist für die Verwendung in einer professionellen Gesundheitseinrichtung geeignet.
Das Gerät verwendet HF-Energie ausschließlich für seine internen Funktionen. Daher sind seine HF-
Emissionen sehr gering und es ist unwahrscheinlich, dass benachbarte elektronische Geräte gestört
werden.
Endomed 182 wurde von einem akkreditierten Labor nach der Norm 60601-1-2 geprüft und als
konform mit jeder Emissions- und Störfestigkeitsnorm bzw. -prüfung befunden.

Seite 52 von 54 DE109-1634750-40 IFU
14 Kontakt
Für Unterstützung besuchen Sie bitte unsere Website http://www.enraf-nonius.com
Die neueste Version dieser Gebrauchsanweisung (in elektronischer oder ausgedruckter Form)
erhalten Sie kostenfrei auf unserer Website www.enraf-nonius.com oder indem Sie den für Sie
zuständigen Distributor kontaktieren oder unter der folgenden Telefonnummer: +31-(0)10-
2030600. Die Gebrauchsanweisung wird Ihnen (kostenfrei) innerhalb von 7 (sieben) Kalendertagen
zugesendet.
15 Produkthaftung
Zahlreiche Länder unterliegen den Bestimmungen eines Produkthaftungsgesetzes. Dieses
Produkthaftungsgesetz besagt unter anderem, dass der Hersteller nach Ablauf von 10 Jahren nach
der Vermarktung eines Produkts für eventuelle Produktfehler keine Haftung mehr trägt.
Bis zum maximal rechtlich zulässigen Umfang übernimmt Enraf-Nonius oder dessen Zulieferer bzw.
Wiederverkäufer in keinem Fall Haftung für mittelbare, Sonder-, Neben- oder Folgeschäden, die aus
der Verwendung bzw. der Nichtverwendbarkeit des Produkts entstehen, einschließlich, jedoch nicht
beschränkt auf Schäden durch Verlust des Geschäftsansehens, Arbeitsausfälle,
Produktivitätsverluste, Computerversagen oder -fehlfunktionen sowie jegliche anderen
kommerziellen Schäden oder Verluste, selbst dann nicht, wenn bereits Informationen über die
Möglichkeit derartiger Schäden vorliegen und unabhängig von der Rechtstheorie (Vertragsrecht,
Schadenersatzrecht oder sonstige Rechte), auf der ein Haftungsanspruch beruht. Die Gesamthöhe
der Haftung von Enraf-Nonius aus den Bestimmungen dieser Vereinbarung überschreitet auf
keinen Fall die Summe aller Entgelte, die für dieses Produkt gezahlt wurden sowie der Entgelte für
Produktunterstützung, die Enraf-Nonius im Rahmen einer anderen Unterstützungsvereinbarung
möglicherweise erhalten hat, mit Ausnahme von Todesfällen oder Personenschäden als Folge eines
fahrlässigen Verhaltens auf Seiten von Enraf-Nonius, in dem Ausmaß, in dem eine
Haftungsbeschränkung in derartigen Fällen durch geltendes Recht untersagt ist.
Die Gegenpartei (Benutzer des Produkts bzw. dessen Vertreter) stellt Enraf-Nonius gegenüber allen
Ansprüchen Dritter, ungeachtet ihrer Art oder Beziehung zur Gegenpartei, frei.

Seite 53 von 54 DE109-1634750-40 IFU

DE109-1634750-40
Copyright:
Enraf-Nonius B.V.
Vareseweg 127 | 3047 AT | Rotterdam | Niederlande
Tel: +31 (0)10-20 30 600 | [email protected]

Page 1 de 52 FR109-1634750-40 IFU
Endomed 182
FR109-1634750-40 IFU
21 Septembre, 2020
Manuel d’utilisation

Page 2 de 52 FR109-1634750-40 IFU
Sommaire
1 Introduction ...................................................................................................................................................... 3
2 Symboles ............................................................................................................................................................ 7
3 Composants de l'appareil ............................................................................................................................ 9
4 Contenu des emballages ........................................................................................................................... 13
5 Installation ...................................................................................................................................................... 15
6 Usage et utilisateur prévus ....................................................................................................................... 16
7 Indications ...................................................................................................................................................... 17
8 Contre-indications ....................................................................................................................................... 18
9 Consignes de sécurité ................................................................................................................................ 20
10 Utilisation ........................................................................................................................................................ 23
11 Informations d’application ....................................................................................................................... 37
12 Maintenance et dépannage ..................................................................................................................... 44
13 Charactéristiques .......................................................................................................................................... 48
14 Contact ............................................................................................................................................................. 51
15 Responsabilité du fait du produit .......................................................................................................... 51

Page 3 de 52 FR109-1634750-40 IFU
1 Introduction
Préface
Nous sommes heureux que vous ayez acheté un Endomed 182.
L'Endomed 182, conçu et fabriqué par Enraf-Nonius B.V., donne une nouvelle dimension à
l'électrothérapie grâce à une technologie logicielle de pointe. Il en résulte un appareil
extraordinairement polyvalent qui s'utilise facilement.
Ce manuel a été rédigé à l'intention des propriétaires et des opérateurs de l'Endomed 182. Afin de
maximiser l'utilisation, l'efficacité et la durée de vie de votre appareil, veuillez lire attentivement ce
manuel et vous familiariser avec les commandes ainsi que les accessoires avant d'utiliser l'appareil.
Description de l'appareil
L'Endomed 182 est un électrostimulateur alimenté sur secteur, équipé d'un écran tactile couleur.
L'interface utilisateur graphique permet un confort d'utilisation maximal.
Trois modèles d'Endomed 182 sont disponibles :
L'Endomed 182 Type 1 est un électrostimulateur monocanal alimenté sur secteur pour l'application
de l'électrolyse percutanée (EP) au moyen d'un courant continu (CC) de faible intensité.
Dans l'EP, le courant continu (également appelé courant galvanique) est appliqué à l'aide d'une
aiguille qui est placée dans le porte-aiguille d'une pièce à main (l'« applicateur » ou cathode).
L'électrode de retour (ou anode) est une électrode à main (tenue par le patient) ou une autre aiguille,
selon le traitement à effectuer.
Versions Endomed 182
Nom :
Endomed 182 Type 1
Endomed 182 Type 2
Endomed 182 Type 3
Numéro d'article :
1634903
1634901
1634902
Numéro d'article
unité de base :
1634910
1634900
1634900
Forme du courant :
Courant continu
TENS
• courant continu biphasé pulsé
(mode TENS conventionnel)
• trains de courant biphasé
pulsé (mode TENS Salves)
Courant interférentiel
• interférentiel bipolaire
• interférentiel quadripolaire
• interférentiel quadripolaire
avec vecteur isoplanaire
TENS
• courant continu biphasé pulsé
(mode TENS conventionnel)
• trains de courant biphasé
pulsé (mode TENS Salves)
Courant interférentiel
• interférentiel bipolaire
• interférentiel quadripolaire
• interférentiel quadripolaire
avec vecteur isoplanaire
Vide
Canaux :
1
2
2
Protocoles de
traitement
préprogrammés :
-
16
16

Page 4 de 52 FR109-1634750-40 IFU
Le porte-aiguille de l'applicateur (pièce à main) permet de fixer des aiguilles d'acupuncture (stériles,
à usage unique et jetables) de différentes longueurs et de différents diamètres, nécessaires pour
assurer un placement correct dans différentes zones (selon le trouble à traiter).
La pièce à main est équipée d'une touche Marche/Arrêt permettant de démarrer ou d'interrompre
manuellement le flux de courant.
L'appareil délivre un courant galvanique continu avec une puissance maximale de 15 mA.
L'interface utilisateur graphique propose les paramètres de traitement suivants : niveau de sortie du
courant (mA), temps défini pour l'application, courant réel délivré (mC).
L'utilisateur peut régler et ajuster le niveau de sortie du courant (mA) et le temps d'application, en
fonction du type de traitement.
L'appareil ne propose aucun protocole clinique prédéfini, mais les paramètres de traitement peuvent
être réglés et sauvegardés en tant que favoris (paramètres personnalisés) comme référence pour de
futures séances de thérapie.
L'appareil est une unité compacte qui est fournie avec les accessoires suivants : câbles secteur et de
raccordement, pièce à main (applicateur), électrode de retour, pédale (en option) et documentation
du produit. Les consommables tels que les aiguilles (d'acupuncture) jetables ne sont pas livrés avec
le produit.
Enraf-Nonius B.V. ne fournit pas d'électrodes percutanées ou d'aiguilles d'acupuncture jetables.
Les Endomed 182 Type 2 et 3 comprennent 16 protocoles cliniques prédéfinis pour la TENS et les
courants interférentiels. Des paramètres de traitement individuels peuvent également être réglés
manuellement et ajustés par l'opérateur. Tous les paramètres de traitement peuvent être réglés et
sauvegardés en tant que favoris (paramètres personnalisés) comme référence pour de futures
séances de thérapie.
L'Endomed 182 Type 3 est une configuration empilée qui consiste en un module d'aspiration à vide
séparé et un électrostimulateur Endomed 182 Type 2. Le module à vide est placé sous le stimulateur
et connecté à celui-ci. Le but du module est de générer un vide qui permet au thérapeute de fixer
rapidement et (plus) facilement les électrodes de stimulation sur le patient. La fixation est réalisée
au moyen de ventouses. Les ventouses ont des surfaces de stimulation intégrées qui transfèrent
l'électrostimulation via des éponges humidifiées vers le tissu cible.
Pour les Endomed 182 Type 2 et 3, la stimulation électrique peut donc être appliquée sur la peau
par l'intermédiaire d'électrodes de surface : des électrodes flexibles en caoutchouc, des électrodes
autocollantes ou des électrodes à vide (Type 3 uniquement), dans le but de stimuler des types
spécifiques de fibres nerveuses. Enraf-Nonius propose différents types et tailles d'électrodes (de
l'électrode punctiforme d'une surface de 0,3 cm2 aux électrodes d'une surface de 96 cm2) pour
s'adapter à la taille de la zone traitée ou à l'objectif de traitement prévu.

Page 5 de 52 FR109-1634750-40 IFU
Description forme d’onde de courant
TENS
Le courant d’impulsions biphasiques asymétriques est souvent utilisé dans les applications de TENS
(Stimulation Electrique Nerveuse Transcutanée). Durée de phase et fréquence des impulsions sont
variables. La forme et l’amplitude des phases positives et négatives ne sont pas identiques, mais il
s’agit cependant d’un courant à moyenne nulle car les quantités de courant de chaque phase sont
égales. La nature biphasée de l'impulsion signifie qu'il n'y a pas de composant CC net (zéro CC net),
minimisant ainsi toute réaction cutanée due à l'accumulation d'électrolytes sous les électrodes.
Pour prévenir l’accoutumance à la stimulation ou
pour améliorer la tolérance du patient, la
fréquence des impulsions peut varier par
l’intermédiaire de la modulation de fréquence.
Forme d'onde biphasique asymétrique TENS
TENS Salves
TENS Salves est appliquée si la TENS conventionnelle s'avère inefficace, et est particulièrement
adaptée au traitement des régions douloureuses plus profondes et des cas de douleurs chroniques.
TENS Salves utilise une durée de phase relativement importante (150-200 μs), une basse fréquence
de rafale (1-5 Hz) et une haute fréquence.
Des contractions fortes et visibles doivent se produire dans les muscles dont l'innervation
correspond à celle de la région douloureuse.
L'effet anti-douleur n'apparaît généralement pas avant vingt à trente minutes, contrairement à
l'effet de la TENS conventionnelle, qui se produit habituellement assez rapidement. Toutefois, l'effet
dure beaucoup plus longtemps que celui de la TENS conventionnelle après la fin de la stimulation.
L'effet anti-douleur de TENS Salves est dû à la libération d'endorphines aux niveaux spinal et
supraspinal.
Si la TENS conventionnelle ou Salves n'apportent aucun soulagement ou ne procurent qu'un
soulagement insuffisant, la modulation de fréquence peut être utilisée. La modulation de fréquence
peut également empêcher l'accommodation.
Courant interférentiel
Avec le courant interférentiel type, une fréquence porteuse de moyenne fréquence est utilisée pour
faciliter la pénétration de la basse fréquence (battement) de stimulation. L’impédance relativement
basse de la peau à la fréquence porteuse contribue au confort du patient qui est souvent reconnu
avec ce type de courant. Tous les courant interférentiels sont des courants alternatifs sans aucune
composante résiduelle galvanique. Les différentes variations connues du courant interférentiel sont
disponibles dans les Endomed 182 Type 2 et 3 : bipolaire, quadripolaire et vecteur isoplanaire
quadripolaire.
La méthode bipolaire
Dans cette méthode, deux électrodes sont utilisées et
la superposition des deux courants alternatifs a lieu
dans l'appareil. Le courant sortant de l'équipement est
un courant alternatif entièrement modulé. Dans la
méthode bipolaire, la profondeur de modulation est
toujours de 100%.
Thérapie interférentielle bipolaire

Page 6 de 52 FR109-1634750-40 IFU
La méthode quadripolaire (Interférentielle
classique)
On utilise quatre électrodes et deux courants alternatifs
sont générés. Un canal délivre une fréquence porteuse
fixe alors que l’autre canal délivre une fréquence
déterminée par le choix des fréquences de battement
et de modulation. L’interférence se réalise à
l’intersection des deux courants dans les tissus. La
profondeur de modulation (qui détermine l’amplitude
du courant de la stimulation) dépend de la direction
des courants et peut varier de 0 à 100%. La profondeur
de modulation de 100% se manifeste seulement aux
diagonales (et par conséquent à l’intersection des deux
courants). C’est naturellement une situation théorique
basée sur l’hypothèse que les tissus sont homogènes.
En réalité, les tissus sont hétérogènes, aussi il est
nécessaire de répartir le courant entre les deux canaux
pour obtenir la profondeur de modulation de 100%. La
répartition du courant peut également être employée
pour compenser les différences de sensation sous les
quatre électrodes.
Dans la méthode quadripolaire, la
profondeur de modulation est seulement
de 100% aux diagonales.
La méthode quadripolaire avec vecteur isoplanaire
Avec le Vecteur isoplanaire, la surface totale entre les 4
électrodes est stimulée de façon optimale. Le
positionnement des électrodes peut être fait de
manière simple et rapide. La profondeur de modulation
est de 100% partout.
Interférentiel isoplanaire peut être utilisé pour le
traitement de problèmes qui sont situés dans une
grande zone et qui sont très difficiles à localiser.
Interférentiel isoplanaire est également utilisé comme
un prétraitement léger. Après cette application, le
traitement est poursuivi en se concentrant sur une
zone plus petite et plus locale.
Vecteur isoplanaire
Courant Continu
Un courant continu (CC) ou courant galvanique est un courant continu qui est utilisé en médecine
pour un certain nombre de buts thérapeutiques. Le courant continu désigne le flux continu de
charge électrique via un conducteur de courant entre deux points (électrodes) ayant des potentiels
(polarité) différents, qui ne change pas de direction au fil du temps. Contrairement aux courants
alternatifs, les charges électriques circulent toujours dans le même sens.

Page 7 de 52 FR109-1634750-40 IFU
2 Symboles
Symbole utilisé
Description
Suivez les instructions du manuel d'utilisation.
Il est important de lire, de comprendre et de respecter les instructions
préalables et le mode d’emploi.
Interdiction générale
Ce signe est utilisé pour indiquer que « vous NE DEVEZ PAS »
Avertissement ou attention:
Indique une situation dangereusse qui, si elle n’est pas évitée, peut avoir pour
conséquence:
a. Des blessures graves ou le décès de patient (ou)
b. Des blessures légères ou modérées du patient (ou)
c. Des dommages à l’équipment
Action générale obligatoire.
Les actions obligatoires indiquent qu'il faut faire quelque chose.
Pièce appliquée de type BF conforme aux exigences spécifiées pour fournir un
degré de protection contre les chocs électriques plus élevé que celui fourni par
les pièces appliquées de type B.
Limites de température.
Indique la plage de température acceptable.
Limites d’humidité.
Indique la plage acceptable d’humidité relative.
Limites de pression atmosphérique.
Indique la plage de pression atmosphérique à laquelle l’appareil peut être
exposé en toute sécurité.
Déchets électriques pouvant être recyclés.
Indique que les composants électriques et électroniques de l’appareil peuvent
être recyclés et doivent être jetés séparément.
Gardez l’appareil au sec.
Nom du fabricant, adresse et date de fabrication.
Numéro de référence ou numéro de pièce
Numéro de série.
Indique le numéro de série du fabricant afin d’identifier un dispositif médical
précis.

Page 8 de 52 FR109-1634750-40 IFU
Courant alternatif
Connexion électrothérapie câble électrode.
Connexions câbles pour électrothérapie sous vide.
« allumé » (alimentation)
« éteint » (alimentation)
Le sigle CE et le nombre qui l’accompagne indiquent la conformité avec la
Directive du Conseil de l’Union Européenne relative aux dispositifs médicaux et
que cet appareil est sous la surveillance directe de l’organisme notifié.

Page 9 de 52 FR109-1634750-40 IFU
3 Composants de l'appareil
Endomed 182 Type 1
Endomed 182 Type 2
7
8
1
9
1
2
1
3
1
1
4
1
6
1
5
1
10
11

Page 10 de 52 FR109-1634750-40 IFU
Endomed 182 Type 3
12
13
16
15
14
17
18
19
21
20

Page 11 de 52 FR109-1634750-40 IFU
Description des pièces
Numéro
de la pièce
Description
Fonction
[1]
Écran LCD tactile
Écran TFT couleur tactile 4,3’’.
Interface utilisateur qui permet à l'opérateur de
commander l'appareil et de modifier les
paramètres des protocoles de traitement.
[2]
Connexion Porte-électrode
Connexion pour Porte-électrode
[3]
Connexion Électrode de masse
vierge
Connexion pour le Câble de référence CC qui se
connecte à l'électrode de masse vierge
[4]
Électrode de masse vierge
Électrode de référence
[5]
Câble de référence CC
Câble de connexion de l'électrode de retour
[6]
Porte-électrode
Pièce à main pour porte-aiguille
[7]
Connexion A
Connexion pour le Module de Vide (Endomed 182
Type 3 / Interrupteur au pied (Endomed 182 Type
1)
[8]
Connexion B
Connexion pour le Module Courant
[9]
Module Courant
Module Courant avec connexion pour les
électrodes adhésives et en caoutchouc.
[10]
Connexion 1 Module Courant
Canal de connexion 1 pour le câble patient pour les
électrodes adhésives ou en caoutchouc sur le
Module de Courant Endomed 182.
[11]
Connexion 2 Module Courant
Canal de connexion 2 pour le câble patient pour les
électrodes adhésives ou en caoutchouc sur le
Module de Courant Endomed 182.
[12]
Support d'électrode sous vide
Support pour électrode sous vide
[13]
Module de Vide
Module de Vide intégré à Endomed 182 avec des
connexions pour des électrodes adhésives ou en
caoutchouc et des électrodes à vide.
[14]
Câbles d'électrodes du Module
de Vide
Les câbles des électrodes du Module de Vide
doivent être connectés à la connexion du Module
Courant [7] et [8] pour le bon fonctionnement des
connexions du Module de Vide.
[15]
Connexions supérieures
Module de Vide
Canal de connexion 1 et 2 pour le câble patient
pour les électrodes adhésives ou en caoutchouc sur
le Module de Vide.
[16]
Connexions inférieures Module
de Vide
Connexions canal 1 et 2 pour le tuyau de plomb de
vide pour les électrodes de vide sur le Module de
Vide.
[17]
Interrupteur secteur
Pour allumer et éteindre l’appareil.
Quand arrêter l'affichage reste évident pendant
quelques secondes (méthode à énergie réduite).
[18]
Étiquette de référence
Fournit des informations sur l'appareil, telles que le
type et le numéro de série
[19]
Connecteur pour câble
d'alimentation
Connectez le câble d'alimentation fourni ici pour
alimenter l'appareil.
[20]
Sortie d'air
Sortie d'air pour le Module de vide.

Page 12 de 52 FR109-1634750-40 IFU
Description des pièces
Numéro
de la pièce
Description
Fonction
[21]
Raccordement pour réservoir
d'eau
Cette connexion sert à relier le réservoir d'eau.
Aucun vide ne peut être créé si le réservoir d'eau
n'est pas raccordé. Le réservoir d'eau assure que
l'excès d'eau des éponges est collecté et ne peut
pas être expulsé par la pompe. Le réservoir doit
être vidé quotidiennement. Veuillez vous référer à
la section sur l'entretien.

Page 13 de 52 FR109-1634750-40 IFU
4 Contenu des emballages
Appareil
Le contenu de l'ensemble dépend du modèle commandé. Les modèles suivants sont connus :
Numéro
d'article
Description
1634903
Endomed 182 Type 1
1634901
Endomed 182 Type 2
1634902
Endomed 182 Type 3 (comprend un Module de Vide intégré)
Accessoires standard Endomed 182 Type 1
1634750
CD-ROM avec manuel d'utilisation (PDF sur CD-ROM)
1634751
Brochure d’information
3444357
Câble secteur 250V/2,5A, 2,5 mètres noir
3444080
Porte-électrode
3444582
Électrode de masse vierge
3444677
Câble de référence CC
Accessoires standard Endomed 182 Type 2 et Endomed 182 Type 3
1634750
CD-ROM avec manuel d'utilisation (PDF sur CD-ROM)
1634751
Brochure d’information
3444357
Câble secteur 250V/2,5A, 2,5 mètres noir
3444021
Sangle de fixation 250 x 3 cm
3444020
Sangle de fixation 100 x 3 cm
3444129
(2x) Electrodes caoutchouc 6x8 cm, 2 mm cheville, jeu de 2 pc.
1460266
Eponges pour électrodes caoutchouc 6x8 cm, jeu de 4 pc.
3444211
(2x) Câble patient 2 mm fiche-noir, avec des clips colorés
Accessoires standard supplémentaires Endomed 182 Type 3
3444503
(2x) Electrodes sous vide Ø 60 mm, jeu de 2 pc.
3444505
Eponges Ø 65 mm, jeu de 4 pc. (pour électrodes sous vide Ø 60 mm)
3444507
(2x) Câble d'électrode pneumatique rouge
3444508
(2x) Câble d'électrode pneumatique noir
Accessoires optionnels Endomed 182 Type 1
1634810
Interrupteur au pied
Accessoires optionnels Endomed 182 Type 2 et Endomed 182 Type 3
Electrodes adhésives
3444056
EN-Trode Ø 3,2 cm, 2 mm cheville, 10x4 pc.
3444135
EN-Trode Ø 5,0 cm, 2 mm cheville, 10x4 pc.
3444057
EN-Trode 5x5 cm, 2 mm cheville, 10x4 pc.
3444058
EN-Trode 5x9 cm, 2 mm cheville, 10x4 pc.
3444222
Electrodes adhésives Ø 2,0 cm, 2 mm cheville, 10x8 pc.
Electrodes caoutchouc
3444128
Electrodes caoutchouc 4x6 cm, 2 mm cheville, 2 pc.
3444129
Electrodes caoutchouc 6x8 cm, 2 mm cheville , 2x2 pc.
3444130
Electrodes caoutchouc 8x12 cm, 2 mm cheville, 2 pc.
3444380
Electrode de silicium 5x5 cm

Page 14 de 52 FR109-1634750-40 IFU
Eponges pour électrodes caoutchouc
1460273
Eponges pour électrodes caoutchouc 4x6 cm, 4 pc.
1460266
Eponges pour électrodes caoutchouc 6x8 cm, 4 pc.
1460275
Eponges pour électrodes caoutchouc 8x12 cm, 4 pc.
Sangles de fixation
3444020
Sangle de fixation 100x3 cm
3444021
Sangle de fixation 250x3 cm
3444022
Sangle de fixation 100x5 cm
3444023
Sangle de fixation 250x5 cm
Électrode punctiforme
3444180
Electrode ponctiforme (modèle de stylo), Ø 5 mm, 2 mm femelle, y compris 10
bouchons en caoutchouc conducteurs
Adapteurs
2523523
Adaptateur pour 4 mm fiche à 2 mm cheville, noir
2523524
Adaptateur pour 2 mm fiche à4mm cheville, rouge
Câble patient
3444211
Câble patient 2 mm fiche-noir, avec des clips colorés
Accessoires optionnels supplémentaires Endomed 182 Type 3
Électrodes à vide
3444503
Electrodes sous vide Ø 60 mm, 2 pc.
3444504
Electrodes sous vide Ø 90 mm, 2 pc.
3444509
Electrodes sous vide Ø 30 mm, 2 pc
Eponges
3444505
Eponges Ø 65 mm, jeu de 4 (pour électrodes sous vide Ø 60 mm)
3444506
Eponges Ø 95 mm, jeu de 4 (pour électrodes sous vide Ø 90 mm)
3444516
Eponges Ø 30 mm, jeu de 4 (pour électrodes sous vide Ø 30 mm)
Câble d'électrode pneumatique
3444507
Câble d'électrode pneumatique noir, avec bouchons rouge
3444508
Câble d'électrode pneumatique noir, avec bouchons noir
Informations relatives à la commande
Pour les données de commande de l'Endomed 182, ainsi que des accessoires standard et en option,
nous nous référons au site Web www.enraf-nonius.com.

Page 15 de 52 FR109-1634750-40 IFU
5 Installation
Inspection
Si vous constatez des dommages dus au transport, contactez votre distributeur local.
N'UTILISEZ PAS l'appareil !
L'appareil doit être installé de manière à ce que sa chaleur puisse être transmise à
l'environnement.
Immédiatement après avoir déballé l'appareil, procédez comme suit :
• Vérifiez les documents de livraison pour vous assurer que la livraison est complète.
• Vérifier que l'emballage contient tous les éléments énumérés dans la liste des accessoires
standard. (Reportez-vous au chapitre 4 - Contenu de l'emballage de ce manuel).
• Vérifiez que les composants externes et les accessoires ne présentent pas d'éventuels dommages
dus au transport.
Déballage
Endomed 182 est spécialement emballé pour le transport dans un seul paquet avec un remplissage
qui a été spécialement conçu pour un transport et un stockage en toute sécurité.
• Pour sortir l'équipement de l'emballage, placez la boîte sur une surface lisse et plane.
• Ouvrez le haut de la boîte et retirez le remplissage en polystyrène.
• Soyez prudent quand vous retirez le contenu du paquet.
Configuration de l'appareil
Endomed 182 Type 2:
• Connectez le câble du Module Courant [9] au Connecteur B [8].
Endomed 182 Type 3:
• Connectez le câble du Module Courant [9] au Connecteur B [8].
• Connectez le câble du Module de Vide [13] au Connecteur A [7].
Reportez-vous au chapitre 3 - Composants de l'appareil dans ce manuel.
Raccordement au secteur
L'utilisation de tout autre câble que le câble fourni est strictement INTERDITE, car
elle affecte la sécurité du patient et le bon fonctionnement de l'appareil.
Avant de raccorder l'appareil au secteur, vérifiez que la tension et la fréquence du secteur
indiquées sur la plaque signalétique de l'appareil correspondent à celles du secteur.
Pour éviter tout risque de choc électrique, cet appareil ne doit être branché qu'à un réseau
d'alimentation avec mise à la terre protégée.
Raccordez l'appareil à une prise murale à l'aide du câble secteur.
• Insérez le câble secteur dans la prise [19] et raccordez-le à une prise murale.
Déconnexion de l'alimentation secteur
• Lorsque vous avez terminé le traitement, éteignez l'appareil en mettant l'interrupteur secteur
sur Arrêt.
• Débranchez le câble secteur de la prise murale.
• Débranchez le câble secteur de la prise [19].

Page 16 de 52 FR109-1634750-40 IFU
6 Usage et utilisateur prévus
Usage prévu
Endomed 182 Type 1
L'Endomed 182 Type 1 est un électrostimulateur monocanal destiné et conçu pour être utilisé par les
professionnels de la santé pour effectuer une électrolyse percutanée (EP) au moyen d'un courant
continu (CC) de faible intensité.
Endomed 182 Type 2 et 3
Les Endomed 182 Type 2 et 3 sont des électrostimulateurs à 2 canaux destinés et conçus pour être
utilisés par les professionnels de la santé pour la gestion de la douleur au moyen d'un courant
interférentiel (CIF) et d'un courant de TENS.
La gestion de la douleur par électrostimulation désigne :
- Le soulagement symptomatique de la douleur chronique et irréductible
- La prise en charge de la douleur associée aux états post-traumatiques ou post-opératoires
- Le soulagement de la douleur associée à l'arthrite
La stimulation électrique est appliquée sur la peau par l'intermédiaire d'électrodes de surface dans
le but de stimuler des types spécifiques de fibres nerveuses. Le soulagement de la douleur
(modulation de la douleur) peut être obtenu :
1. en bloquant l'information circulant le long des fibres nociceptives (c'est-à-dire celles qui
provoquent la douleur) par stimulation des fibres A afférentes de grand diamètre ;
2. par la libération des opioïdes endogènes de l'organisme en stimulant les fibres afférentes et
motrices de petit diamètre.
Utilisateur prévu
L'Endomed 182 est destiné à être utilisé, et ne doit être utilisé que par des utilisateurs
professionnels dans le domaine de la médecine physique et de la réadaptation dans des
établissements de santé professionnels, ou sous leur supervision.
En outre pour Endomed 182 Type 1 :
Si un professionnel de la santé (physiothérapeute, médecin) est autorisé et formé à utiliser le
traitement par électrolyse galvanique échoguidée, le professionnel de la santé est autorisé et formé
à effectuer les opérations suivantes :
-> effectuer des piqûres d'aiguille sur un patient ;
-> utiliser l'échographie ;
-> utiliser le traitement par électrolyse galvanique.

Page 17 de 52 FR109-1634750-40 IFU
7 Indications
Indications Endomed 182 Type 1
Électrolyse percutanée
L'électrolyse percutanée (EP) peut être utilisée pour le traitement des troubles suivants :
• Maladie de Sinding-Larsen et Johansson / tendinite patellaire (« genou du sauteur »)
• Tendinopathie en latéral du coude (tennis elbow)
• Tendinopathie externe du coude (golf elbow)
• Syndrome de douleur myofasciale / Points de déclenchement (trigger points)
• Syndrome du whiplash aigu (AWS)
• Troubles de l'épaule (tendinopathies de la coiffe des rotateurs, syndrome de douleur sous-
acromiale)
• Pubalgie (douleur à l'aine)
• Tendinopathie des muscles ischio-jambiers
• Tendinopathie du tendon d'Achille
• Fasciite plantaire / Douleur au talon
Indications Endomed 182 Type 2 et 3
TENS
Soulagement de la douleur aiguë
• Douleur post-opératoire
o Abdominale
o Thoracique
o Douleur orthopédique post-opératoire
• Douleur de l'accouchement et douleur post-accouchement
• Dysménorrhée
• Douleur bucco-faciale, y compris les interventions dentaires
• Traumatisme physique, y compris fractures des côtes et interventions médicales mineures
Soulagement de la douleur chronique
• Lombalgie
• Douleur arthritique, y compris l'arthrose et la polyarthrite rhumatoïde
• Douleur musculaire, y compris la douleur myofasciale, la tension musculaire et la douleur
post-exercice
• Douleur neuropathique, y compris post-amplification (douleur fantôme), post-herpétique
et névralgie du trijumeau
• Douleur cancéreuse, y compris douleur osseuse métastatique
• Algoneurodystrophie
Courant interférentiel
Soulagement de la douleur aiguë et chronique, par exemple :
• Douleur post-opératoire / douleur orthopédique
• Lombalgie
• Douleur au cou
• Douleur à l'épaule
• Douleur arthritique, y compris l'arthrose et la polyarthrite rhumatoïde
• Douleur musculaire, y compris la douleur myofasciale, la tension musculaire, la douleur
post-exercice et fibromyalgie
Stimulation musculaire
• Renforcement musculaire (en général)
• Incontinence fécale et urinaire
Dysfonctionnement intestinal
Augmentation du flux sanguin (cutané) local

Page 18 de 52 FR109-1634750-40 IFU
8 Contre-indications
L'Endomed 182 NE PEUT PAS être utilisé dans le cadre des pathologies et symptômes
mentionnés ci-dessous.
Contre-indications Endomed 182 Type 1
Contre-indications d'utilisation
• Arthrite infectieuse
• Maladie cardiaque / arythmie cardiaque
• Grossesse
• Ulcères cutanés et autres infections cutanées
• Endoprothèses et/ou ostéosynthèses
• Pacemakers
• Processus oncologiques
• Thrombophlébite / antécédents d'insuffisance vasculaire dans les jambes
• Coagulopathie / médicaments anticoagulants
• Dyscrasie sanguine
• Menstruations
• Phobie des aiguilles
• Peur de l'électrostimulation
• Glandes endocrines
• Patients présentant une altération de la sensibilité
• Patients souffrant de troubles neurologiques centraux et périphériques
• Patients atteints de troubles neurovégétatifs
• Patients pédiatriques
• Affections médicales compliquées
• Déficience cognitive
• Abus de drogues ou d'alcool
Points auxquels des traitements ne doivent pas être appliqués :
• Vaisseaux sanguins
• Glandes endocrines
• Organes
• Nerfs périphériques (endoneurium)
• Tête, yeux, nuque et thorax ou partie supérieure du dos, en traversant le cœur
Précautions relatives à l'électrolyse percutanée
Régions nécessitant une prudence particulière :
• Région abdominale
• Région intercostale (précaution contre le pneumothorax)
• Région thoracique (précaution contre le pneumothorax)
• Sortie thoracique (précaution contre le pneumothorax)
• Région inguinale, creux poplité (précaution contre l'endommagement des faisceaux
neurovasculaires)

Page 19 de 52 FR109-1634750-40 IFU
Contre-indications Endomed 182 Type 2 et 3
Contre-indications absolues :
• Douleur non diagnostiquée
• Implants actifs (y compris stimulateurs cardiaques et défibrillateurs automatiques implantables
- DAI)
• Saignement des tissus (hémorragie)
• Patients qui ne comprennent pas les instructions du praticien/physiothérapeute ou qui sont
incapables de coopérer
Contre-indications relatives (= contre-indications locales) :
• Grossesse (ne pas appliquer n'importe où sur l'abdomen/la région pelvienne)
• Tumeur maligne (ne pas appliquer sur la tumeur maligne active)
• Épilepsie (ne pas appliquer sur le cou ou la tête)
• Troubles cardiaques tels que dysrythmies (ne pas appliquer sur la poitrine)
• Placement des électrodes autour des yeux
• Placement des électrodes sur la face antérieure du cou ou du sinus carotidien
• Placement des électrodes sur la poitrine (c.-à-d. positions des électrodes antérieures et
postérieures)
• Placement des électrodes sur les testicules
• Placement des électrodes sur les régions épiphysaires actives chez les enfants
• Placement des électrodes sur une peau abîmée ou des plaies ouvertes
• Placement des électrodes sur des lésions dermatologiques, p. ex. dermatite, eczéma ou sur une
peau fragile
• Placement des électrodes au-dessus de zones présentant un tissu ischémique et/ou une
thrombose
Remarque : Il n'existe aucun effet indésirable connu de l'administration de la TENS / Courant
Interférentiel sur la peau au-dessus ou à proximité d'implants métalliques. TENS / Courant
Interférentiel peuvent être utilisés sur la peau intacte recouvrant des implants contenant du métal,
du plastique ou du ciment. Des personnes ayant des prothèses articulaires comprenant des
composants métalliques ont été traitées par électrostimulation et en ont tiré des avantages sans
subir d'effets indésirables.
Précautions TENS et Courant Interférentiel
• Zones présentant une sensation cutanée anormale (dysesthésie)
o hyperesthésie (allodynie/hyperalgie)
o hypoesthésie
• Dermatite de contact
• Femmes enceintes
• Patients sensibles aux réactions autonomes de la TENS (nausées, étourdissements et
évanouissements, par exemple).
Effets indésirables potentiels
On a signalé des cas d'irritation et d'attaque cutanées sous les électrodes lors de l'utilisation d'une
stimulation électrique thérapeutique.
Des cas isolés d'irritation cutanée peuvent survenir chez les patients dont la peau est
particulièrement sensible. En cas de réaction allergique au gel d'électrode, suspendez le traitement
et contactez un spécialiste. Si, pendant le traitement, des signes de tachycardie et d'extrasystole
apparaissent, suspendez le traitement et contactez votre médecin.

Page 20 de 52 FR109-1634750-40 IFU
9 Consignes de sécurité
Si l'utilisation de cet appareil a entraîné ou a contribué à entraîner des effets indésirables
menant au décès de l'utilisateur ou à des blessures graves, le fabricant ET l'autorité
compétente de l'État membre DOIVENT être immédiatement prévenus !
Cet appareil doit être tenu hors de portée des enfants.
Le patient et l'appareil doivent être à portée de vue du thérapeute en tout temps.
N'utilisez pas cet appareil dans les « pièces humides » (salles d'hydrothérapie).
Cet équipement n'est pas adapté à une utilisation en présence d'un mélange d'anesthésiques
inflammables avec de l'air, de l'oxygène ou du protoxyde d'azote.
N'exposez pas l'appareil à la lumière directe du soleil, à la chaleur d'un radiateur, à des
quantités excessives de poussière, à l'humidité, aux vibrations et aux chocs mécaniques.
L'appareil doit être utilisé uniquement sous la surveillance continue d'un médecin ou d'un
praticien autorisé.
Si vous constatez des dommages dus au transport, contactez votre distributeur local.
N'UTILISEZ PAS l'appareil !
L'appareil doit être installé de manière à ce que sa chaleur puisse être transmise à
l'environnement.
L'utilisation de tout autre câble que le câble fourni est strictement INTERDITE, car elle affecte
la sécurité du patient et le bon fonctionnement de l'appareil.
Avant de raccorder l'appareil au secteur, vérifiez que la tension et la fréquence du secteur
indiquées sur la plaque signalétique de l'appareil correspondent à celles du secteur.
Pour éviter tout risque de choc électrique, cet appareil ne doit être branché qu'à un réseau
d'alimentation avec mise à la terre protégée.
N'utilisez pas l'appareil après des variations de température extrêmes.
Avant de commencer le traitement, assurez-vous que : Vous avez lu et compris le contenu du
présent manuel
Avant de commencer le traitement, assurez-vous que : Vous suivez scrupuleusement les
AVERTISSEMENTS et les MISES EN GARDE mentionnés dans les Précautions d’emploi
Avant de commencer le traitement, assurez-vous que : Vous avez vérifié que le patient ne
présentait pas de contre-indications éventuelles.
Le raccordement d'accessoires autres que ceux spécifiés par le fabricant peut nuire à la
sécurité du patient et au bon fonctionnement de l'appareil et n'est donc pas autorisé.
Pour prévenir l'infection, évitez d'utiliser les électrodes et les tampons éponges sur une peau
abîmée.
Pendant le traitement, le patient ne peut pas ressentir de sensations désagréables
assimilables à de la douleur. Une légère sensation d'excitation est admise.
Si, à la suite du traitement, des céphalées, des vertiges, de la fatigue et/ou d'autres réactions
(du système nerveux autonome) surviennent, le traitement suivant doit être administré à une
intensité plus faible.
l est recommandé de garder les appareils de diathermie (comme les appareils à ondes
courtes et à micro-ondes) à au moins un mètre appareils d'électrostimulation, car la sortie des
appareils d'électrostimulation peut être affectée par la proximité d'une machine à ondes
courtes ou à micro-ondes (à impulsions) en fonctionnement.
La stimulation ne doit pas être appliquée à travers ou sur la tête, directement sur les yeux, en
couvrant la bouche, sur le devant du cou (en particulier le sinus carotidien), ou à partir
d'électrodes placées sur la poitrine et le haut du dos ou traversant le cœur.
L'application d'électrodes près du thorax peut augmenter le risque de fibrillation cardiaque.
La connexion simultanée d'un patient à un équipement électrique médical chirurgical à haute
fréquence peut entraîner des brûlures au niveau des électrodes du stimulateur et d'éventuels
dommages au stimulateur.

Page 21 de 52 FR109-1634750-40 IFU
Toutes les électrodes dont la densité de courant est supérieure à 2 mA/cm² peuvent
nécessiter une attention particulière de la part de l'opérateur.
L'utilisation répétée d'électrodes prégélifiées entraîne une perte rapide de conductivité et une
détérioration de l'adhésivité.
La perte d'adhérence et le séchage du gel provoquent le soulèvement des bords, ce qui peut
augmenter considérablement la densité du courant et provoquer une distribution inégale du
courant sur la surface de l'électrode. Cela peut augmenter le risque de brûlure et entraîner un
mouvement de l'électrode.
Les changements qui se produisent dans les électrodes auto-adhésives au fil du temps
mènent à une situation dangereuse susceptible de provoquer une irritation de la peau et
l'inconfort du patient.
Les électrodes auto-adhésives ne doivent jamais être partagées entre patients.
Nettoyez régulièrement l'appareil et ses accessoires afin de maintenir une sécurité hygiénique.
Avant de procéder à une tâche de maintenance utilisateur, mettez l'appareil hors tension et
débranchez-le de la prise secteur.
Ne pulvérisez pas l'agent nettoyant directement sur le panneau en verre.
N'utilisez pas d'agents nettoyants qui contiennent des alcalins forts, de la soude, de l'acide, ou
encore des détergents à base de fluorure ou d'ammoniac.
Ne laissez aucun liquide pénétrer dans l'appareil ou ses accessoires pendant le nettoyage et la
désinfection !
Avant toute nouvelle utilisation, séchez toutes les prises et tous les connecteurs qui sont
mouillés !
Les chocs mécaniques et/ou vibrations DOIVENT être évités lors du nettoyage de l'appareil.
Ne faites pas tomber l'appareil.
L'appareil ne doit pas être utilisé lorsque des dommages mécaniques sont constatés. Cela
inclut les isolations de câble endommagées.
Si un message d'erreur ou un avertissement s'affiche, cessez immédiatement toute utilisation
de l'appareil. Arrêtez l’appareil et redémarrez-le. Si le problème persiste, contactez le
fournisseur ou Enraf-Nonius B.V. en vue d'une réparation. Des erreurs et des avertissements
indiquent un problème interne de l'appareil qui doit être testé par un technicien de terrain
agréé par Enraf-Nonius B.V. avant toute autre utilisation ou mise en service du système.
L'utilisation d'un dispositif qui indique une erreur ou un avertissement peut présenter un
risque de blessure pour le patient, l'utilisateur ou de dommages internes importants au
système.
En cas de panne de l'écran ou d'autres défauts évidents, débranchez immédiatement
l'appareil et contactez un technicien de maintenance agréé.
En cas de pénétration de liquides, débrancher l'appareil du réseau et le faire contrôler par une
personne autorisée.
L'ouverture de l'équipement par des organismes non agréés est interdite et entraînera la
nullité de la garantie.
Le fabricant ne peut pas être tenu responsable des conséquences d'un entretien ou de
réparations réalisés par une personne non habilitée.
Seuls les techniciens de service agréés par Enraf-Nonius peuvent effectuer l'entretien ou
modifier cet équipement conformément aux informations d'entretien.
Si cet équipement est modifié, une inspection et des tests appropriés doivent être effectués
pour garantir une utilisation sûre et continue de l'équipement.
Il est recommandé de faire contrôler chaque année l'Endomed 182 par le personnel autorisé
d'Enraf-Nonius ou par son distributeur agréé.
Les appareils électriques médicaux tels que l'Endomed 182 font l'objet de précautions
particulières au regard de la compatibilité électromagnétique (CEM) et doivent être installés et
mis en service conformément aux recommandations CEM figurant dans le mode d'emploi.

Page 22 de 52 FR109-1634750-40 IFU
L'utilisation de cet équipement à proximité d'autres appareils ou leur empilement sont
déconseillés, car cela risque de provoquer des dysfonctionnements. Dans le cas où une telle
utilisation est nécessaire, cet équipement et les autres appareils doivent être vérifiés afin de
s'assurer qu'ils fonctionnent normalement.
L'utilisation d'accessoires, de transmetteurs et de câbles autres que ceux indiqués ou fournis
par le fabricant de cet équipement peut donner lieu à une augmentation des émissions
électromagnétiques ou une diminution de l'immunité électromagnétique de l'appareil et
entraîner un mauvais fonctionnement.
Les équipements de communication RF portables (y compris les périphériques tels que les
câbles d'antenne et les antennes externes) ne doivent pas être utilisés à moins de 30 cm des
composants de l'Endomed 182, y compris les câbles spécifiés par le fabricant. Sinon, les
performances de cet équipement pourraient se dégrader.
L'Endomed 182 ne doit être utilisé qu'avec le câble d'alimentation d'origine qui figure sur la
liste des éléments livrés. L'utilisation de l'appareil avec un autre câble d'alimentation peut
augmenter les émissions ou réduire son immunité aux interférences.

Page 23 de 52 FR109-1634750-40 IFU
10 Utilisation
Configuration
N'utilisez pas l'appareil après des variations de température extrêmes.
Fonctions fréquemment utilisées
Sélection des boutons Protocoles cliniques (ne s'applique qu'à Endomed 182 Type 2 et 3), Favoris et
Paramétrage manuel sur l'écran tactile.
Mise sous tension
• Allumez l'appareil en appuyant sur le bouton Marche/Arrêt situé à l'arrière de l'appareil.
• Après la mise en marche, l'appareil s'initialisera et un écran de bienvenue s'affichera pendant
que l'appareil effectuera un autotest.
• À la fin de l'autotest, l'appareil entre dans le Menu Principal et est prêt à être utilisé.
Lors de la mise sous tension de l'appareil, toutes les fonctions vitales sont contrôlées par un
microprocesseur interne. Pendant le fonctionnement de l'appareil, la sortie réelle du courant est
mesurée en continu et comparée à la sortie demandée. Dès qu'une situation défectueuse est
détectée, l'appareil coupe immédiatement le courant.
Navigation
Menu Principal
Le Menu Principal donne accès à toutes les fonctions de l'appareil. Le Menu Principal permet un
accès structuré à toutes les thérapies disponibles dans l'appareil, avec les paramètres par défaut
appropriés. Il suffit de sélectionner une option de menu en appuyant sur le bouton pour passer à
l'écran suivant. Vous pouvez revenir à l'écran précédent en appuyant sur le bouton Retour en haut
de l'écran.
• Sélectionnez “Protocoles
préprogrammés” pour
commencer à travailler
avec les protocoles
préréglés. Ceci ne
s'applique pas à Endomed
182 Type 1.
• Sélectionnez "Favoris"
pour utiliser un protocole
enregistré manuellement
• Sélectionner "Paramétrage
manuel" pour régler tous
les paramètres
manuellement
• Sélectionnez “Informations
système”) pour accéder au
menu des paramètres
Endomed 182 Type 1
menu principal
Endomed 182 Type 2 et 3
menu principal

Page 24 de 52 FR109-1634750-40 IFU
Informations système
Sélectionnez Informations système dans le Menu Principal, pour régler divers paramètres, vérifier la
version du logiciel ou restaurer les valeurs par défaut de l'appareil. Les options Retour Acoustique,
Tonalité de sonnerie et Durée de la sonnerie ne sont disponibles que dans les Endomed 182 Type 2
et 3.
Modifier la Langue
1) Sélectionnez “Informations
système”)
2) Sélectionnez “Langue”
3) Sélectionnez la langue
préférée avec des boutons
4) Touchez « OK » pour
confirmer et revenir au menu
précédent.
Modifier le Luminosité écran
Pour modifier la luminosité de
l'écran :
1) Sélectionnez “Luminosité”
2) Réglez la luminosité à l'aide
des boutons
Gamme: 10 – 100%
3) Touchez « OK » pour
confirmer votre choix et
revenir au menu précédent

Page 25 de 52 FR109-1634750-40 IFU
Informations système
1) Sélectionnez “Informations
système”
Dans l'écran suivant, vous
trouverez des informations sur
l'appareil
La version du logiciel
actuellement installée est
indiquée
2) Touchez “RETOUR” pour
revenir au menu précédent
Retour Acoustic
Endomed 182 Type 2 et 3:
Select this option to turn on
or off audio signals at the end
of treatment.
1) Sélectionnez "Retour
Acoustique"
2) Allumer ou éteindre le
feedback acoustique
3) Touchez “RETOUR” pour
revenir au menu précédent

Page 26 de 52 FR109-1634750-40 IFU
Tonalité de sonnerie et Durée de la sonnerie
Endomed 182 Type 2 et 3:
1) Sélectionnez “Tonalité de
sonnerie” ou “Durée de la
sonnerie”
Tonalité de sonnerie donne
accès à 7 airs différents pour
signaler la fin d'un traitement.
Durée de la sonnerie donne
accès à 7 intervalles différents
pour signaler la fin d'un
traitement.
Maintenance
Restaurer les valeurs par
défaut d'usine supprime tous
les favoris enregistrés sur
l'appareil et efface tous les
réglages du système, ce qui
remet l'appareil dans son état
d'usine d'origine.
Le menu Service est destiné
aux organismes de service
qualifiés Enraf-Nonius et ne
peut être entré qu'avec un
code d'accès.
Nettoyage du réservoir
activera la pompe. Voir le
chapitre 12 Entretien et
dépannage. (S'applique
uniquement à l'Endomed 182
Type 3).
1) Sélectionnez “Maintenance”
(Applicable pour Endomed 182
Type 2 et 3)

Page 27 de 52 FR109-1634750-40 IFU
Paramétrage manuel Endomed 182 Type 1
Endomed 182 Type 1 possède un canal de sortie. Voir chapitre 11 pour la connexion des électrodes.
1) Sélectionnez "Paramètres
manuels" dans Menu Principal
Sélectionnez (K) pour fixer la Durée
de traitement
Sélectionnez (L) pour régler
l'intensité
2) Fixer la Durée de traitement
Option: 3 s / 10 s / 60 s
Ou via les boutons
3) Régler l'intensité
Option: 1 mA / 3 mA / 5 mA
Ou via les boutons
4) Pressez le bouton Start
(l’interrupteur au pied quand
connecté) pour commencer le
traitement
5) Pressez le bouton Stop (ou
l’interrupteur au pied quand
connecté) pour arrêter le
traitement.
Le traitement s'arrête
automatiquement lorsque le
temps de traitement est écoulé.
K
L

Page 28 de 52 FR109-1634750-40 IFU
Protocoles cliniques
Pour les Endomed 182 de type 2 et 3, une liste des traitements d'électrothérapie courants peut être
trouvée sous Protocoles cliniques. Ces protocoles fondés sur des preuves ont été créés par des
opérateurs professionnels et experts après des années d'expérience dans le domaine.
Les protocoles préprogrammés sont ajustables et réinscriptibles. Voir chapitre 11 pour la connexion
des électrodes.
1) Sélectionnez “Protocoles
cliniques” sur Menu Principal
pour activer la liste.
2) Sélectionnez le bouton
pour faire défiler la liste.
3) Sélectionnez l'icône
pour plus d'informations sur
le
protocole
4) Sélectionnez le Protocole
Clinique choisi pour accéder à
l'écran des paramètres
Écran d'information sur le
protocole
5) Touchez les boutons
pour faire défiler les pages
6) Sélectionnez OK pour aller
à l'écran des paramètres ou
RETOUR pour revenir au
menu des Protocoles cliniques

Page 29 de 52 FR109-1634750-40 IFU
7) L'écran des paramètres
affiche tous les paramètres
d'un seul coup d'œil
8) Les paramètres prédéfinis du
protocole clinique peuvent être
ajustés
9) Appuyez sur l'onglet de
canal 1 ou 2 en bas de l'écran
pour modifier le niveau
d'intensité
10) Régler le niveau d'intensité
via les boutons
11) Sélectionnez OK pour
confirmer et revenir à l'écran
précédent
12) Le protocole commencera
après avoir fixé le niveau
d'intensité
13) Le protocole peut être
arrêté en appuyant sur l'icône
d'arrêt (A) sur l'écran tactile. Le
protocole s'arrête
automatiquement lorsque le
temps de traitement est écoulé.
A

Page 30 de 52 FR109-1634750-40 IFU
Paramétrage manuel Endomed 182 Type 2 et Type 3
Paramètrage Manuel permet de définir des paramètres personnels pour l'électrothérapie.
L'Endomed 182 Type 2 et 3 possède deux canaux de sortie indépendants. Pour sélectionner le canal
de sortie, touchez l'onglet du canal en bas de l'écran. Voir le chapitre 11 pour la connexion des
électrodes.
1) Sélectionnez "Paramètrage
Manuel" dans Menu Principal
2) Sélectionnez la forme d'onde
courante souhaitée ; l'écran des
paramètres apparaît
3) En fonction de la forme
d'onde courante sélectionnée,
différents paramètres peuvent
être définis.
Configuration des paramètres : Fréquence
1) Sélectionnez Fréquence (B)
2) Ajustez Fréquence via les
boutons
Gamme : 1 Hz – 200 Hz
3) Sélectionnez OK pour
confirmer et revenir à l'écran
précédent
B

Page 31 de 52 FR109-1634750-40 IFU
Configuration des paramètres : Fréquence des salves
1) Sélectionnez Fréquence des
salves (C)
2) Ajustez Fréquence des
salves
Option : 1 Hz / 2 Hz / 4 Hz
3) Sélectionnez OK pour
confirmer et revenir à l'écran
précédent
Configuration des paramètres : Fréquence de modulation
1) Sélectionnez Fréquence de
modulation (D)
2) Ajustez Fréquence de
modulation via les boutons
Gamme : 1 Hz- 180 Hz
3) Sélectionnez OK pour
confirmer et revenir à l'écran
précédent
D
C

Page 32 de 52 FR109-1634750-40 IFU
Configuration des paramètres : Durée de modulation
1) Sélectionnez Durée de
modulation (E)
2) Ajustez Durée de
modulation
Option :
1-1 secondes
6-6 secondes
1-30 secondes
3) Sélectionnez OK pour
confirmer et revenir à l'écran
précédent
Configuration des paramètres : Durée de traitement
1) Sélectionnez Durée de
traitement (F)
2) Ajustez Durée de
traitement via les boutons
Gamme: 0 to 60 minutes
3) Sélectionnez OK pour
confirmer et revenir à l'écran
précédent
E
F

Page 33 de 52 FR109-1634750-40 IFU
Configuration des paramètres : Module de Vide
Avec l'Endomed 182 Type 3, il
est possible d'utiliser des
électrodes à vide
1) Sélectionnez Vide (G)
2) Définir les paramètres du
vide
Option : mode pulsé 1 Hz /
mode pulsé 2 Hz / continu
3) Régler la pression des
ventouses via les boutons
Les ventouses sont
automatiquement
sélectionnées lorsque la
pompe commence à
fonctionner
Configuration des paramètres : Intensité
1) Pressez l'onglet du canal 1
ou 2 (H) en bas de l'écran pour
régler le niveau d'intensité
(après avoir réglé la durée de
traitement)
2) Ajustez le niveau d'intensité
via les boutons
3) Sélectionnez OK pour
confirmer et revenir à l'écran
précédent
4) Le programme commencera
après avoir fixé le niveau
d'intensité
5) Le programme peut être
arrêté en appuyant sur l'icône
d'arrêt sur l'écran tactile. Le
programme s'arrête
automatiquement lorsque le
temps de traitement est écoulé.
H
G

Page 34 de 52 FR109-1634750-40 IFU
Configuration des paramètres : Contrôle de la balance
Pour 4P Interférence
quadripolaire, l'option de
contrôle de la balance est
disponible après que l'intensité
ait été définie.
Avec le contrôle de la balance,
l'intensité du canal 1 par
rapport au canal 2 peut être
augmentée ou diminuée. Une
augmentation de l'intensité du
canal 1 diminuera
automatiquement l'intensité
du canal 2 et vice versa.
1) Sélectionner le contrôle de
la balance (I)
2) Définir les paramètres de
contrôle de la balance
3) Sélectionnez OK pour
confirmer et revenir à l'écran
précédent
Configuration des paramètres : Vue Vecteur
Pour Vecteur isoplanaire
quadripolaire, un écran de
visualisation du vecteur est
disponible après le début du
traitement.
1) Sélectionnez Vue Vecteur
(J)
Dans cet écran, on peut voir
une animation des anneaux
de rétrécissement et de
gonflement rythmiques ainsi
que le temps de traitement
restant et le niveau
d'intensité.
J
I

Page 35 de 52 FR109-1634750-40 IFU
Favoris
Avant l'exécution d'un protocole préprogrammé modifié ou d'un réglage manuel, il peut être
sauvegardé pour une utilisation ultérieure dans les favoris.
Lorsque tous les paramètres de l'écran de traitement sont entièrement réglés comme requis, vous
pouvez choisir d'enregistrer les réglages comme favoris en appuyant sur le bouton de
mémorisation.
Les favoris peuvent être enregistrés tant que le traitement n'a pas été démarré.
1) Pressez Sauvegarde (M) pour
sauvegarder les paramètres du
programme
2) Sélectionnez le numéro du
programme via les boutons
20 emplacements de magasins
sont disponibles pour les 182
Endomed
3) Sélectionnez OK pour
confirmer
4) Entrez un nom pour votre
favori.
5) Touchez OK pour enregistrer
le favori.
M

Page 36 de 52 FR109-1634750-40 IFU
Chargement et Suppression des Favoris
1) Sélectionnez "Favoris" dans
le Menu Principal.
2) Pour charger un programme,
sélectionnez un favori à l'aide
des boutons
L'écran des paramètres
s'affiche.
3) Pour supprimer un favori,
touchez le bouton de
suppression (N) et sélectionnez
le favori à supprimer à l'aide
des boutons .
4) Touchez OK pour supprimer
définitivement le favori.
N

Page 37 de 52 FR109-1634750-40 IFU
11 Informations d’application
Avant de commencer le traitement, assurez-vous que : Vous avez lu et compris le contenu du
présent manuel
Avant de commencer le traitement, assurez-vous que : Vous suivez scrupuleusement les
AVERTISSEMENTS et les MISES EN GARDE mentionnés dans les Précautions d’emploi
Avant de commencer le traitement, assurez-vous que : Vous avez vérifié que le patient ne
présentait pas de contre-indications éventuelles.
Le raccordement d'accessoires autres que ceux spécifiés par le fabricant peut nuire à la
sécurité du patient et au bon fonctionnement de l'appareil et n'est donc pas autorisé.
Pour prévenir l'infection, évitez d'utiliser les électrodes et les tampons éponges sur une peau
abîmée.
Pendant le traitement, le patient ne peut pas ressentir de sensations désagréables
assimilables à de la douleur. Une légère sensation d'excitation est admise.
Si, à la suite du traitement, des céphalées, des vertiges, de la fatigue et/ou d'autres réactions
(du système nerveux autonome) surviennent, le traitement suivant doit être administré à une
intensité plus faible.
l est recommandé de garder les appareils de diathermie (comme les appareils à ondes
courtes et à micro-ondes) à au moins un mètre appareils d'électrostimulation, car la sortie des
appareils d'électrostimulation peut être affectée par la proximité d'une machine à ondes
courtes ou à micro-ondes (à impulsions) en fonctionnement.
La stimulation ne doit pas être appliquée à travers ou sur la tête, directement sur les yeux, en
couvrant la bouche, sur le devant du cou (en particulier le sinus carotidien), ou à partir
d'électrodes placées sur la poitrine et le haut du dos ou traversant le cœur.
L'application d'électrodes près du thorax peut augmenter le risque de fibrillation cardiaque.
La connexion simultanée d'un patient à un équipement électrique médical chirurgical à haute
fréquence peut entraîner des brûlures au niveau des électrodes du stimulateur et d'éventuels
dommages au stimulateur.
Toutes les électrodes dont la densité de courant est supérieure à 2 mA/cm² peuvent
nécessiter une attention particulière de la part de l'opérateur.
Connexion des électrodes
Voir le chapitre 3 pour la description des parties numérotées.
Endomed 182 Type 1
• Raccordez le câble de référence CC [5] au connecteur [3]
• Raccordez l'électrode de masse vierge [4] au câble de référence CC [5]
• Utilisation d'une électrode de masse vierge : pendant le traitement, le patient doit tenir
l'électrode de masse vierge à la main
• Raccordez le porte-électrode [6] au connecteur [2]
• Fixez l'aiguille (non fournie) au porte-électrode par le système de filetage, ce qui permet
d'ouvrir le porte-électrode, d'insérer l'aiguille et de fermer le porte-électrode
• Le porte-électrode est équipé d'une touche Marche/Arrêt permettant de démarrer ou
d'interrompre manuellement le flux de courant.

Page 38 de 52 FR109-1634750-40 IFU
Endomed 182 Type 2
• Raccordez les câbles patients au connecteur 1 [10] et/ou au connecteur 2 [11] du module de
courant [9] (fiche rouge dans le connecteur rouge, fiche noire dans le connecteur noir).
• Raccordez les électrodes au câble patient.
Endomed 182 Type 3
• Pour l'utilisation d'électrodes adhésives ou en caoutchouc : raccordez les câbles patients aux
connecteurs supérieurs [15] du module à vide [13] et raccordez les électrodes aux câbles
patients (fiche rouge dans le connecteur rouge, fiche noire dans le connecteur noir).
• Pour l'utilisation d'électrodes à vide : raccordez les flexibles des électrodes à vide aux
connecteurs inférieurs [16] du module à vide [13] et raccordez les électrodes des électrodes à
vide aux flexibles des électrodes à vide (fiche rouge dans le connecteur rouge, fiche noire dans
le connecteur noir).
Traitement
Avant le traitement
• Nettoyez (dégraissage) la peau de la zone concernée avec du savon ou de l'alcool à 70 %.
• En cas de peau poilue, un rasage est recommandé.
• Testez la sensibilité de la zone à traiter.
• Positionnez les électrodes et/ou les éponges (n'oubliez pas de les humidifier).
• Suivez les instructions du chapitre 10 sur la manière de régler les paramètres et de démarrer et
d'arrêter le traitement
Pendant le traitement
• L'intensité est réglée au niveau souhaité.
• Interrogez régulièrement le patient sur ses sensations. Le cas échéant, modifiez le traitement.
Fin du traitement
• Il est possible d'arrêter le traitement en appuyant sur l'icône Stop sur l'écran tactile ou en
réglant le minuteur sur zéro. Le traitement s'arrête automatiquement lorsque le temps de
traitement est écoulé.
Après le traitement
• Retirez les électrodes et/ou les éponges.
• Nettoyez la peau du patient à l'aide d'une serviette ou d'un mouchoir.
• Les effets attendus sont vérifiés (p. ex. douleur, circulation et mobilité).
• Il est demandé au patient de commenter ultérieurement toute réaction susceptible de survenir.
Endomed 182 Type 1 :
Électrolyse Percutanée
L'électrolyse percutanée (EP) est une technique de traitement non pharmacologique mini-invasive
pour les tendinopathies chroniques et présente peu d'effets secondaires par rapport à une
intervention pharmaceutique. L'EP est généralement bien tolérée par la plupart des patients, et les
complications et les effets indésirables sont extrêmement rares. Cependant, les patients doivent
être informés des risques potentiels associés à l'application de l'électrolyse percutanée :
• Le traitement peut produire une légère douleur qui dure normalement de 48 à 72 heures
L'un des effets secondaires les plus courants liés à l'intervention est l'inconfort dans la zone traitée,
causé par l'insertion de l'aiguille. Lors des applications de courant galvanique, les patients peuvent
ressentir une douleur modérée à forte (selon l'intensité utilisée). Habituellement, aucun anesthésique
n'est injecté localement avant l'électrolyse percutanée, car la procédure est généralement bien
tolérée par les patients (l'application de courant galvanique peut être arrêtée à tout moment si la

Page 39 de 52 FR109-1634750-40 IFU
douleur n'est pas supportable). En outre, l'utilisation de seringues pour introduire les anesthésiques
augmenterait considérablement le caractère invasif global de l'intervention. Toutefois, l'utilisation
d'anesthésiques reste une option à envisager.
• Réactions vasovagales pendant et immédiatement après l'intervention
L'électrolyse percutanée affecte le système nerveux autonome. Comme dans toute procédure
impliquant des aiguilles, des réactions vagales (telles que pâleur, transpiration, piloérection et
froideur de la peau) ont été signalées lors de l'EP. Plusieurs études contiennent des informations sur
le risque potentiel d'éventuelles réactions vasovagales. Ces réactions peuvent être largement
justifiées par l'effet de l'aiguille et pas seulement par celui du courant.
• Saignement dans la zone d'insertion de l'aiguille
Après le traitement, un pansement compressif peut être appliqué, mais cela n'est normalement pas
nécessaire.
L'utilisation de glace ou la prise de tout médicament anti-inflammatoire (AINS) dans les 72 heures
qui suivent le traitement n'est pas recommandée, car cela contrarierait l'effet thérapeutique attendu
(amorcer un processus inflammatoire contrôlé).
Aiguille d'acupuncture
Il est recommandé d'utiliser des aiguilles d'acupuncture de haute qualité, à usage unique et stériles,
qui ont reçu l'approbation médicale CE, y compris le numéro d'Organisme Notifié. Enraf-Nonius ne
fournit pas d'aiguilles. L'aiguille doit être compatible avec l'application de l'électrolyse échoguidée.
En ce qui concerne les dimensions de l'aiguille, veillez toujours à choisir l'épaisseur et la longueur
correctes pour le type de blessure à traiter.
• Diamètre de l'aiguille : 0,30 mm – 0,35 mm
• Diamètre extérieur de la poignée : 1,25 mm – 1,45 mm
• Longueur du corps de l'aiguille : 20 mm – 100 mm
• Longueur de la poignée : 25 mm – 30 mm
Interrupteur au pied
L'Endomed 182 Type 1 dispose d'une pédale en option qui peut être raccordée au connecteur A [7]
(voir chapitre 3).
Placez la pédale de manière à ce qu'elle soit facilement
accessible pendant le traitement. L'unité de commande de la
pédale est multidirectionnelle, il n'est donc pas nécessaire
d'aligner précisément la pédale.
Pour éviter tout dommage, veuillez noter que seule une légère
pression doit être exercée sur l'interrupteur. Utilisez la partie
avant de votre pied, et non le talon, pour actionner la pédale.
Appuyez une fois sur la pédale pour activer le traitement. Appuyez à nouveau sur la pédale pour
arrêter le traitement.

Page 40 de 52 FR109-1634750-40 IFU
Endomed 182 Type 2 et 3 :
TENS / courant interférentiel
Protocol for the safe application of TENS / courant interférentiel
• Vérifiez les contre-indications avec le patient
• Testez si la sensation de la peau est normale à l'aide d'un test émoussé/tranchant.
• L'appareil doit être hors tension et les fils électriques débranchés.
• Réglez les caractéristiques électriques de la TENS / courant interférentiel lorsque l'appareil est
hors tension
• Raccordez les électrodes aux broches du fil conducteur et positionnez les électrodes sur la peau
du patient.
• Assurez-vous que l'appareil est toujours hors tension et raccordez le fil d'électrode à l'appareil.
• Mettez l'appareil sous tension.
• Augmentez progressivement (lentement) l'intensité jusqu'à ce que le patient ressente la
première sensation de « picotement » du stimulateur.
• Augmentez progressivement (lentement) l'intensité jusqu'à ce que le patient ressente une
sensation de « picotement » forte mais confortable.
Protocole pour l'arrêt sûr de la TENS / courant interférentiel
• Diminuez progressivement (lentement) l'intensité jusqu'à ce que le patient ne ressente plus de
« picotements ».
• Mettez l'appareil hors tension.
• Débranchez le fil de l'électrode de l'appareil.
• Débranchez les électrodes des broches du fil conducteur.
• Retirez les électrodes de la peau du patient.
Endomed 182 Type 2 et 3:
Électrodes flexibles en caoutchouc
Nous recommandons d'utiliser les électrodes flexibles en caoutchouc en combinaison avec les
tampons éponges fournis. Lorsqu'ils sont correctement humidifiés, les tampons éponges assurent
une faible impédance entre la peau et le stimulateur pendant le traitement et se nettoient
facilement par la suite. Suivez les lignes directrices ci-dessous lors de l'utilisation de ces électrodes.
• Avant la première utilisation, rincez soigneusement les tampons éponges à l'eau tiède du
robinet pour éliminer l'agent d'imprégnation.
• Avant l'application, saturez les tampons éponges avec de l'eau du robinet. Pour une meilleure
conduction électrique, il est préférable d'utiliser une solution saline.
• Les tampons éponges fournis possèdent trois couches. Avec des courants CA, appliquez une
couche d'éponge entre la peau et l'électrode pour une résistance minimale.
• Fixez l'ensemble électrode/tampon éponge au patient à l'aide des sangles de fixation fournies.
Selon la taille de l'électrode, utilisez deux ou trois enveloppements pour maximiser la surface
de contact. Voir les illustrations ci-dessous.
Mauvaise application des sangles de fixation,
entraînant une mauvaise conductivité électrique
Application correcte des sangles de fixation, entraînant
une bonne conductivité électrique

Page 41 de 52 FR109-1634750-40 IFU
• Il est important que les électrodes restent en contact complet sans que les bords ne se
soulèvent pendant toute la durée du traitement.
• Le mode de sortie d'Endomed 182 est le courant constant (CC). Ceci maintiendra l'amplitude de
courant réglée, même lorsque l'impédance des tampons éponges augmente pendant le
traitement en raison de l'évaporation de l'eau.
• Gardez les tampons éponges bien humidifiés (prêts à dégouliner lorsque vous les pressez
légèrement) pendant le traitement. Réhumidifiez-les si le traitement dure plus de 10 minutes.
• Après utilisation, nettoyez les tampons éponges comme décrit à la section « Nettoyage et
désinfection ».
Endomed 182 Type 2 et 3:
Électrodes auto-adhésives
L'utilisation répétée d'électrodes prégélifiées entraîne une perte rapide de conductivité et une
détérioration de l'adhésivité.
La perte d'adhérence et le séchage du gel provoquent le soulèvement des bords, ce qui peut
augmenter considérablement la densité du courant et provoquer une distribution inégale du
courant sur la surface de l'électrode. Cela peut augmenter le risque de brûlure et entraîner un
mouvement de l'électrode.
Les changements qui se produisent dans les électrodes auto-adhésives au fil du temps
mènent à une situation dangereuse susceptible de provoquer une irritation de la peau et
l'inconfort du patient.
Les électrodes auto-adhésives ne doivent jamais être partagées entre patients.
Les électrodes auto-adhésives ont une impédance de série plus élevée que les électrodes flexibles
en caoutchouc. Cela peut amener le stimulateur à interrompre le traitement à des amplitudes de
courant plus élevées. Dans ce cas, il est recommandé de poursuivre le traitement à l'aide
d'électrodes flexibles en caoutchouc, combinées à des tampons éponges correctement humidifiés.

Page 42 de 52 FR109-1634750-40 IFU
Endomed 182 Type 3:
Electrodes sous vide
Il y a un choix de grandes et petites électrodes. Les surfaces des électrodes correspondent à celles
des électrodes en caoutchouc de 4x6 cm, de 6x8 cm et de 8 x 12 cm. Les électrodes sous vide sont
suffisamment flexibles pour assurer un contact optimum avec la peau, mais assez rigides pour
empêcher toute modification importante de la surface cutanée et permettent ainsi de profiter au
maximum de l’effet de massage provoqué par le rythme d’aspiration.
L’effet de massage causé par la succion stimule la circulation sanguine dans la
peau sous les électrodes, de sorte que la résistance de la peau diminue, l’effet du courant de
stimulation augmente et que le temps de traitement soit réduit.
• Choisir la taille des électrodes, selon la surface corporelle à traiter
• Mouiller les éponges. Ensuite les essorer légère-ment et les placer dans les électrodes à
succion
• Choisir la succion constante, cela facilité le positionnement des electrodes
• Placer les électrodes à succion sur une surface lisse (p.e. une table)
• Tourner le bouton de réglage de l’intensité un peu enfin de creer un vide dans les électrodes
• Placer les électrodes à succion l’une apres l’autre de la surface lisse au corps du patient
• Ajuster l’intensité au valeur desiré
• Suivez les instructions du chapitre 10 sur la manière de régler les paramètres et de démarrer et
d'arrêter le traitement
• Si nécessaire, corriger la force de succion. Une force de succion faible est suffisante.
• Si nécessaire, sélectionnez le vide pulsé
Gardez les tampons éponges bien humidifiés (prêts à dégouliner lorsque vous les pressez
légèrement) pendant le traitement. Réhumidifiez-les si le traitement dure plus de 10 minutes.
Après utilisation, nettoyez les tampons éponges comme décrit à la section « Nettoyage et
désinfection ».
• Lorsque vous n'utilisez qu'un seul canal à vide, fermez l'autre canal avec un des câbles à vide
non utilisé.
Succion continue ou pulsée
En succion continue, la pompe arrête de fonctionner dès que la dépression ajustée est atteinte, ce
qui fait du Module de Vide un appareil silencieux. Un dispositif régulateur veille à la constance de la
dépression. La pompe sera activée brièvement durant le traitement pour maintenir la dépression au
niveau désiré.
En succion pulsée, la pompe est mise en marche/arrêt alternativement. Le rythme pulsé pour le
massage par succion peut être ajusté en continue ou pulsée (2 positions). La succion pulsée est très
appropriée pour les patients sensibles au courant, vu que la sensation du courant est plus ou moins
écartée.

Page 43 de 52 FR109-1634750-40 IFU
Densité du courant
Dans la norme IEC 60601-2-10 relative aux stimulateurs électriques de nerfs et de muscles, il est
recommandé de ne pas dépasser une densité de courant de 2 mA rms/cm², sous peine de
provoquer des irritations ou des attaques de la peau.
Pour trouver la densité de courant maximum recommandée en mA pour le Courant Interférentiel, il
faut multiplier la surface des électrodes en cm² par 2. Pour toutes les autres formes de courants
alternatifs la densité de courant ne doit jamais excéder 50 mA r.m.s. Ce qui implique qu’avec une
surface d’électrodes de 25 cm² la densité de courant ne doit jamais excéder 2 mA r.m.s. / cm². Par
principe, pour de plus petites électrodes, telles que les électrodes adhésives de diamètre 3,2 cm, le
courant maximum devrait proportionnellement être réduit.
Pour un calcul précis de la valeur r.m.s. d’un courant d’impulsions la formule suivante peut être
utilisée :
Notez que les électrodes doivent être placées avec soin, en assurant un bon contact électrique sur
toute la surface de l'électrode, et que l'utilisation de petites électrodes en combinaison avec des
intensités élevées peut provoquer des irritations ou des attaques de la peau.
Réactions au moment de la connexion/déconnexion
Les caractéristiques de la sortie de courant constant (CC) peuvent provoquer des réactions
désagréables au moment de la connexion/déconnexion si les électrodes ne sont pas bien placées
ou perdent le contact avec la peau. Assurez-vous que l'amplitude du courant est réglée sur 0 mA
lorsque vous appliquez ou retirez les électrodes.

Page 44 de 52 FR109-1634750-40 IFU
12 Maintenance et dépannage
Nettoyage et Désinfection
Nettoyez régulièrement l'appareil et ses accessoires afin de maintenir une sécurité hygiénique.
Avant de procéder à une tâche de maintenance utilisateur, mettez l'appareil hors tension et
débranchez-le de la prise secteur.
Ne pulvérisez pas l'agent nettoyant directement sur le panneau en verre.
N'utilisez pas d'agents nettoyants qui contiennent des alcalins forts, de la soude, de l'acide, ou
encore des détergents à base de fluorure ou d'ammoniac.
Ne laissez aucun liquide pénétrer dans l'appareil ou ses accessoires pendant le nettoyage et la
désinfection !
Avant toute nouvelle utilisation, séchez toutes les prises et tous les connecteurs qui sont
mouillés !
Les chocs mécaniques et/ou vibrations DOIVENT être évités lors du nettoyage de l'appareil.
Ne faites pas tomber l'appareil.
Appareil
Pour nettoyer l'appareil, éteignez-le et débranchez l'alimentation électrique.
Nettoyez l’appareil à l’aide d’un chiffon humidifié. N'utilisez pas de produits
nettoyants abrasifs. Une petite quantité de détergent ménager doux peut être
utilisée, si nécessaire.
L’écran
L’écran a un enduit anti-réfléchissant, qui nécessite un soin particulier. Employez
un tissu mou et sec de coton ou un tissu microfibre pour le nettoyage. Pour
enlever les empreintes digitales ou la graisse, employez un produit non-abrasif
pour le verre. Appliquez un peu du produit sur un tissu mou (coton) et nettoyez
soigneusement la face supérieure de l’appareil.
Électrodes,
porte-électrodes,
éponges et
accessoires
Entre chaque utilisation sur un patient, les électrodes en caoutchouc doivent
être nettoyées à l'eau tiède. Pour désinfecter les électrodes ou enlever les taches
tenaces de saleté, utilisez une solution d'alcool à 70 %. La solution d'alcool peut
tacher la couleur noire, mais cela n'affecte pas le fonctionnement des électrodes.
Entre chaque utilisation sur le patient, les tampons éponges doivent être lavés
sous l'eau du robinet, bien égouttés, puis séchés. Les tampons éponges
endommagés doivent être remplacés.
Il est recommandé de disposer d'une quantité suffisante d'éponges pour
permettre un séchage complet avant réutilisation, ce qui limitera la croissance
de bactéries d'origine hydrique.
Lorsque les électrodes ne sont pas utilisées, les éponges doivent être retirées.
Cela permet d'augmenter la durée de vie des électrodes en caoutchouc. Nous
vous conseillons de garder un jeu supplémentaire des éponges en stock.
L'électrode de masse vierge peut être nettoyée avec un chiffon humide.
Utilisez du savon et de l'eau tiède ou une solution alcoolisée.
Le porte-électrode peut être nettoyé avec un chiffon humide. Utilisez de l'eau
tiède et un produit de nettoyage ménager non abrasif et non invasif ou une
solution alcoolisée. Ne pas mettre dans un autoclave.

Page 45 de 52 FR109-1634750-40 IFU
Câble patient et
Câble de
référence CC
Nettoyez le câble patient avec un chiffon humide. Utilisez de l'eau tiède et un
produit de nettoyage ménager non abrasif. N'utilisez pas de solution alcoolisée.
Vérifiez régulièrement si le câble n'est pas endommagé et/ou si le contact
électrique n'est pas inadéquat. Nous vous conseillons de garder un câble patient
de rechange en stock.
Electrodes sous
vide et éponges
Les électrodes et les éponges devraient être nettoyées avec de l'eau tiède. En
cas de saleté persistante, et pour la désinfection, une solution d'alcool de 70%
peut être employée.
Les éponges devraient être remplacées régulièrement. Il est recommandé
d’avoir des éponges et des électrodes en stock.
Du tartre peut se déposer sur les surfaces en métal des électrodes. Ceci a un
effet isolant. Afin de maintenir une conductivité optimale, ces surfaces
devraient être régulièrement nettoyées et polies.
Câbles sous vide
Nettoyez le câble sous vide à l'aide d'un chiffon humide. N'utilisez pas une
solution à l'alcool. Vérifiez le câble régulièrement pour la présence de
dommages et/ou de mauvais contact électrique. Nous vous conseillons de
conserver un câble sous vide de réserve en stock.
Nettoyage du
réservoir et des
tuyaux d'eau
• Détachez les câbles des électrodes sous vide.
• Placez un conteneur rempli d'un liquide de nettoyage (*) sous le système.
• Enlevez les câbles des électrodes sous vide sous vide et placez les extrémités
des cables dans le conteneur.
• Allez dans Paramètres système et sélectionnez Nettoyage du réservoir.
• Le réservoir d'eau sera rempli du liquide de nettoyage jusqu'au remplissage
complet du réservoir d'eau.
• Videz le réservoir d'eau comme décrit au Réservoir d'eau plein.
(*) Les produits enregistrés suivants peuvent être utilisés pour désinfecter le réservoir d’eau :
BAKTONIL, BAKTOLAN à 5%, CHINOSOL à 1%, solution de CHLORAMIN, DETTOL, ELMOCID Gamma
à 2%, PERODIN, ZEPHIROL à 5%.
Observez les informations de application du fabricant correspondant.
Dépannage
L'appareil ne doit pas être utilisé lorsque des dommages mécaniques sont constatés. Cela
inclut les isolations de câble endommagées.
Si un message d'erreur ou un avertissement s'affiche, cessez immédiatement toute utilisation
de l'appareil. Arrêtez l’appareil et redémarrez-le. Si le problème persiste, contactez le
fournisseur ou Enraf-Nonius B.V. en vue d'une réparation. Des erreurs et des avertissements
indiquent un problème interne de l'appareil qui doit être testé par un technicien de terrain
agréé par Enraf-Nonius B.V. avant toute autre utilisation ou mise en service du système.
L'utilisation d'un dispositif qui indique une erreur ou un avertissement peut présenter un
risque de blessure pour le patient, l'utilisateur ou de dommages internes importants au
système.
En cas de panne de l'écran ou d'autres défauts évidents, débranchez immédiatement
l'appareil et contactez un technicien de maintenance agréé.
En cas de pénétration de liquides, débrancher l'appareil du réseau et le faire contrôler par une
personne autorisée.

Page 46 de 52 FR109-1634750-40 IFU
Messages d'erreur
Lorsque l'appareil est mis sous tension, il exécute d'abord un autotest. Lorsqu'une erreur est
détectée, tant pendant l'autotest que pendant le fonctionnement normal, un écran contextuel
s'affiche à l'écran. Lorsque l'erreur est affichée, toutes les sorties seront désactivées. Lorsque cette
situation se produit, éteignez l'appareil et débranchez tous les accessoires. Attendez environ 15
secondes et remettez l'appareil en marche.
Lorsque l'erreur réapparaît, arrêtez d'utiliser l'appareil et contactez le fournisseur.
L'appareil doit refroidir avant de pouvoir continuer
La température de l'appareil est trop élevée pour lancer le traitement. Éloignez l'appareil de toute
source de chaleur potentielle (par exemple, les rayons directs du soleil) et laissez-le refroidir.
Redémarrez l'appareil pour continuer.
Courant de sortie insuffisant ou inexistant
• Vérifiez que le câble du patient n'est pas coupé ou qu'il n'y a pas de mauvais contact.
• Assurez-vous que les éponges sont suffisamment humides
• Nettoyez les électrodes
• Vérifier les mauvais contacts
• Dans les régions où l'eau est douce, il est possible que l'eau soit mal conduite, ce qui entraîne
des courants anormalement faibles. Dans ce cas, il est possible d'utiliser une solution saline
pour améliorer la conductivité de l'eau.
Réservoir d'eau plein
Le réservoir de séparation d'eau du Module de Vide est plein. Continuez le traitement avec les
électrodes standard ou videz le réservoir comme suit :
• Placez le commutateur de la ligne électrique [17] sur Arrêt (0)
• Détachez le tuyau du raccord de tuyau supérieur [21] et videz le réservoir.
• Refixez le tuyau au raccord du tuyau.
• Placez le commutateur de la ligne électrique [17] sur Marche (1).
Fuite de vide
Il y a probablement un vide dans le système sous vide. Cette erreur est généralement précédée
d'une pompe continue essayant d'atteindre le vide défini. Pour protéger le système, la pompe est
automatiquement interrompue après un certain temps. Inspectez les câbles sous vide et les
électrodes, redéfinissez le vide à zéro et réessayez. Si la panne persiste, arrêtez d'utiliser l'appareil et
contactez votre fournisseur.

Page 47 de 52 FR109-1634750-40 IFU
Il est également recommandé de conserver un enregistrement de l'historique d'entretien. Dans
certains pays, c'est même obligatoire.
Sur demande, un manuel d'entretien peut être mis à disposition. Celui-ci contient : la liste des
pièces de rechange, les descriptions, les instructions d'étalonnage et d'autres informations qui
aideront le personnel technique qualifié de l'utilisateur à réparer les pièces de l'équipement qui
sont désignées par le fabricant comme réparables.
Durée de service prévue
Cet appareil restera adapté à l'usage auquel il est destiné aussi longtemps qu'il fera l'objet d'un
entretien annuel par un technicien qualifié, comme décrit dans le manuel d'entretien.
Le technicien d'entretien décidera si l'appareil peut être utilisé conformément aux spécifications.
Fin de vie
Votre Endomed 182 contient des matériaux recyclables et/ou nocifs pour l'environnement.
Entretien technique
L'ouverture de l'équipement par des organismes non agréés est interdite et entraînera la
nullité de la garantie.
Le fabricant ne peut pas être tenu responsable des conséquences d'un entretien ou de
réparations réalisés par une personne non habilitée.
Seuls les techniciens de service agréés par Enraf-Nonius peuvent effectuer l'entretien ou
modifier cet équipement conformément aux informations d'entretien.
Si cet équipement est modifié, une inspection et des tests appropriés doivent être effectués
pour garantir une utilisation sûre et continue de l'équipement.
Il est recommandé de faire contrôler chaque année l'Endomed 182 par le personnel autorisé
d'Enraf-Nonius ou par son distributeur agréé.
Veuillez vous assurer de détenir toutes les informations concernant les réglementations
locales inhérentes à la mise au rebut de l'équipement et de ses accessoires.

Page 48 de 52 FR109-1634750-40 IFU
13 Charactéristiques
Caractéristiques techniques
Informations relatives au raccordement électrique
Tension secteur
100 - 240 Volt
Fréquence
50/60 Hz
Entrée d'alimentation max.
50 VA
Dimensions (largeur x longueur x hauteur)
Endomed 182 Type 1
14.5 x 17 x 9 cm
Endomed 182 Type 2
14 x 16 x 14 cm
Endomed 182 Type 3
14 x 22,5 x 17,5 cm
Ces valeurs représentent les dimensions des boîtiers
sans câbles de communication, électrodes ou tuyaux.
Poids
Endomed 182 Type 1
710 grammes
Endomed 182 Type 2
1460 grammes
Endomed 182 Type 3
2750 grammes
Ces valeurs représentent le poids des boîtiers sans les
électrodes et les cordons d'alimentation.
Spécifications Type 1
Canaux
1
Sortie
Courant constant
Courant Continu
Polarité
Négatif
Intensité
0 – 15 mA
Durée de traitement
0 – 300 secondes
Spécificationss Type 2 et 3
Canaux
2
Sortie
Courant constant
Intensité
0 -100 mA
Durée
0 – 60 min (par étapes de 1 min)
Interférentiel bipolaire
Onde porteuse
4 kHz
Fréquence AMF
1 – 200 Hz
Fréquence de modulation
0 – 180 Hz
Programme de modulation
1-1, 6-6, 1-30 secondes
Interférentiel quadripolaire et vecteur isoplanaire
Onde porteuse
4 kHz
Fréquence AMF
1 – 200 Hz
Fréquence de modulation
0 – 180 Hz
Programme de modulation
1-1, 6-6, 1-30 secondes

Page 49 de 52 FR109-1634750-40 IFU
Courant pulsé biphasé asymétrique (TENS)
Largeur d'impulsion
150 μs
Fréquence
1 – 200 Hz
Fréquence de modulation
0 – 180 Hz
Programme de modulation
1-1, 6-6, 1-30 secondes
Fréquence de salves
1-2-4 Hz
Sous réserve de modifications techniques
Normes de sécurité et de performance
Catégorie de dispositif médical
IIa ; Règle 9 Annexe IX de 93/42/EEC
Cet appareil est conforme à toutes les exigences de la
Directive relative aux dispositifs médicaux (93/42/EEC).
Catégorie de sécurité selon la norme
IEC 60601-1
Classe de protection électrique I
Mode de fonctionnement
Continu
Pièces appliquées
Pièce appliquée de type BF pour l'électrothérapie.
Performance Essentielle
La performance essentielle est basée sur la norme 60601-2-10 où la sortie maximale de courant et
d'énergie pulsée est spécifiée. Compte tenu des différentes formes de thérapie, la performance
essentielle est construite à partir de cinq exigences :
1) Le courant efficace maximal de la TENS ne doit pas dépasser 50 mA.
2) Le courant interférentiel efficace maximal ne doit pas dépasser 100 mA.
3) L'énergie pulsée maximale de la TENS ne doit pas dépasser 300 mJ.
4) L'énergie pulsée interférentielle maximale ne doit pas dépasser 300 mJ.
5) Le courant continu efficace maximal ne doit pas dépasser 80 mA.
Les sorties d'électrothérapie ne doivent pas s'écarter de plus de 20 % de la valeur réglée.
Comme l'appareil est un système qui n'est pas vital, il peut tomber en panne en toute sécurité
(absence de sortie) et exiger l'intervention de l'opérateur pour redémarrer.
Conditions environnementales
Conditions environnementales pour le transport et le stockage
Température ambiante :
–20° à +70° C
Humidité relative :
10 à 90% (sans condensation)
Pression atmosphérique :
500 à 1060 hPa
Conditions environnementales en cas d'utilisation normale
Température ambiante :
10° à 40° C
Humidité relative :
10 à 90 % (sans condensation)
Pression atmosphérique :
800 à 1060 hPa

Page 50 de 52 FR109-1634750-40 IFU
Informations CEM
Les appareils électriques médicaux tels que l'Endomed 182 font l'objet de précautions
particulières au regard de la compatibilité électromagnétique (CEM) et doivent être installés et
mis en service conformément aux recommandations CEM figurant dans le mode d'emploi.
L'utilisation de cet équipement à proximité d'autres appareils ou leur empilement sont
déconseillés, car cela risque de provoquer des dysfonctionnements. Dans le cas où une telle
utilisation est nécessaire, cet équipement et les autres appareils doivent être vérifiés afin de
s'assurer qu'ils fonctionnent normalement.
L'utilisation d'accessoires, de transmetteurs et de câbles autres que ceux indiqués ou fournis
par le fabricant de cet équipement peut donner lieu à une augmentation des émissions
électromagnétiques ou une diminution de l'immunité électromagnétique de l'appareil et
entraîner un mauvais fonctionnement.
Les équipements de communication RF portables (y compris les périphériques tels que les
câbles d'antenne et les antennes externes) ne doivent pas être utilisés à moins de 30 cm des
composants de l'Endomed 182, y compris les câbles spécifiés par le fabricant. Sinon, les
performances de cet équipement pourraient se dégrader.
L'Endomed 182 ne doit être utilisé qu'avec le câble d'alimentation d'origine qui figure sur la
liste des éléments livrés. L'utilisation de l'appareil avec un autre câble d'alimentation peut
augmenter les émissions ou réduire son immunité aux interférences.
L'Endomed 182 est classé comme un dispositif du groupe 1, classe B, conformément à la norme
CISPR 11.
L'Endomed 182 est adapté à une utilisation dans un environnement professionnel de soins de
santé. L'appareil utilise l’énergie RF uniquement pour son fonctionnement interne. De ce fait, ses
émissions RF sont très faibles et ne sont pas susceptibles de provoquer des interférences avec les
équipements électroniques situés à proximité.
L'Endomed 182 a été testé selon la norme 60601-1-2 par un laboratoire accrédité et a été jugé
conforme à chaque norme ou essai relatifs aux émissions et à l'immunité.

Page 51 de 52 FR109-1634750-40 IFU
14 Contact
Pour toute assistance, nous vous invitons à vous rendre sur notre site Web http://www.enraf-
nonius.com
La dernière version (électronique ou imprimée) de ce mode d'emploi peut être obtenue
gratuitement sur notre site Web www.enraf-nonius.com, en contactant votre distributeur ou en
composant le numéro de téléphone suivant : +31-(0)10-2030600. Le mode d'emploi vous sera
envoyé (gratuitement) sous 7 (sept) jours calendaires.
15 Responsabilité du fait du produit
La plupart des pays ont instauré une législation sur la responsabilité du fait des produits. Cette
législation dispose, entre autres choses, qu'après un délai de 10 ans à compter de la mise en
circulation du produit, le fabricant ne peut plus être tenu responsable des potentiels défauts dudit
produit.
Dans toute la mesure autorisée par la loi applicable, Enraf-Nonius ou ses distributeurs ou
revendeurs ne peuvent, en aucun cas, être tenus responsables de tout dommage indirect, spécial,
accessoire ou consécutif résultant de l'utilisation ou de l'incapacité à utiliser le produit, y compris
sans limitation, les pertes de clientèle, de travail ou de productivité, les défaillances ou
dysfonctionnements informatiques, ou tout autre dommage ou perte de nature commerciale,
même si une telle éventualité a été évoquée, et indépendamment du fondement (contractuel,
délictuel ou autre) sur lequel repose la plainte. Dans tous les cas, la responsabilité globale d'Enraf-
Nonius en vertu des dispositions du présent contrat ne peut excéder la somme totale des montants
payés pour ce produit et pour l'assistance qui lui est associée en vertu d'un contrat d'assistance
séparé (s'il y a lieu), excepté en cas de décès ou de dommages corporels causés par la négligence
d'Enraf-Nonius dans la mesure où les lois applicables interdisent les limitations des dommages et
intérêts dans de telles situations.
La partie adverse (l'utilisateur du produit ou son représentant) est tenue de dégager Enraf-Nonius
de toute responsabilité à l'égard des réclamations provenant de tierces parties, quels que soient
leur nature ou leur lien avec la partie adverse.

FR109-1634750-40
Droits
d'auteur :
Enraf-Nonius B.V.
Vareseweg 127 | 3047 AT | Rotterdam | Pays-Bas
Tél: +31 (0)10-20 30 600 | [email protected]

Página 1 de 52 ES109-1634750-40 IFU
Endomed 182
ES109-1634750-40 IFU
El 21 de septiembre, 2020
Instrucciones de uso

Página 2 de 52 ES109-1634750-40 IFU
Indice
1 Introducción ...................................................................................................................................................... 3
2 Símbolos ............................................................................................................................................................. 7
3 Componentes del dispositivo ..................................................................................................................... 9
4 Contenido del embalaje ............................................................................................................................ 13
5 Instalación ....................................................................................................................................................... 15
6 Uso y usuario previstos .............................................................................................................................. 16
7 Indicaciones ................................................................................................................................................... 17
8 Contraindicaciones ...................................................................................................................................... 18
9 Instrucciones de precaución .................................................................................................................... 20
10 Funcionamiento ............................................................................................................................................ 23
11 Información de la aplicación.................................................................................................................... 37
12 Mantenimiento y solución de problemas ........................................................................................... 43
13 Especificaciones ............................................................................................................................................ 47
14 Contacto .......................................................................................................................................................... 50
15 Responsabilidad del producto ................................................................................................................ 50

Página 3 de 52 ES109-1634750-40 IFU
1 Introducción
Prefacio
Nos complace que haya comprado un Endomed 182.
Endomed 182, diseñado y fabricado por Enraf-Nonius B.V., aporta una nueva dimensión en
electroterapia gracias a su avanzado diseño de hardware y software. El resultado es un dispositivo
con una extraordinaria versatilidad basada en la facilidad de manejo.
Este manual ha sido redactado para los propietarios y operadores de Endomed 182. Para maximizar
el uso, la eficiencia y la duración de su unidad, lea detenidamente este manual y familiarícese con
los controles y los accesorios antes de utilizar el dispositivo.
Descripción del dispositivo
El Endomed 182 es un electroestimulador que se conecta a la red y viene equipado con una
pantalla táctil a todo color. La interfaz gráfica de usuario permite al operador trabajar con la
máxima comodidad.
Hay tres versiones disponibles del Endomed 182:
El Endomed 182 de tipo 1 es un electroestimulador monocanal que se conecta a la red para la
aplicación de electrólisis percutánea (EP) mediante corriente directa (CD) de baja intensidad.
Endomed 182 versiones
Nombre:
Endomed 182 Tipo 1
Endomed 182 Tipo 2
Endomed 182 Tipo 3
número de
artículo:
1634903
1634901
1634902
número de
artículo unidad
base:
1634910
1634900
1634900
Forma de onda
de la corriente:
Corriente directa
TENS
• corriente continua bifásica
pulsada (modo TENS
convencional)
• trenes de corriente pulsada
bifásica (modo Burst TENS)
Corriente Interferencial (IFC)
• Interferencial de 2 polos
modo (bipolar)
• Interferencial de 4 polos
modo (tetrapolar)
• Interferencial de 4 polos
(tetrapolar) con el vector
isoplanar
TENS
• corriente continua bifásica
pulsada (modo TENS
convencional)
• trenes de corriente pulsada
bifásica (modo Burst TENS)
Corriente Interferencial (IFC)
• Interferencial de 2 polos
modo (bipolar)
• Interferencial de 4 polos
modo (tetrapolar)
• Interferencial de 4 polos
(tetrapolar) con el vector
isoplanar
Vacío
Canales:
1
2
2
Protocolos de
tratamiento
preprogramados:
-
16
16

Página 4 de 52 ES109-1634750-40 IFU
En la EP, la corriente directa (también denominada corriente galvánica) se aplica a través de una aguja
que se coloca en el portaagujas de una pieza de mano (el «aplicador» o cátodo). El electrodo de
retorno (o ánodo) es un electrodo de mano (que sostiene el paciente) u otra aguja, dependiendo del
tratamiento que se vaya a realizar.
El portaagujas del aplicador (pieza de mano) permite acoplar agujas de acupuntura (estériles, de un
solo uso y desechables) de distintos diámetros y longitudes, lo cual es necesario para asegurar una
correcta colocación en distintas zonas (según el trastorno que vaya a tratarse).
La pieza de mano lleva un botón de iniciar/detener con el cual iniciar o interrumpir manualmente el
flujo de corriente.
El dispositivo emite una corriente galvánica continua con una salida máxima de 15 mA.
La interfaz gráfica de usuario muestra los siguientes parámetros del tratamiento: nivel de salida de la
corriente (mA), hora establecida para la aplicación, corriente real emitida (mC).
El usuario puede configurar y ajustar el nivel de salida de la corriente (mA) y el tiempo de aplicación,
dependiendo del tipo de tratamiento.
El dispositivo no ofrece ningún protocolo clínico preconfigurado, pero todos los parámetros de
tratamiento pueden ajustarse y guardarse como favoritos (configuración personalizada) como
referencia para futuras sesiones de terapia.
El dispositivo es una unidad compacta que lleva los siguientes accesorios: cables de alimentación y
de conexión, pieza de mano (aplicador), electrodo de retorno, pedal (opcional) y documentación del
producto. Los consumibles como las agujas (de acupuntura) desechables no se suministran con el
producto.
Enraf-Nonius B.V. no suministra electrodos percutáneos ni agujas de acupuntura desechables.
Los Endomed 182 de tipos 2 y 3 incluyen 16 protocolos clínicos preconfigurados para TENS y
corrientes interferenciales. El operador también puede introducir manualmente y ajustar los
parámetros de tratamiento individuales. Todos los parámetros de tratamiento pueden ajustarse y
guardarse como favoritos (configuración personalizada) como referencia para futuras sesiones de
terapia.
El Endomed 182 de tipo 3 es una configuración apilada que consta de un módulo de succión por
vacío independiente y un electroestimulador Endomed 182 de tipo 2. El módulo de vacío se coloca
bajo el estimulador y se conecta a este. El objetivo del módulo es generar un vacío que permite al
terapeuta adherir (fijar) rápido y con (mayor) facilidad los electrodos de estimulación al paciente. La
fijación se logra mediante el uso de ventosas. Las ventosas tienen superficies de estimulación
integradas que transfieren la electroestimulación al tejido objetivo a través de esponjas
humedecidas.
Con los Endomed 182 de tipos 2 y 3, por tanto, la estimulación eléctrica puede aplicarse a la piel
mediante los electrodos de superficie: electrodos flexibles de goma, electrodos autoadhesivos o
electrodos de vacío (sólo tipo 3), a fin de estimular tipos específicos de fibras nerviosas. Enraf-
Nonius dispone de electrodos de varios tipos y tamaños (desde electrodos de punta cuya superficie
es de 0,3 cm2 a electrodos cuya superficie es de 96 cm2) para adaptarse a las dimensiones del área
tratada o al objetivo esperado del tratamiento.

Página 5 de 52 ES109-1634750-40 IFU
Descripción de la onda de corriente
TENS (Corrientes bifásicas pulsadas)
La forma de corriente de onda pulsada bifásica asimétrica a menudo se usa en aplicaciones del
TENS (Estimulación Eléctrica Transcutánea del Nervio). Esta forma de onda se caracteriza por la
duración de fase variable y la frecuencia de pulso variable. La amplitud típica, duración y tasa de
incremento y declive son desiguales para cada fase con respecto a la línea de base. La onda de
corriente está totalmente en equilibrio i.e. las cargas para cada fase son iguales. La naturaleza
bifásica del pulso implica que no hay un componente neto de corriente continua (la corriente
continua neta es nula), minimizando así posibles reacciones cutáneas por la acumulación de
electrolitos bajo los electrodos.
Para evitar el acomodo a la estimulación o
mejorar la tolerancia del paciente, la frecuencia de
pulso puede ser variada a través de la modulación
de frecuencia.
Forma de onda bifásica asimétrica TENS
Burst TENS
La Burst TENS se aplica si la TENS convencional demuestra ser ineficaz, y es especialmente apta
para el tratamiento de regiones dolorosas más profundas y casos de dolor crónico. La Burst TENS
emplea una duración de fase relativamente larga (150-200 μs), una frecuencia de ráfagas baja (1-5
Hz) y una frecuencia elevada.
En los músculos cuya inervación corresponde a la de la región dolorosa deberían darse
contracciones fuertes y visibles.
El efecto reductor del dolor generalmente no aparece hasta pasados entre veinte y treinta minutos,
a diferencia de la TENS convencional, en la que suele aparecer bastante rápido. Sin embargo, el
efecto tiene una duración considerablemente mayor que el de la TENS convencional una vez
finalizada la estimulación. El efecto reductor del dolor de la Burst TENS se debe a la liberación de
endorfinas a nivel espinal y supraespinal.
Si la TENS convencional o Burst TENS no alivian lo suficiente o en absoluto, se puede emplear la
modulación de frecuencia. La modulación de frecuencia también puede prevenir la acomodación.
Corriente Interferencial (IFC)
Con la corriente de tipo interferencial se usa una frecuencia portadora de frecuencia media para
pasar la estimulación de baja frecuencia (pulso) a través de la piel. La relativamente baja resistencia
de la piel a la frecuencia portadora contribuye a la comodidad del paciente que es a menudo
asociada con este tipo de corriente. Las corrientes interferenciales son todas las corrientes AC sin
ningún componente residual DC. Son conocidas varias variaciones de corriente interferencial, están
disponibles en el Endomed 182 Tipo 2 y 3: 2 polos, 4 polos y 4 polos con vector isoplanar.
El método de los dos polos
En este método se utilizan dos electrodos y la
superposición de las dos corrientes alternas tiene lugar
dentro del equipo. La corriente que sale del equipo es
una corriente alterna totalmente modulada. En el
método de dos polos la profundidad de modulación es
siempre del 100%.
La terapia de interferencia bipolar

Página 6 de 52 ES109-1634750-40 IFU
El método de los cuatro polos (Inteferencial clásica)
Con este método de terapia se usan cuatro electrodos
y se generan dos corrientes no moduladas. La
frecuencia de un canal se fija en la frecuencia
portadora, mientras que el otro canal tiene una
frecuencia variable, basada en pruebas de la Frecuencia
de Pulso y Modulación de Frecuencia. La interferencia
ocurre en la intersección de las dos corrientes en el
tejido. La profundidad de modulación (que determina
la amplitud de corriente de la estimulación) depende
de la dirección de las corrientes, y puede variar desde 0
a 100%. El 100% de frecuencia de modulación
solamente ocurre en las diagonales (y por lo tanto en la
intersección) de las dos corrientes. Esto es por
supuesto una situación teórica, basada en la suposición
de que el tejido fuera homogéneo. En realidad, el
tejido es heterogéneo, de esta manera el balance de
corriente entre los dos canales tiene que ser usado
hasta llegar a conseguir el 100% de profundidad de
modulación. El balance de corriente también se usa
para compensar diferencias de sensación que ocurran
bajo el par de electrodos.
En el método de cuatro polos, la
profundidad de modulación es sólo del
100% en las diagonales.
El método de cuatro polos con el vector isoplanar
Con el vector isoplanar el área total entre los 4
electrodos es estimulada de manera óptima. El
posicionamiento de los electrodos puede hacerse de
forma sencilla y rápida. La profundidad de modulación
es del 100% en todas partes.
El Vector Isoplanar puede ser utilizado para el
tratamiento de problemas que se encuentran en una
gran área y que son muy difíciles de localizar. La
interferencia isoplanar también se utiliza como un
pretratamiento suave. Después de esta aplicación el
tratamiento se continúa con un enfoque en un área
más pequeña y más local.
Vector isoplanar
Corriente directa
Una corriente directa (CD) o corriente galvánica es una corriente continua que se utiliza en medicina
con una serie de objetivos terapéuticos. La corriente continua se refiere al flujo continuo de una
carga eléctrica a través de un conductor de corriente entre dos puntos (electrodos) con distintos
potenciales (polaridad), la cual no cambia de dirección con el tiempo. Al contrario que las corrientes
alternas, las cargas eléctricas siempre fluyen en el mismo sentido.

Página 7 de 52 ES109-1634750-40 IFU
2 Símbolos
Símbolo
Descripción
Siga las instrucciones de las instrucciones de uso.
Es importante que lea, entienda y respete las instrucciones de precaución y de
funcionamiento.
Señal de prohibición general.
La señal de prohibido quiere decir que «NO DEBE...».
Advertencia o precaución:
Indica una situación peligrosa que, si no se evita, podría provocar:
a. La muerte o una lesión grave al paciente (o)
b. Lesiones de leves a moderadas al paciente (o)
c. Daños en el equipo
Señal de acción obligatoria general.
La acción obligatoria quiere decir que «Debe...».
Pieza aplicada de tipo BF conforme con todos los requisitos estipulados para
ofrecer un mayor grado de protección contra descargas eléctricas que las
piezas aplicadas de tipo B.
Límites de temperatura
Indica el rango de temperatura aceptable.
Límites de humedad
Indica el rango de humedad relativa aceptable.
Límites de presión atmosférica
Indica el rango de presión atmosférica al que se puede exponer el producto
sanitario con seguridad.
Deseche los artículos eléctricos que se puedan reciclar.
Indica que los componentes eléctricos y electrónicos del dispositivo pueden
reciclarse y deben desecharse por separado.
Mantenga seco el producto.
Nombre del fabricante, dirección y fecha de fabricación.
Número de referencia o número de pieza.
Indica el número de serie del fabricante para que sea posible identificar un
producto médico específico.
Corriente alterna

Página 8 de 52 ES109-1634750-40 IFU
Conexión electroterapia cable electrodo
Conexiones de vacío cables electroterapia
“ENCENDIDO” (poder)
“APAGADO” (poder)
La marca CE junto con el número denota la conformidad con la directiva del
Consejo Europeo sobre productos sanitarios e indica que este producto está
bajo la supervisión directa del cuerpo notificado.

Página 9 de 52 ES109-1634750-40 IFU
3 Componentes del dispositivo
Endomed 182 Tipo 1
Endomed 182 Tipo 2
7
8
1
9
1
2
1
3
1
1
4
1
6
1
5
1
10
11

Página 10 de 52 ES109-1634750-40 IFU
Endomed 182 Tipo 3
12
13
16
15
14
17
18
19
21
20

Página 11 de 52 ES109-1634750-40 IFU
Descripción de las piezas
Pieza
numerada
Descripción
Función
[1]
Pantalla táctil LCD
Display en color TFT de 4.3” con pantalla táctil.
Interfaz de usuario que permite al operador
controlar el dispositivo y cambiar los parámetros
de los protocolos de tratamiento.
[2]
Conexión Portaelectrodos
Conexión para el Portaelectrodos
[3]
Conexión del Electrodo de
masa blanco
Conexión para el Cable de referencia de la CD que
se conecta al electrodo de masa blanco
[4]
Electrodo de masa blanco
Electrodo de referencia
[5]
Cable de referencia de la CD
Cable de conexión del electrodo de masa blanco
[6]
Portaelectrodos
Pieza de mano para el porta agujas
[7]
Conexión A
Conexión para el Módulo de vacío (Endomed 182
Tipo 3 / Interruptor de pie (Endomed 182 Tipo 1)
[8]
Conexión B
Conexión para el Módulo de corriente
[9]
Módulo de corriente
Módulo de corriente con conexión para electrodos
adhesivos y de goma.
[10]
Conexión 1 Módulo de
corriente
Canal de conexión 1 para el cable del paciente para
electrodos adhesivos o de goma en el Módulo de
corriente Endomed 182.
[11]
Conexión 2 Módulo de
corriente
Canal de conexión 2 para el cable del paciente para
electrodos adhesivos o de goma en el módulo de
corriente Endomed 182.
[12]
Portaelectrodos de vacío
Soporte para electrodos de vacío.
[13]
Módulo de vacío
Módulo de vacío integrado con Endomed 182 con
conexiones para electrodos adhesivos o de goma y
electrodos de vacío.
[14]
Cables de electrodos del
Módulo de vacío
Los cables de electrodos del Módulo de vacío
deben ser conectados a la conexión del Módulo de
corriente [7] y [8] para el correcto funcionamiento
de las conexiones del Módulo de vacío.
[15]
Conexiones superiores Módulo
de vacío
Conexiones de los canales 1 y 2 para el cable del
paciente para los electrodos adhesivos o de goma
en el Módulo de vacío.
[16]
Conexiones inferiores Módulo
de vacío
Conexiones de los canales 1 y 2 para la manguera
de vacío para los electrodos de vacío en el módulo
de vacío.
[17]
Interruptor de red eléctrica
Para apagar y encender la Unidad.
Cuando apagar la exhibición sigue siendo visible
por algunos segundos (método de poca energía).
[18]
Tipo y número
Se proporciona información del Equipo, tipo de
aparato y número de serie
[19]
Conector para cable de red
Conecte el cable de red eléctrica suministrado aquí
para alimentar el dispositivo.
[20]
Salida de aire
Salida de aire para el Módulo de vacío.

Página 12 de 52 ES109-1634750-40 IFU
Descripción de las piezas
Pieza
numerada
Descripción
Función
[21]
Conexión para el depósito de
agua
Esta conexión se utiliza para conectar el depósito
de agua. No se puede crear un vacío a menos que
el depósito de agua esté conectado. El depósito de
agua asegura que cualquier exceso de agua de las
esponjas se recoja y no pueda ser expulsada a
través de la bomba. El depósito debe vaciarse
diariamente. Por favor, consulte la sección de
Mantenimiento.

Página 13 de 52 ES109-1634750-40 IFU
4 Contenido del embalaje
Dispositivo
El contenido del paquete depende del modelo de aparato pedido. Los siguientes modelos están
disponibles:
Número de art.
Descripción
1634903
Endomed 182 Tipo 1
1634901
Endomed 182 Tipo 2
1634902
Endomed 182 Tipo 3 (incluye un Módulo de vacío integrado)
Accesorios estándar Endomed 182 Tipo 1
1634750
CD-ROM con Instrucciones de uso (PDF en CD-ROM)
1634751
Folleto informativo
3444357
Cable de alimentación de 250V/2,5A, 2,5 metros negro
3444080
Portaelectrodos
3444582
Electrodo de masa blanco
3444677
Cable de referencia de la CD
Accesorios estándar Endomed 182 Tipo 2 y Endomed 182 Tipo 3
1634750
CD-ROM con Instrucciones de uso (PDF en CD-ROM)
1634751
Folleto informativo
3444357
Cable de alimentación de 250V/2,5A, 2,5 metros negro
3444021
Cincha de fijación 250x3 cm
3444020
Cincha de fijación 100x3 cm
3444129
(2x) Electrodos de caucho 6x8 cm, 2 mm hembra, juego de 2
1460266
Almohadillas húmedas para electrodos de 6x8 cm, juego de 4
3444211
(2x) Cavo paziente 2 mm maschio di contatto negro, con clips de colores
Accesorios estándar adicionales Endomed 182 Tipo 3
3444503
(2x) Electrodos de vacío Ø 60 mm, juego de 2x
3444505
Esponjas Ø 65 mm, juego de 4 (para electrodos de vacio Ø 60 mm)
3444507
(2x) Cable de electrodo de vacío rojo
3444508
(2x) Cable de electrodo de vacío negro
Accesorios opcionales Endomed 182 Tipo 1
1634810
Interruptor de pie
Accesorios opcionales Endomed 182 Tipo 2 y Endomed 182 Tipo 3
Electrodos adhesivos
3444056
EN-Trode Ø 3,2 cm, 2 mm hembra, 10 envases de 4
3444135
EN-Trode Ø 5,0 cm, 2 mm hembra, 10 envases de 4
3444057
EN-Trode 5x5 cm, 2 mm hembra, 10 envases de 4
3444058
EN-Trode 5x9 cm, 2 mm hembra, 10 envases de 4
3444222
Electrodos adhesivos Ø 2,0 cm, 2 mm hembra, 10 envases de 8
Electrodos de caucho
3444128
Electrodos de caucho 4x6 cm, 2 mm hembra, 2x
3444129
Electrodos de caucho 6x8 cm, 2 mm hembra, 2x
3444130
Electrodos de caucho 8x12 cm, 2 mm hembra, 2x
3444380
Electrodo de silicona 5x5 cm

Página 14 de 52 ES109-1634750-40 IFU
Almohadillas húmedas para electrodos
1460273
Almohadillas húmedas para electrodos de 4x6 cm, 4x
1460266
Almohadillas húmedas para electrodos de 6x8 cm, 4x
1460275
Almohadillas húmedas para electrodos de 8x12 cm, 4x
Banda de fijación
3444020
Banda de fijación 100x3 cm
3444021
Banda de fijación 250x3 cm
3444022
Banda de fijación 100x5 cm
3444023
Banda de fijación 250x5 cm
Electrodos puntiagudo
3444180
Electrodo puntiagudo (Modelo de Bolígrafo), Ø 5 mm, 2mm hembra, incluye 10
tapas de goma conductora
Adaptador
2523523
Adaptador de 4 mm macho a 2 mm hembra, negro
2523524
Adaptador de 4 mm macho a 2 mm hembra, rojo
Cable de paciente
3444211
Cable de paciente 2 mm macho - negro, con clips de colores
Accesorios opcionales adicionales Endomed 182 Tipo 3
Vacuum electrodes
3444503
Electrodos de vacío Ø 60 mm, juego de 2
3444504
Electrodo de vacio, Ø 90 mm, juego de 2
3444509
Electrodos de vacío Ø 30 mm, juego de 2
Esponjas
3444505
Esponjas Ø 65 mm, juego de 4 (para electrodos de vacio Ø 60 mm)
3444506
Esponjas Ø 95 mm, juego de 4 (para electrodo de vacio Ø 90 mm)
3444516
Esponjas Ø 30 mm, juego de 4 (para electrodos de vacio Ø 30 mm)
Cable de electrodo de vacio
3444507
Cable de electrodo de vacio negro, con enchufes rojo
3444508
Cable de electrodo de vacio negro, con enchufes negro
Información sobre pedidos
Para los datos de pedido del Endomed 182, los accesorios estándar y los accesorios adicionales,
consulte la página web www.enraf-nonius.com.

Página 15 de 52 ES109-1634750-40 IFU
5 Instalación
Inspección
En caso de observar daños por el transporte, contacte con su distribuidor local.
¡NO UTILICE el dispositivo!
La unidad debe instalarse de forma que el calor pueda disiparse en el entorno.
Inmediatamente después de desembalar la unidad, realice los siguientes pasos:
• Revise los documentos de entrega para comprobar que la entrega esté completa.
• Compruebe que el paquete contiene todos los elementos indicados en la lista de accesorios
estándar (ver el capítulo 4 Contenido del embalaje en estas Instrucciones de uso).
• Compruebe los componentes externos y accesorios en busca de posibles daños debidos al
transporte.
Desembalaje
El equipo Endomed 182 está especialmente embalado para su transporte en un solo paquete
completo con relleno, que ha sido diseñado específicamente para un transporte y almacenamiento
seguros.
• Para sacar el equipo del paquete, coloque la caja sobre una superficie lisa y plana.
• Abra la parte superior de la caja y retire el relleno de poliestireno.
• Tenga mucho cuidado al extraer el contenido del paquete.
Configuración del dispositivo
Endomed 182 Tipo 2:
• Conecta el cable del Módulo de corriente [9] al Conector B [8].
Endomed 182 Tipo 3:
• Conecta el cable del Módulo de Corriente [9] al Conector B [8].
• Conecte el cable del Módulo de Vacío [13] al Conector A [7].
Consulte el capítulo 3 - Componentes del dispositivo en este manual.
Conexión a la red eléctrica
El uso de cualquier otro cable distinto del suministrado está estrictamente PROHIBIDO ya que
afecta a la seguridad de los pacientes y al correcto funcionamiento del dispositivo.
Antes de conectar esta unidad a la red eléctrica, verifique que la tensión y la frecuencia
indicadas en la placa de características del dispositivo se corresponden con las de la red
eléctrica.
Para evitar el riesgo de descarga eléctrica, este equipo sólo debe conectarse a una red de
suministro con tierra protegida.
Conecte el dispositivo a un enchufe usando el cable de alimentación.
• Conecte el cable de alimentación al dispositivo [19] y a un enchufe.
Desconexión de la red eléctrica
• Cuando termine el tratamiento, apague el dispositivo poniendo el interruptor de red en «Off».
El dispositivo quedará desconectado de la red eléctrica.
• Desconecte el cable de red de la toma de corriente.
• Desconecte el cable de red del enchufe [19].

Página 16 de 52 ES109-1634750-40 IFU
6 Uso y usuario previstos
Uso previsto
Endomed 182 Tipo 1
El Endomed 182 de tipo 1 es un electroestimulador monocanal, previsto y diseñado para que lo
utilicen los profesionales sanitarios para realizar la electrólisis percutánea (EP) mediante corriente
directa (CD) de baja intensidad.
Endomed 182 Type 2 and 3
Endomed 182 Tipo 2 y 3 son equipo de estimulación eléctrica de 2 canales, diseñado para el uso por
profesionales sanitarios, que posibilita terapias de electroestimulación para el tratamiento del dolor
con corriente IFC (corriente interferencial) y corriente TENS.
El tratamiento del dolor mediante electroestimulación incluye:
- Alivio sintomático de dolor crónico incurable
- Tratamiento del dolor asociado a estados postraumáticos o posoperativos
- Alivio del dolor asociado a la artritis
La estimulación eléctrica se aplica en la piel mediante electrodos superficiales (TENS) o electrodos
percutáneos (PENS) con el objetivo de estimular tipos específicos de fibras nerviosas. El alivio
(modulación) del dolor puede lograrse:
1. bloqueando la información que viaja por las fibras nociceptivas (es decir, las que producen
dolor) mediante la estimulación de las fibras aferentes A de gran diámetro
2. a través de la secreción de opioides endógenos del cuerpo mediante la estimulación de las
fibras aferentes de pequeño diámetro y las motoras
Usuario previsto
El Endomed 182 está destinado a ser utilizado, y sólo será utilizado, por o bajo la supervisión de
usuarios profesionales en el campo de la medicina física y la rehabilitación en centros de salud
profesionales.
Adicionalmente para el Endomed 182 Tipo 1:
Si un profesional sanitario (fisioterapeuta, médico) está facultado y formado para administrar la
terapia de electrólisis galvánica guiada por ecografía, el profesional sanitario está facultado y
formado para:
-> realizar punciones con agujas a un paciente;
-> utilizar la ecografía;
-> administrar la terapia de electrólisis galvánica.

Página 17 de 52 ES109-1634750-40 IFU
7 Indicaciones
Indicaciones Endomed 182 Tipo 1
Electrólisis percutánea
La electrólisis percutánea (EP) puede utilizarse para tratar las siguientes afecciones:
• Tendinopatía rotuliana/tendinitis rotuliana («rodilla de saltador»)
• Tendinopatía lateral del codo («codo de tenista»)
• Tendinopatía medial del codo («codo de golfista»)
• Síndrome de dolor miofascial/puntos gatillo
• Síndrome del latigazo cervical (SLC)
• Trastornos del hombro (tendinopatías del manguito de los rotadores, síndrome de dolor
subacromial)
• Pubalgia (dolor en la ingle)
• Tendinopatía en la corva
• Tendinopatía aquílea
• Fascitis plantar/dolor en el talón
Indicaciones Endomed 182 Tipo 2 y 3
TENS
Alivio del dolor agudo
• Dolor posoperatorio
o Abdominal
o Torácico
o Dolor ortopédico posoperatorio
• Dolor en el parto y el posparto
• Dismenorrea
• Dolor orofacial, incluidas intervenciones dentales
• Trauma físico, incluidas fracturas de costillas e intervenciones médicas menores
Alivio del dolor crónico
• Dolor lumbar
• Dolor artrítico, incluidas osteoartritis y artritis reumatoide
• Dolor muscular, incluidos dolor miofascial, tensión muscular y molestias tras el ejercicio
• Dolor neuropático, incluido dolor tras una amputación (dolor fantasma), neuralgia
posherpética, neuralgia trigeminal
• Dolor por cáncer, incluido el dolor óseo metastásico
• Síndrome de dolor regional complejo
Corriente Interferencial (IFC)
Alivio del dolor agudo y crónico, como:
• Dolor posoperatorio / Dolor ortopédico
• Dolor lumbar
• Dolor de cuello
• Dolor de hombre
• Dolor artrítico, incluidas osteoartritis y artritis reumatoide
• olor muscular, incluidos dolor miofascial, tensión muscular y molestias tras el ejercicio, y
fibromialgia
Estimulación muscular
• Fortalecimiento muscular (en general)
• Incontinencia fecal y urinaria
Disfunción intestinal
Aumento del flujo sanguíneo (cutáneo) local

Página 18 de 52 ES109-1634750-40 IFU
8 Contraindicaciones
El Endomed 182 NO DEBE utilizarse para los síntomas o afecciones médicas que se
mencionan a continuación.
Contraindicaciones Endomed 182 Tipo 1
Contraindicaciones de uso
• Artritis infecciosa
• Cardiopatía/arritmia cardíaca
• Mujeres embarazadas
• Úlceras en la piel y otras infecciones cutáneas
• Endoprótesis y/u osteosíntesis
• Marcapasos
• Procesos oncológicos
• Tromboflebitis/antecedentes de insuficiencia vascular en las piernas
• Coagulopatía/fármacos anticoagulantes
• Discrasia sanguínea
• Menstruación
• Fobia a las agujas
• Miedo a la estimulación eléctrica
• Glándulas endocrinas
• Pacientes con deficiencias de la sensibilidad
• Pacientes con trastornos neurológicos centrales y periféricos
• Pacientes con trastornos neurovegetativos
• Pacientes pediátricos
• Afecciones médicas complicadas
• Deficiencia cognitiva
• Drogadicción o alcoholismo
Puntos en los que no deben aplicarse tratamientos:
• Vasos sanguíneos
• Glándulas endocrinas
• Órganos
• Nervios periféricos (endoneuro)
• Cabeza, ojos, cuello y tórax o parte superior de la espalda atravesando el corazón
Precauciones de la electrólisis percutánea
Zonas que requieren especial precaución:
• Región abdominal
• Región intercostal (precaución frente al neumotórax)
• Región torácica (precaución frente al neumotórax)
• Salida torácica (precaución frente al neumotórax)
• Región inguinal, fosa poplítea (precaución para no dañar los haces neurovasculares)

Página 19 de 52 ES109-1634750-40 IFU
Contraindicaciones Endomed 182 Tipo 2 y 3
Contraindicaciones absolutas:
• Dolor no diagnosticado
• Implantes activos (incl. marcapasos y desfibriladores automáticos implantables (DAI))
• Hemorragia
• Pacientes que no entienden las instrucciones del médico/fisioterapeuta o son incapaces de
cooperar
Contraindicaciones relativas (= contraindicaciones locales)
• Embarazo (no aplicar en ningún punto de la región abdominal/pélvica)
• Neoplasia (no aplicar sobre una neoplasia activa)
• Epilepsia (no aplicar en el cuello o la cabeza)
• Trastornos cardiacos como arritmias (no aplicar a través del pecho)
• Colocación de electrodos alrededor de los ojos
• Colocación de electrodos en la parte anterior del cuello o seno carotídeo
• Colocación de electrodos a través del pecho (p. ej. posiciones de electrodos anterior y
posterior)
• Colocación de electrodos en los testículos
• Colocación de electrodos en regiones epifisarias activas en niños
• Colocación de electrodos sobre piel dañada o heridas abiertas
• Colocación de electrodos sobre lesiones dermatológicas, p. ej. dermatitis, eccemas o en piel
delicada
• Colocación de electrodos en zonas con tejido isquémico y/o trombosis
Nota: no se conocen efectos adversos por administrar TENS / IFC en la piel situada sobre o cerca de
implantes metálicos. La TENS / IFC puede emplearse sobre la piel intacta que cubre implantes que
contienen metal, plástico o cemento. Las personas sometidas a artroplastias que incluyen
componentes metálicos han recibido tratamientos de electroestimulación con beneficios y sin
reacciones adversas.
Precauciones TENS y Corriente Interferencial (IFC)
Debe ponerse especial cuidado y atención en caso de:
• Zonas con percepción táctil anormal (disestesia)
o Hiperestesia (alodinia / hiperalgesia)
o Hipoestesia
• Dermatitis de contacto
• Mujeres embarazadas
• Pacientes sensibles a reacciones involuntarias de TENS (p. ej. náusea, mareo leve y desmayo)
Efectos adversos potenciales
Se ha informado de la aparición de irritación y marcas cutáneas en la zona de aplicación de los
electrodos con el uso de la estimulación eléctrica terapéutica.
Pueden darse casos aislados de irritación cutánea en pacientes con pieles especialmente sensibles.
En caso de reacción alérgica al gel de los electrodos, se debe suspender el tratamiento y consultar a
un especialista. Si aparecen señales de taquicardia y extrasistolia durante el tratamiento, se debe
suspender el tratamiento y consultar al médico.

Página 20 de 52 ES109-1634750-40 IFU
9 Instrucciones de precaución
Si el uso de este dispositivo provoca o contribuye a la presencia de un suceso no
deseado, como la muerte o lesiones graves del usuario, DEBE informarse de inmediato al
fabricante Y TAMBIÉN a las autoridades competentes del Estado miembro.
Este dispositivo debe mantenerse fuera del alcance de los niños.
El paciente y el dispositivo deben permanecer a la vista del terapeuta en todo momento.
No utilice este dispositivo en las llamadas «salas húmedas» (salas de hidroterapia).
Este equipo no debe utilizarse en presencia de una mezcla de anestésicos inflamables con
aire, oxígeno u óxido nitroso.
No exponga el dispositivo a la luz solar directa, el calor irradiado por un radiador, cantidades
excesivas de polvo, humedad, vibraciones o golpes mecánicos.
Este dispositivo solo debe utilizarse bajo la supervisión continua de un médico o sanitario
con licencia.
En caso de observar daños por el transporte, contacte con su distribuidor local.
¡NO UTILICE el dispositivo!
La unidad debe instalarse de forma que el calor pueda disiparse en el entorno.
El uso de cualquier otro cable distinto del suministrado está estrictamente PROHIBIDO ya que
afecta a la seguridad de los pacientes y al correcto funcionamiento del dispositivo.
Antes de conectar esta unidad a la red eléctrica, verifique que la tensión y la frecuencia
indicadas en la placa de características del dispositivo se corresponden con las de la red
eléctrica.
Para evitar el riesgo de descarga eléctrica, este equipo sólo debe conectarse a una red de
suministro con tierra protegida.
No utilice el dispositivo después de fluctuaciones extremas de temperatura.
Antes de comenzar el tratamiento, por favor asegúrese: Ha leído y comprendido el contenido
de este manual.
Antes de comenzar el tratamiento, por favor asegúrese: Respeta rigurosamente las
ADVERTENCIAS y PRECAUCIONES mencionadas en la sección de «Instrucciones de
precaución».
Antes de comenzar el tratamiento, por favor asegúrese: Ha comprobado si el paciente presenta
posibles contraindicaciones.
La conexión de accesorios distintos a los especificados por el fabricante puede afectar
negativamente a la seguridad del paciente y al correcto funcionamiento del equipo, por lo
que no está permitido.
Para evitar infecciones, los electrodos y las almohadillas de tipo esponja no deben utilizarse
sobre piel dañada.
Durante el tratamiento, el paciente no debe sentir sensaciones desagradables que rocen el
dolor. Se permite una sensación de estimulación suave.
Si, como resultado del tratamiento, aparecen dolor de cabeza, mareos, fatiga y/u otras
reacciones (del sistema nervioso autónomo), el tratamiento subsiguiente deberá
administrarse a menor intensidad.
Se recomienda mantener los equipos de diatermia (como dispositivos de onda corta y
microondas) a una distancia mínima de dos metros de los dispositivos de electroestimulación,
ya que el rendimiento de estos últimos puede verse afectado por la proximidad de un equipo
de onda corta o microondas (pulsadas) en funcionamiento.
La estimulación no debe aplicarse a través de la cabeza, directamente sobre los ojos,
cubriendo la boca o en la parte anterior del cuello (especialmente el seno carotídeo), o
mediante electrodos colocados en el pecho y la espalda superior o que crucen el corazón.
La aplicación de electrodos cerca del tórax puede aumentar el riesgo de fibrilación cardiaca.

Página 21 de 52 ES109-1634750-40 IFU
La conexión simultánea de un paciente a un equipo electromédico de alta frecuencia puede
provocar quemaduras en la posición de los electrodos y daños en el equipo de estimulación.
Los electrodos con densidades de corriente superiores a 2 mA/cm² pueden requerir una
atención especial por parte del operador.
El uso repetido de los electrodos con aplicación previa de gel provoca una rápida pérdida de
conductividad y un deterioro de la adherencia.
La pérdida de adherencia y el secado del gel harán que los bordes empiecen a levantarse, lo
que puede aumentar drásticamente la densidad de corriente, causar una distribución desigual
de la corriente en la superficie del electrodo, incrementar el riesgo de quemaduras y dar lugar
al movimiento del electrodo.
Con el tiempo, los cambios que se producen en los electrodos autoadhesivos reducen la
seguridad y pueden provocar irritación de piel y molestias al paciente.
Los electrodos autoadhesivos no deben compartirse nunca entre pacientes.
Limpie el dispositivo y sus accesorios regularmente para mantener la seguridad higiénica.
Antes de realizar cualquier mantenimiento, apague el dispositivo y desenchúfelo de la corriente.
No rocíe el agente limpiador directamente sobre la pantalla de cristal.
No utilice agentes limpiadores que contengan álcalis fuertes, lejía, ácidos, detergentes con
fluoruro o detergentes con amoniaco.
No permita que ningún líquido penetre en el dispositivo o sus accesorios durante la limpieza y
la desinfección.
Seque todos los enchufes y conectores que se hayan humedecido antes de usarlos.
DEBEN evitarse los golpes mecánicos y/o las vibraciones durante la limpieza del dispositivo.
No deje caer el dispositivo.
El aparato no debe utilizarse cuando se observen daños mecánicos. Esto incluye el
aislamiento dañado del cable.
En caso de que aparezca un mensaje de error o advertencia, detenga inmediatamente
cualquier uso del dispositivo. Apague y reinicie el dispositivo. Si el problema persiste,
póngase en contacto con su proveedor o con Enraf-Nonius B.V. para la revisión del
dispositivo. Los errores y las advertencias indican un problema interno del dispositivo, que
debe ser revisado por un técnico de servicio certificado por Enraf-Nonius B.V antes de
continuar utilizando el sistema.
El uso de un dispositivo que indique un error o una advertencia puede entrañar riesgo de
lesiones para el paciente y el usuario o causar graves daños internos en el sistema.
En caso de fallo de la pantalla u otros defectos evidentes, desconecte inmediatamente el
dispositivo e informe a un técnico de servicio certificado.
En caso de entrada de líquidos, desenchufe el aparato de la red y hágalo revisar por una
persona autorizada.
La apertura del equipo por agencias no autorizadas no está permitida y supondrá la anulación
de cualquier reclamación de garantía.
El fabricante no podrá considerarse responsable de los resultados del mantenimiento o las
reparaciones efectuadas por personas no autorizadas.
Solo los técnicos de servicio autorizados por Enraf-Nonius pueden realizar el mantenimiento
o modificar este equipo de acuerdo con la información de mantenimiento.
Si se modifica el equipo, debe realizarse una inspección y pruebas adecuadas para garantizar
el uso seguro del equipo.
Se recomienda que el Endomed 182 sea revisado anualmente por personal autorizado de
Enraf-Nonius o por su distribuidor autorizado.
Los productos sanitarios eléctricos como Endomed 182 están sujetos a precauciones especiales
respecto a la compatibilidad electromagnética (EMC) y deben instalarse y ponerse en servicio
de acuerdo con los consejos relativos a EMC indicados en las instrucciones de uso.

Página 22 de 52 ES109-1634750-40 IFU
Debe evitarse el uso de este equipo junto a otro o encima de otro, ya que podría producirse
un funcionamiento incorrecto. Si tal uso es necesario, deberá observar ambos equipos para
verificar que funcionan normalmente.
El uso de accesorios, transductores y cables diferentes de los especificados o proporcionados
por el fabricante de este equipo podría provocar el aumento de las emisiones
electromagnéticas o la disminución de la inmunidad electromagnética de este equipo y, por
tanto, originar un funcionamiento inadecuado.
Los equipos portátiles de comunicación de radiofrecuencia (incluidos periféricos como cables
de antena y antenas externas) deben utilizarse a una distancia mínima de 30 cm de cualquier
componente de Endomed 182, incluidos los cables especificados por el fabricante. De lo
contrario, el rendimiento de este equipo podría verse afectado.
Endomed 182 solo debe utilizarse con el cable de alimentación original especificado en la
lista de contenido entregada. Si utiliza el producto con cualquier otro cable de alimentación,
puede generar un aumento de las emisiones o una disminución de la inmunidad a las
interferencias del producto.

Página 23 de 52 ES109-1634750-40 IFU
10 Funcionamiento
Configuración
No utilice el dispositivo después de fluctuaciones extremas de temperatura.
Funciones de uso frecuente
Selección de los botones de Protocolos Clínicos (se aplica sólo a los Endomed 182 Tipo 2 y 3),
Favoritos y Operación Manual en la pantalla táctil.
Encender el dispositivo
• Encienda el aparato pulsando el botón de encendido/apagado en la parte posterior del
aparato.
• Después de encenderlo, el aparato se inicializará y se mostrará una pantalla de bienvenida
mientras el aparato realiza un autodiagnóstico.
• Al final de la autocomprobación, el dispositivo entra en el menú de inicio y está listo para su
uso.
Cuando se enciende la unidad, se controlan todas las funciones vitales mediante un
microprocesador interno. Durante el funcionamiento de la unidad, el valor real de salida se mide de
forma continua y se compara con el valor de salida solicitado. Cuando se detecta una situación de
fallo, la unidad detiene la corriente inmediatamente.
Navegación
Menú de Inicio
El Menú de Inicio da acceso a todas las funciones de la unidad. El menú de Inicio proporciona un
acceso estructurado a todas las terapias disponibles en la unidad, con los parámetros adecuados
por defecto. El Endomed 182 está equipado con tecnología de pantalla táctil. Seleccione un
elemento del menú tocando el botón para navegar a la siguiente pantalla. Puede navegar hacia
atrás a la pantalla anterior tocando el botón de regreso en la parte superior de la pantalla.
• Seleccione “Protocolos
clínicos“ para empezar a
trabajar con los protocolos
preestablecidos Esto no se
aplica al Endomed 182
Tipo 1.
• Seleccione "Favoritos"
para utilizar un protocolo
guardado manualmente
• Seleccione "Operación
Manual" para ajustar
todos los parámetros
manualmente
• Seleccione "Información
Sistema" para entrar en el
menú de ajustes
Endomed 182 Typo 1
Menú de inicio
Endomed 182 Typo 2 y 3
Menú de inicio

Página 24 de 52 ES109-1634750-40 IFU
Ajustes de sistema
Seleccione Información Sistema en el Menú Inicio, para ajustar varias configuraciones, comprobar la
versión del software o restaurar el dispositivo a los valores predeterminados de fábrica. Las
opciones Retroalimentación acústica, Tono de timbre y Duración del timbre sólo están disponibles
en el Endomed 182 Tipo 2 y 3.
Ajustes de Sistema
1) Seleccione “Información
Sistema”
2) Seleccione “Idioma”
3) Seleccione el idioma
preferido con los botones
4) ulsar OK para confirmar y
volver al menú anterior.
Ajuste el Luminosidad
Para cambiar el luminosidad
de la pantalla:
1) Seleccione “Brightness” ("
Luminosidad").
2) Ajuste el luminosidad con
los botones.
Rango: 10 – 100%
3) Pulsar OK para confirmar y
volver al menú anterior.

Página 25 de 52 ES109-1634750-40 IFU
Información Sistema
1) Seleccione “Información
Sistema”
En la siguiente pantalla se
puede encontrar información
sobre la unidad.
Se muestra la versión de
software instalada
actualmente.
2) Pulse ATRÁS para volver al
menú anterior.
Retroalimentación acústica
Endomed 182 Tipo 2 y 3:
Seleccione esta opción para
activar o desactivar las señales
de audio al final del
tratamiento.
1) Seleccione
"Retroalimentación acústica"
2) Activar o desactivar la
retroalimentación acústica
3) Pulse ATRÁS para volver al
menú anterior

Página 26 de 52 ES109-1634750-40 IFU
Tono de timbre y Duración del timbre
Endomed 182 Tipo 2 y 3:
1) Seleccione “Tonode timbre”
o “Duración del timbre”
Tono de timbre da acceso a 7
melodías diferentes para
señalar el final de un
tratamiento.
Duración del timbre da acceso
a 7 intervalos diferentes para
señalar el final de un
tratamiento.
Mantenimiento
Restaurar los valores de
fábrica) eliminará cualquier
favorito almacenado en el
dispositivo y borrará cualquier
configuración del sistema,
devolviendo el dispositivo a
su estado original de fábrica.
El Menú de servicio está
destinado a las
organizaciones de servicio
calificadas de Enraf-Nonius y
sólo puede ser introducido
con un código de acceso.
Limpieza del depósito activará
la bomba. Consulte el capítulo
12 Mantenimiento y solución
de problemas.
(Sólo se aplica a Endomed
182 Tipo 3.)
1) Seleccione “Mantenimiento”
(Aplicable a Endomed 182 Tipo
2 y 3)

Página 27 de 52 ES109-1634750-40 IFU
Operación Manual Endomed 182 Type 1
Endomed 182 Tipo 1 tiene un canal de salida. Véase capítulo 11 para la conexión de los electrodos.
1) Seleccione “Modo Manual”
en Menú de Inicio
Seleccione (K) para establecer
el tiempo de tratamiento
Seleccione (L) para establecer
la Intensidad
2) Establecer el tiempo de
tratamiento
Opción: 3 s / 10 s / 60 s
O con los botones
3) Establecer la intensidad
Opción: 1 mA / 3 mA / 5 mA
O con los botones
4) Presione el botón Start (o el
interruptor de pie cuando esté
conectado) para iniciar el
tratamiento
5) Presione el botón Stop (o el
interruptor de pie) para
detener el tratamiento.
El tratamiento se detiene auto-
máticamente cuando ha transcurrido
el tiempo de tratamiento.
K
L

Página 28 de 52 ES109-1634750-40 IFU
Protocolos Clínicos
Para el Endomed 182 Tipo 2 y 3 se puede encontrar una lista de tratamientos de electroterapia
comunes en Protocolos Clínicos. Estos protocolos basados en la evidencia han sido creados por
operadores profesionales y expertos después de años de experiencia en el campo.
Los protocolos clínicos preestablecidos son ajustables y reescribibles. Véase capítulo 11 para la
conexión de los electrodos.
1) Seleccione "Protocolos
Clínicos" en el Menú de Inicio
para activar la lista.
2) Seleccione el botón
para desplazarse por la lista.
3) Seleccione el icono para
obtener más información
sobre el protocolo
4) Seleccione el Protocolo
Clínico elegido para ir a la
Pantalla de Parámetros
Pantalla de información de
protocol
5) Toque los botones
para desplazarse por las
páginas
6) Seleccione OK para ir a la
pantalla de parámetros o
ATRÁS para volver al menú de
Protocolos Clínicos

Página 29 de 52 ES109-1634750-40 IFU
7) La pantalla de parámetros
muestra todos los parámetros
de un vistazo
8) Los parámetros del
protocolo clínico
preestablecidos pueden ser
ajustados
9) Presione la pestaña del canal
1 o 2 en la parte inferior de la
pantalla para cambiar el nivel
de Intensidad
10) Ajustar la Intensidad con
los botones
11) Pulse OK para confirmar y
volver a la pantalla anterior
12) El protocolo comenzará
después de establecer la
Intensidad
13) El protocolo se puede
detener pulsando el icono de
parada (A) en la pantalla táctil.
El protocolo se detiene
automáticamente cuando el
tiempo de tratamiento ha
transcurrido.
A

Página 30 de 52 ES109-1634750-40 IFU
Operación Manual Endomed 182 Tipo 2 y Tipo 3
Con la operación manual se pueden definir los parámetros personales de la electroterapia.
Endomed 182 Tipo 2 y 3 tiene dos canales de salida independientes. Para seleccionar el canal de
salida, toque la pestaña del canal en la parte inferior de la pantalla. Vea el capítulo 11 para la
conexión de los electrodos.
1) Seleccione “Operación
Manual” en Menú de Inicio
2) Seleccione la Corriente
deseada; aparecerá la pantalla
de parámetros
3) Dependiendo de la Corriente
seleccionada se pueden ajustar
varios parámetros.
Ajustando los parámetros: Frecuencia
1) Seleccione Frequencia (B)
2) Ajustar la Frecuencia con
los botones
Rango: 1 Hz – 200 Hz
3) Pulse OK para confirmar y
volver a la pantalla de
parámetros
B

Página 31 de 52 ES109-1634750-40 IFU
Ajustando los parámetros: Frecuencia Burst
1) Seleccione Frequencia Burst
(C)
2) Ajustar Frequencia Burst
Opción: 1 Hz / 2 Hz / 4 Hz
3) Pulse OK para confirmar y
volver a la pantalla de
parámetros
Ajustando los parámetros: Frecuencia de modulación
1) Seleccione Frequencia de
modulación (D)
2) Ajustar Frecuencia de
modulación con los botones
Rango: 1 Hz- 180 Hz
3) Pulse OK para confirmar y
volver a la pantalla de
parámetros
D
C

Página 32 de 52 ES109-1634750-40 IFU
Ajustando los parámetros: Tiempo de Modulación
1) Seleccione Tiempo de
Modulación (E)
2) Establecer Tiempo de
Modulación
Opción:
1-1 segundos
6-6 segundos
1-30 segundos
3) Pulse OK para confirmar y
volver a la pantalla de
parámetros
Ajustando los parámetros: Tiempo de Tratamiento
1) Seleccione Tiempo de
Tratamiento (F)
2) Ajustar Tiempo de
Tratamiento con los botones
Rango: 0 to 60 minutos
3) Pulse OK para confirmar y
volver a la pantalla de
parámetros
E
F

Página 33 de 52 ES109-1634750-40 IFU
Ajustando los parámetros: Módulo de vacío
Con el Endomed 182 Tipo 3
es posible usar electrodos de
vacío
1) Seleccione Vacío (G)
2) Establecer los parámetros
del vacío
Opción: modo pulsado 1 Hz /
modo pulsado 2 Hz /
continuo
3) Ajustar la presión de las
copas de vacío a través de los
botones
Las copas de vacío se
seleccionan automáticamente
cuando la bomba comienza a
funcionar
Ajustando los parámetros: Intensidad
1) Pulse la pestaña del canal 1
o 2 (H) en la parte inferior de la
pantalla para ajustar la
Intensidad (después de ajustar
el tiempo de tratamiento)
2) Ajustar la intensidad con los
botones
3) Pulsar OK para confirmar y
volver a la pantalla anterior
4) El programa se iniciará
después de ajustar la
Intensidad
5) El programa se puede
detener pulsando el icono de
parada en la pantalla táctil. El
programa se detiene
automáticamente cuando el
tiempo de tratamiento ha
transcurrido.
G
H

Página 34 de 52 ES109-1634750-40 IFU
Ajustando los parámetros: Control de Equilibrio
Para Interferencial 4P la opción
de Control de Equilibrio está
disponible después de que la
Intensidad haya sido fijada.
Con el Control del Equilibrio, la
intensidad del Canal 1 en
relación con el Canal 2 puede
ser aumentada o disminuida.
Un aumento de la intensidad
del Canal 1 disminuirá
automáticamente la intensidad
del Canal 2 y viceversa.
1) Seleccione Control de
Equilibrio (I)
2) Ajustar los parámetros de
Control de Equilibrio
3) Pulsar OK para confirmar y
volver a la pantalla anterior
Ajustando los parámetros: Vista de Vector
Para el Vector Isoplanar 4P se
dispone de una pantalla de
visualización de vectores
después de iniciado el
tratamiento.
1) Seleccione Vista de Vector
(J)
En esta pantalla se puede ver
una animación de anillos
rítmicos de contracción e
hinchazón, así como el
tiempo de tratamiento
restante y el nivel de
intensidad.
I
J

Página 35 de 52 ES109-1634750-40 IFU
Favoritos
Antes de la ejecución de un protocolo clínico modificado o de un ajuste manual, puede guardarse
para su uso posterior en los favoritos.
Cuando todos los parámetros de la pantalla de tratamiento estén completamente configurados
según lo requerido, puede elegir guardar los ajustes como favoritos pulsando el botón de guardar.
Los favoritos pueden guardarse mientras no se haya iniciado el tratamiento.
1) Pulse Guardar (M) para
guardar los ajustes del
programa
2) Seleccione el número de
programa con los botones
.
Hay 20 lugares de
almacenamiento disponibles
para el Endomed 182.
3) Pulse OK para confirmar.
4) Introduzca un nombre para
su favorito.
5) Pulse OK para guardar el
favorito.
M

Página 36 de 52 ES109-1634750-40 IFU
Cargar y Borrar Favoritos
1) Seleccione "Favoritos" en el
Menú de Inicio.
2) Para cargar un programa,
seleccione un favorito con los
botones
Aparecerá la pantalla de
parámetros.
3) Para borrar un favorito, pulse
el botón de borrado (N) y
seleccione el favorito que
desea eliminar mediante los
botones .
4) Pulse OK para borrar el
favorito de forma permanente.
N

Página 37 de 52 ES109-1634750-40 IFU
11 Información de la aplicación
Antes de comenzar el tratamiento, por favor asegúrese: Ha leído y comprendido el contenido
de este manual.
Antes de comenzar el tratamiento, por favor asegúrese: Respeta rigurosamente las
ADVERTENCIAS y PRECAUCIONES mencionadas en la sección de «Instrucciones de
precaución».
Antes de comenzar el tratamiento, por favor asegúrese: Ha comprobado si el paciente
presenta posibles contraindicaciones.
La conexión de accesorios distintos a los especificados por el fabricante puede afectar
negativamente a la seguridad del paciente y al correcto funcionamiento del equipo, por lo
que no está permitido.
Para evitar infecciones, los electrodos y las almohadillas de tipo esponja no deben utilizarse
sobre piel dañada.
Durante el tratamiento, el paciente no debe sentir sensaciones desagradables que rocen el
dolor. Se permite una sensación de estimulación suave.
Si, como resultado del tratamiento, aparecen dolor de cabeza, mareos, fatiga y/u otras
reacciones (del sistema nervioso autónomo), el tratamiento subsiguiente deberá
administrarse a menor intensidad.
Se recomienda mantener los equipos de diatermia (como dispositivos de onda corta y
microondas) a una distancia mínima de un metro de los dispositivos de electroestimulación,
ya que el rendimiento de estos últimos puede verse afectado por la proximidad de un equipo
de onda corta o microondas (pulsadas) en funcionamiento.
La estimulación no debe aplicarse a través de la cabeza, directamente sobre los ojos,
cubriendo la boca o en la parte anterior del cuello (especialmente el seno carotídeo), o
mediante electrodos colocados en el pecho y la espalda superior o que crucen el corazón.
La aplicación de electrodos cerca del tórax puede aumentar el riesgo de fibrilación cardiaca.
La conexión simultánea de un paciente a un equipo electromédico de alta frecuencia puede
provocar quemaduras en la posición de los electrodos y daños en el equipo de estimulación.
Los electrodos con densidades de corriente superiores a 2 mA/cm² pueden requerir una
atención especial por parte del operador.
Conexión de los electrodos
Véase el capítulo 3 para la descripción de las partes numeradas.
Endomed 182 Tipo 1
• Conecte el cable de referencia de la CD [5] al puerto [3].
• Conecte el electrodo de masa blanco [4] al cable de referencia de la CD [5].
• Uso del electrodo de masa blanco: durante el tratamiento, el paciente debe sostener el
electrodo de masa blanco en la mano.

Página 38 de 52 ES109-1634750-40 IFU
• Conecte el cable del soporte de electrodo [6] al puerto [2].
• Acople la aguja (no suministrada) al soporte de electrodo mediante el sistema de rosca, que
permite que se abra el soporte de electrodo, se inserte la aguja y se cierre el soporte.
• El portaagujas lleva un botón de iniciar/detener con el cual iniciar o interrumpir manualmente
el flujo de corriente.
Endomed 182 Tipo 2
• Conecte los cables del paciente al puerto 1 [10] y/o al puerto 2 [11] en el módulo de corriente
[9] (clavija roja en el puerto rojo, clavija negra en el puerto negro).
• Conecte los electrodos al cable del paciente.
Endomed 182 Tipo 3
• Para usar electrodos adhesivos o de goma: conecte los cables del paciente a los puertos
superiores [15] en el módulo de vacío [13] y conecte los electrodos a los cables del paciente
(clavija roja en el puerto rojo, clavija negra en el puerto negro).
• Para usar electrodos de vacío: conecte los tubos de las derivaciones de vacío a los puertos
inferiores [16] en el módulo de vacío [13] y conecte los electrodos de vacío a los tubos de las
derivaciones de vacío (clavija roja en el puerto rojo, clavija negra en el puerto negro).
Tratamiento
Antes del tratamiento
• La piel de la zona respectiva se limpia (eliminación de grasa) con jabón o alcohol de 70 grados
• Se recomienda afeitar la piel vellosa
• Compruebe la sensibilidad de la zona de tratamiento
• Coloque los electrodos y/o las esponjas (no olvide humedecerlas)
• Siga las instrucciones de funcionamiento del capítulo 10 sobre cómo ajustar la configuración e
iniciar y detener el tratamiento
Durante el tratamiento
• La intensidad se configura al nivel deseado
• Debe pedirse regularmente al paciente que comente sus sensaciones. En caso necesario, se
modificará el tratamiento
Fin del tratamiento
• El tratamiento puede detenerse pulsando el icono de «parada» en la pantalla táctil o poniendo
el temporizador a cero. El tratamiento se detiene automáticamente cuando concluye el tiempo
de tratamiento
Después del tratamiento
• Retire los electrodos y/o las esponjas
• Limpie la piel del paciente con una toalla o un pañuelo
• Compruebe los efectos esperados (p. ej. dolor, circulación y movilidad)
• Se pide al paciente que notifique cualquier reacción que pueda producirse posteriormente
Endomed 182 Tipo 1:
Electrólisis Percutánea
La electrólisis percutánea (EP) es una técnica de tratamiento no farmacológica y mínimamente
invasiva para las tendinopatías crónicas y tiene pocos efectos secundarios en comparación con la
intervención farmacológica. Generalmente la mayoría de pacientes toleran bien la EP, y es
extremadamente raro que haya complicaciones y acontecimientos adversos. No obstante, se debe
informar a los pacientes de los posibles riesgos asociados con la aplicación de la electrólisis
percutánea:

Página 39 de 52 ES109-1634750-40 IFU
• El tratamiento puede provocar un dolor leve que normalmente dura entre 48 y 72 horas
Uno de los efectos secundarios más frecuentes relacionados con la intervención son las molestias en
la zona tratada, causadas por la inserción de la aguja. Durante la aplicación de la corriente galvánica,
es posible que los pacientes experimenten dolor entre moderado e intenso (dependiendo de la
intensidad empleada). No suelen inyectarse anestésicos localmente antes de la electrólisis
percutánea, dado que los pacientes suelen tolerar bien el procedimiento (la aplicación de la corriente
galvánica puede detenerse en cualquier momento si el dolor no es tolerable). Además, el uso de
jeringuillas para administrar los anestésicos aumentaría notablemente el carácter invasivo global de
la intervención. Sin embargo, el uso de anestésicos sigue siendo una opción que se puede considerar.
• Reacciones vasovagales durante la intervención e inmediatamente después
La electrólisis percutánea afecta al sistema nervioso autónomo. Como en cualquier procedimiento
que conlleve la punción con agujas, se han comunicado reacciones vagales (como palidez,
sudoración, piloerección y frío en la piel) durante la EP. Existen varios estudios que incluyen
información sobre el posible riesgo de reacciones vasovagales. Estas reacciones pueden justificarse
ampliamente por el efecto del uso de agujas y no sólo por el de la corriente.
• Hemorragia en la zona de inserción de la aguja
Tras el tratamiento, puede aplicarse un vendaje compresivo, aunque ello no suele ser necesario.
No se recomienda el uso de hielo o la toma de fármacos antiinflamatorios (AINE) 72 horas después
del tratamiento, dado que ello contrarrestaría el efecto terapéutico previsto (iniciar un proceso
inflamatorio controlado).
Aguja de acupuntura
Se recomienda el uso de agujas de acupuntura de alta calidad, de un solo uso y estériles, que
tengan la aprobación médica de la CE, incluido el número del Cuerpo Notificado. Enraf-Nonius no
suministra agujas. La aguja debe ser compatible con la aplicación de la electrólisis guiada mediante
ecografía. Por lo que respecta a las dimensiones de las agujas, asegúrese siempre de escoger el
grosor y la longitud correctas para el tipo de lesión que se vaya a tratar.
• Diámetro de la aguja: 0,30 mm – 0,35 mm
• Diámetro exterior del mango: 1,25 mm – 1,45 mm
• Longitud del cuerpo de la aguja: 20 mm – 100 mm
• Longitud del mango: 25 mm – 30 mm
Interruptor de pie
El Endomed 182 de tipo 1 tiene un pedal opcional que puede conectarse al puerto A [7] (ver
capítulo 3).
Coloque el pedal para que pueda alcanzarse fácilmente durante
el tratamiento. La unidad de control del pedal es
multidireccional, por lo que no es necesario alinear exactamente
el pedal.
Para evitar daños, tenga en cuenta que sólo hace falta ejercer
una leve presión sobre el pulsador. Utilice la parte delantera del
pie para operar el pedal y no el talón.
Pulse el pedal una vez para activar el tratamiento. Pulse el pedal de nuevo para detener el
tratamiento.

Página 40 de 52 ES109-1634750-40 IFU
Endomed 182 Tipo 2 y 3:
TENS / IFC
Protocolo para la aplicación segura de TENS / IFC
• Compruebe posibles contraindicaciones con el paciente
• Compruebe la sensibilidad normal de la piel con una prueba de objeto romo/punzante
• El dispositivo debe estar apagado y los cables eléctricos, desconectados
• Configure los valores eléctricos de TENS / IFC mientras el dispositivo está apagado
• Conecte los electrodos a las clavijas del cable y colóquelos sobre la piel del paciente
• Compruebe que el dispositivo sigue apagado y conecte el cable de los electrodos al dispositivo
• Encienda el dispositivo
• Aumente gradualmente (lentamente) la intensidad hasta que el paciente experimente la
primera sensación de «hormigueo» del equipo de estimulación
• Siga aumentando gradualmente (lentamente) la intensidad hasta que el paciente experimente
una sensación de «hormigueo» intensa pero no desagradable
• Esta intensidad no debe ser dolorosa o causar contracción muscular
Protocolo para la finalización segura de TENS / IFC
• Disminuya gradualmente (lentamente) la intensidad hasta que el paciente no experimente
sensación de «hormigueo»
• Apague el dispositivo
• Desconecte el cable de los electrodos del dispositivo
• Desconecte los electrodos de las clavijas del cable
• Retire los electrodos de la piel del paciente
Endomed 182 Tipo 2 y 3:
Electrodos de caucho flexibles
Recomendamos utilizar los electrodos de caucho flexibles en combinación con las almohadillas de
esponja suministradas. Humedecidas adecuadamente, las almohadillas de esponja garantizan una
baja impedancia entre la piel y el estimulador durante el tratamiento y son fáciles de limpiar.
Aplique las siguientes instrucciones cuando utilice estos electrodos.
• Antes del uso inicial, lave a fondo las almohadillas de esponja en agua caliente del grifo para
eliminar el agente de impregnación.
• Antes de la aplicación, sature las almohadillas de esponja con agua del grifo. Es preferible
utilizar una solución salina por su mejor conducción eléctrica.
• Las almohadillas de esponja suministradas tienen tres capas. Con corrientes alternas (CA),
aplique una capa de esponja entre la piel y el electrodo para minimizar la resistencia.
• Fije el conjunto de electrodo/almohadilla de esponja a la piel del paciente con las cintas de
fijación suministradas. Dependiendo del tamaño del electrodo, aplique dos o tres cintas para
maximizar la superficie de contacto. Vea las ilustraciones más abajo.
Aplicación incorrecta de las cintas de fijación que
resulta en una mala conductividad eléctrica
Aplicación correcta de las cintas de fijación que resulta
en una buena conductividad eléctrica

Página 41 de 52 ES109-1634750-40 IFU
• Es importante que los electrodos hagan contacto con toda su superficie, sin que los bordes se
levanten, durante todo el tratamiento.
• El modo de salida de Endomed 182 es Corriente Constante (CC). Esto mantendrá la amplitud de
la corriente establecida, incluso cuando la impedancia de las almohadillas de la esponja
aumente durante el tratamiento causado por la evaporación del agua.
• Mantenga las almohadillas de esponja bien húmedas (a punto de gotear si se estrujan
levemente) durante el tratamiento. Vuelva a humedecerlas si el tratamiento supera los 10
minutos.
• Tras el uso, limpie las almohadillas de esponja del modo descrito en la sección «Limpieza y
desinfección».
Endomed 182 Tipo 2 y 3:
Electrodos autoadhesivos
El uso repetido de los electrodos con aplicación previa de gel provoca una rápida pérdida de
conductividad y un deterioro de la adherencia.
La pérdida de adherencia y el secado del gel harán que los bordes empiecen a levantarse, lo
que puede aumentar drásticamente la densidad de corriente, causar una distribución desigual
de la corriente en la superficie del electrodo, incrementar el riesgo de quemaduras y dar lugar
al movimiento del electrodo.
Con el tiempo, los cambios que se producen en los electrodos autoadhesivos reducen la
seguridad y pueden provocar irritación de piel y molestias al paciente.
Los electrodos autoadhesivos no deben compartirse nunca entre pacientes.
Los electrodos autoadhesivos tienen una impedancia de serie más elevada que los electrodos de
caucho flexibles. Esto puede provocar que el estimulador termine el tratamiento con una amplitud
de corriente más alta. Si esto ocurre, se recomienda continuar el tratamiento con electrodos de
caucho flexibles combinados con almohadillas de esponja humedecidas adecuadamente.
Endomed 182 Tipo 3:
Electrodos de vacío
Se puede elegir entre electrodos pequeños y grandes. Dependiendo del área a tratar pueden usarse
electrodos flexibles de goma de 4 x 6cm, 6 x 8cm y 8 x 12 cm. Los electrodos de vacío son
suficientemente flexibles para asegurar un óptimo contacto con la piel, pero a la vez
suficientemente rígidos para prevenir cualquier cambio en el contorno de la zona que está siendo
tratada, permitiendo proporcionar un satisfactorio efecto masaje.
La succión crea un efecto de masaje, que aumenta la circulación en la piel bajo los electrodos. Por
consecuencia, la resistencia cutánea disminuye, la efectividad de la corriente aplicada aumenta y el
tiempo de tratamiento se reduce.
• Elegir el tamaño de los electrodos, según la parte del cuerpo por tartar.
• Mojar las esponjas, exprimirlas ligeramente y colocarlas en los electrodos de succión.
• Seleccione vacío constante, esto facilitará el posicio-namiento de los electrodos.
• Colocar los electrodos de succión a una superficie lisa (p.ej. una mesa).
• Girar el control de succión un poco para crear una fuerza de succión en los electrodos.
• Trasladar los electrodos de succión uno por uno de la superficie lisa al cuerpo del paciente.
• Ajustar la intensidad de succión al valor deseado.
• Siga las instrucciones de funcionamiento del capítulo 10 sobre cómo ajustar la configuración e
iniciar y detener el tratamiento
• Si es necesario, corregir la fuerza de succión; Un nivel muy bajo es suficiente.
• Si es necesario, seleccione el vacío pulsátil

Página 42 de 52 ES109-1634750-40 IFU
Mantenga las almohadillas de esponja bien húmedas (a punto de gotear si se estrujan levemente)
durante el tratamiento. Vuelva a humedecerlas si el tratamiento supera los 10 minutos. Tras el uso,
limpie las almohadillas de esponja del modo descrito en la sección «Limpieza y desinfección».
Cuando use sólo un canal de vacío, cierre el otro canal con uno de los cables de vacío que no esté
en uso.
Succión continua o pulsátil
En succión continua, la bomba se desconecta al obtenerse el grado de vació ajustado, haciendo que
el Módulo de Vacío sea virtualmente silencioso en su funcionamiento. Un sistema de regulación
mantiene el vacío a un nivel constante. La bomba funciona brevemente para mantener el vacío
durante el tratamiento.
En succión pulsátil, la bomba se conecta y desconecta en alternancia. El ritmo de los impulsos para
el masaje mediante succión puede ajustarse continuamente o pulsátil (2 posiciones). La succión
pulsátil es muy adecuada para el uso con pacientes sensibles a la estimulación eléctrica, ya que
suplanta más o menos la sensación de la corriente.
Densidad de corriente
En la norma específica para estimuladores eléctricos de nervios y de músculos, IEC 60601-2-10, se
recomienda no superar una densidad de corriente de 2 mA r.m.s. / cm² (donde «r.m.s.» es el valor
cuadrático medio); de lo contrario, pueden producirse irritación o marcas cutáneas.
Para encontrar la máxima amplitud de corriente recomendada en mA para la corriente
interferencial, multiplique la superficie del electrodo en cm² por dos. Para todos los demás tipos de
ondas de corriente la corriente de salida del estimulador no debe exceeder un máximo de 50 mA
r.m.s. Esto implica que con una superficie de electrodo de 25 cm² la densidad de corriente no
deberá exceder 2 mA r.m.s. / cm². Como regla para electrodos más pequeños, como el
autoadhesivo de 3.2mm, el máximo de corriente fijado disponible en el estimulador para una onda
de corriente dada debería reducirse proporcionalmente.
Para calcular exactamente el valor r.m.s. de una corriente pulsada, puede aplicarse la siguiente
fórmula:
Tenga en cuenta que los electrodos deben colocarse con cuidado, asegurando un buen contacto
eléctrico en toda la superficie del electrodo, y que el uso de electrodos pequeños en combinación
con altas intensidades puede causar irritaciones o marcas cutáneas.
Reacciones a la conexión y la desconexión
Las características de salida de la corriente constante (CC) pueden provocar reacciones molestas en
la conexión y la desconexión si los electrodos no están colocados firmemente o pierden contacto
con la piel. Compruebe que la amplitud de la corriente es de 0 mA cuando vaya a aplicar o retirar
los electrodos.

Página 43 de 52 ES109-1634750-40 IFU
12 Mantenimiento y solución de problemas
Limpieza y Desinfección
Limpie el dispositivo y sus accesorios regularmente para mantener la seguridad higiénica.
Antes de realizar cualquier mantenimiento, apague el dispositivo y desenchúfelo de la corriente.
No rocíe el agente limpiador directamente sobre la pantalla de cristal.
No utilice agentes limpiadores que contengan álcalis fuertes, lejía, ácidos, detergentes con
fluoruro o detergentes con amoniaco.
No permita que ningún líquido penetre en el dispositivo o sus accesorios durante la limpieza y
la desinfección.
Seque todos los enchufes y conectores que se hayan humedecido antes de usarlos.
DEBEN evitarse los golpes mecánicos y/o las vibraciones durante la limpieza del dispositivo.
No deje caer el dispositivo.
Dispositivo
Para limpiar la unidad, apáguela y desenchufe la fuente de alimentación.
Limpie el aparato con un trapo húmedo. No utilice limpiadores abrasivos. Si es
necesario, puede utilizar una pequeña cantidad de detergente doméstico
suave.
Pantalla
El panel display contiene un acolchado anti-reflejo que necesita un cuidado
especial al ser limpiado. Use un trozo de algodón seco para limpiar el panel.
Para limpiar los dedos marcados o cualquier resto de grasa use agentes
limpiadores no abrasivos. Aplique una pequeña cantidad de solución sobre el
algodón y limpie el panel cuidadosamente.
Electrodos,
portaelectrodos,
esponjas y
accesorios
Antes de que lo usen los pacientes, los electrodos de goma deben limpiarse con
agua caliente. Para desinfectar los electrodos o eliminar manchas persistentes,
utilice una solución de alcohol del 70 %. La solución de alcohol puede deteriorar
el color negro, pero eso no afecta al funcionamiento de los electrodos.
Las almohadillas de esponja deben lavarse después de cada uso en agua
corriente del grifo, escurrirse a fondo y dejarse secar. Las almohadillas de
esponja dañadas deben sustituirse.
Se recomienda disponer de una cantidad suficiente de esponjas para que
puedan secarse completamente antes de reutilizarlas; esto limitará el
crecimiento de las bacterias del agua.
Cuando no se usen los electrodos, hay que quitar las almohadillas de esponja.
Esto aumenta la vida útil de los electrodos de goma. Le recomendamos que
mantenga un juego extra de almohadillas de esponja en stock.
El electrodo de masa blanco puede limpiarse con un paño húmedo. Use jabón
y agua tibia o una solución de alcohol.
El portaelectrodos puede limpiarse con un paño húmedo. Use agua tibia y un
agente de limpieza doméstico no abrasivo y no invasivo o una solución de
alcohol. No lo ponga en el autoclave.
Cable de
paciente y
Cable de
referencia de la
CD
Limpie el cable con un trapo húmedo. Use agua tibia y un producto limpiador
no abrasivo. No use soluciones que contengan alcohol. Revise el cable
regularmente por si este sufriera algún daño o no hiciera buen contacto.
Recomendamos que se disponga de un cable de repuesto.

Página 44 de 52 ES109-1634750-40 IFU
Electrodos de
vacío y esponjas
Los electrodos de vacío y las esponjas deben limpiarse con agua tibia. En caso
de que la suciedad persista, y por desinfección, use una solución con un 70%
de alcohol.
Las esponjas deben ser reemplazadas regularmente. Se recomienda disponer
de esponjas y electrodos de repuesto.
El grado de calcio puede ser depositado en las superficies de metal de los
electrodos. Esto tiene un efecto aislante. Para mantener una óptima
conductividad, estas superficies deben ser regularmente limpias y
abrillantadas.
Cables de vacío
Limpie el cable de vacío con un paño húmedo. No utilice una solución con
alcohol. Verifique periódicamente la ausencia de daños o contactos
electrónicos inadecuados en el cable. Recomendamos mantener un cable de
vacío de repuesto en almacén.
Limpieza del
depósito de agua
y de las
mangueras
• Desacople las copas de vacío de los cables de vacío.
• Sitúe un recipiente lleno de un líquido de limpieza (*) debajo del sistema.
• Extraiga las copas de vacío de los cables de vacío y coloque los extremos
periféricos de los cables en el recipiente.
• Vaya a Ajuste de sistema y seleccione Limpieza del Depósito.
• El depósito de agua se rellenará de líquido de limpieza hasta que esté
lleno.
• Vacíe el depósito de agua según se describe abajo (Depósito de agua
lleno).
(*) Se pueden utilizar los siguientes productos registrados para la desinfección del depósito de
agua:
BAKTONIL, BAKTOLAN al 5%, CHINOSOL al 1%, solución CHLORAMIN, DETTOL, ELMOCID Gamma
al 2%, PERODIN, ZEPHIROL al 5%.
Observe la información de aplicación del fabricante correspondiente.
Solución de problemas
El aparato no debe utilizarse cuando se observen daños mecánicos. Esto incluye el
aislamiento dañado del cable.
En caso de que aparezca un mensaje de error o advertencia, detenga inmediatamente
cualquier uso del dispositivo. Apague y reinicie el dispositivo. Si el problema persiste,
póngase en contacto con su proveedor o con Enraf-Nonius B.V. para la revisión del
dispositivo. Los errores y las advertencias indican un problema interno del dispositivo, que
debe ser revisado por un técnico de servicio certificado por Enraf-Nonius B.V antes de
continuar utilizando el sistema.
El uso de un dispositivo que indique un error o una advertencia puede entrañar riesgo de
lesiones para el paciente y el usuario o causar graves daños internos en el sistema.
En caso de fallo de la pantalla u otros defectos evidentes, desconecte inmediatamente el
dispositivo e informe a un técnico de servicio certificado.
En caso de entrada de líquidos, desenchufe el aparato de la red y hágalo revisar por una
persona autorizada.

Página 45 de 52 ES109-1634750-40 IFU
Mensajes de error
Cuando el dispositivo se enciende, primero ejecutará un autodiagnóstico. Cuando se detecta un
error, tanto durante el autodiagnóstico como durante el funcionamiento normal, aparecerá una
pantalla emergente en la pantalla. Cuando se muestre el error, todas las salidas se desactivarán.
Cuando se produzca esta situación, apague el equipo y desconecte todos los accesorios. Espere
aproximadamente 15 segundos y vuelva a encender el equipo.
Cuando vuelva a aparecer el error, deje de utilizar el aparato y póngase en contacto con el
proveedor.
El dispositivo debe enfriarse antes de continuar
La temperatura del dispositivo es demasiado alta para iniciar el tratamiento. Aleje el dispositivo de
cualquier fuente de calor potencial (como la luz solar directa) y deje que se enfríe. Reinicie el
dispositivo para continuar.
Corriente de salida insuficiente o nula
• Revise el cable del paciente para ver si hay roturas o mal contacto.
• Asegúrese de que las esponjas estén suficientemente húmedas.
• Limpie los electrodos
• Comprueba si hay un mal contacto
• En las zonas donde el agua es blanda, es posible que el agua se comporte de manera
deficiente, lo que da lugar a corrientes anormalmente bajas. En este caso es posible utilizar una
solución salina para mejorar la conductividad del agua.
Depósito de agua lleno
El tanque de separación de agua del Módulo de vacío está lleno. Continúe el tratamiento con los
electrodos estándar o vacíe el depósito del siguiente modo:
• Ponga el interruptor de corriente [17] en la posición de apagado (0).
• Desconecte el tubo de la boquilla de la manguera más exterior [21] y vacíe el depósito.
• Vuelva a acoplar el tubo a la boquilla.
• Ponga el interruptor de corriente [17] en la posición de encendido (1).
Escape de vacío
Probablemente hay una fuga en el sistema de vacío. Este error viene habitualmente precedido de
un funcionamiento continuo de la bomba tratando de alcanzar el valor de ajuste del vacío. Para
proteger el sistema, la bomba se detiene automáticamente transcurrido un tiempo determinado.
Inspeccione los cables de vacío y los electrodos, vuelva a poner el vacío a cero e inténtelo de nuevo.
Si persiste el fallo, deje de utilizar el dispositivo y póngase en contacto con su proveedor.

Página 46 de 52 ES109-1634750-40 IFU
También se recomienda llevar un registro del historial de mantenimiento. De hecho, en algunos
países es obligatorio.
Puede solicitarse un manual de mantenimiento con el siguiente contenido: lista de piezas de
repuesto, descripciones, instrucciones de calibración y otra información que ayudará al personal
técnico cualificado del usuario a reparar las piezas del equipo que, según declaración del fabricante,
puedan repararse.
Expectativa de vida útil
El dispositivo seguirá siendo apto para su uso previsto mientras se someta a un mantenimiento anual
por parte de un técnico de servicio cualificado tal como se describe en el manual de mantenimiento.
El técnico de servicio decidirá si el dispositivo es apto para el uso de acuerdo con las especificaciones.
Fin de la vida útil
Endomed 182 contiene materiales que pueden reciclarse y/o son nocivos para el medio ambiente.
Mantenimiento Técnico
La apertura del equipo por agencias no autorizadas no está permitida y supondrá la
anulación de cualquier reclamación de garantía.
El fabricante no podrá considerarse responsable de los resultados del mantenimiento o las
reparaciones efectuadas por personas no autorizadas.
Solo los técnicos de servicio autorizados por Enraf-Nonius pueden realizar el mantenimiento
o modificar este equipo de acuerdo con la información de mantenimiento.
Si se modifica el equipo, debe realizarse una inspección y pruebas adecuadas para garantizar
el uso seguro del equipo.
Se recomienda que el Endomed 182 sea revisado anualmente por personal autorizado de
Enraf-Nonius o por su distribuidor autorizado.
Infórmese de las normativas y los reglamentos locales relativos a la eliminación del
equipo y los accesorios.

Página 47 de 52 ES109-1634750-40 IFU
13 Especificaciones
Datos técnicos
Información eléctrica
Tensión de red:
100 - 240 Volt
Frecuencia:
50/60 Hz
Potencia de entrada máx.:
50 VA
Dimensiones (ancho x largo x alto)
Endomed 182 Tipo 1
14,5 x 17 x 9 cm
Endomed 182 Tipo 2
14 x 16 x 14 cm
Endomed 182 Tipo 3
14 x 22,5 x 17,5 cm
Estos valores representan las dimensiones de las
carcasas sin cables de comunicación, electrodos o
mangueras.
Peso
Endomed 182 Tipo 1
710 gramos
Endomed 182 Tipo 2
1460 gramos
Endomed 182 Tipo 3
2750 gramos
Estos valores representan el peso de las carcasas sin
electrodos ni cables de alimentación.
Especificaciones Tipo 1
Canales
1
Salida
Corriente Constante
Corriente Directa
Polaridad
Negativo
Intensidad
0 – 15 mA
Tiempo de tratamiento
0 – 300 segundos
Especificaciones Tipo 2 y 3
Canales
2
Salida
Corriente Constante
Intensidad
0 -100 mA
Temporizador
0 – 60 min (en pasos de 1 min)
Interferencial de 2 polos
Onda portadora
4 kHz
Frecuencia AMF
1 – 200 Hz
Frecuencia de modulación
0 – 180 Hz
Programa de modulación
1-1, 6-6, 1-30 segundos
Interferencial de 2 polos y el Vector
Isoplanar
Onda portadora
4 kHz
Frecuencia AMF
1 – 200 Hz
Frecuencia de modulación
0 – 180 Hz
Programa de modulación
1-1, 6-6, 1-30 segundos

Página 48 de 52 ES109-1634750-40 IFU
Corriente pulsada bifásica asimétrica (TENS)
Ancho de pulso
150 μs
Frecuencia
1 – 200 Hz
Frecuencia de modulación
0 – 180 Hz
Programa de modulación
1-1, 6-6, 1-30 segundos
Frecuencia Burst
1-2-4 Hz
Modificaciones técnicas reservadas
Normas de seguridad y funcionamiento
Clasificación de dispositivos médicos
IIa; Regla 9 Anexo IX de la Directiva 93/42/EEC
Este equipo cumple con todos los requerimientos de la
directive médica (93/42/EEC)
Clase de seguridad según IEC 60601-1
Clase I de seguridad eléctrica
Modo de operación
Continuo
Piezas aplicadas
Pieza aplicada de tipo BF para electroterapia.
Funcionamiento esencial
El funcionamiento esencial se basa en la norma 60601-2-10, en la que se especifica la salida
máxima de corriente y energía de pulso. Teniendo en cuenta las distintas modalidades terapéuticas,
el rendimiento esencial se basa en cinco requisitos:
1) La MC máxima de la corriente de TENS no debe superar los 50 mA.
2) La MC máxima de la corriente interferencial no debe superar los 100 mA.
3) La energía de pulso de TENS máxima no debe superar los 300 mJ.
4) La energía de pulso interferencial máxima no debe superar los 300 mJ.
5) La MC máxima de la corriente directa no debe superar los 80 mA.
Las señales de salida para la electroterapia se mantendrán en un rango del 20 % del valor
establecido.
Como el dispositivo no es un equipo de soporte vital, se permite que entre en un estado seguro
(sin señales de salida) que requiere la intervención del operador para reiniciarlo.
Condiciones ambientales
Condiciones ambientales para el transporte y el almacenamiento
Temperatura ambiente:
–20° a +70° C
Humedad relativa:
10 a 90% (sin condensación)
Presión atmosférica:
500 a 1060 hPa
Condiciones ambientales para el uso normal
Temperatura ambiente:
10° a 40° C
Humedad relativa:
10 a 90 % (sin condensación)
Presión atmosférica:
800 a 1060 hPa

Página 49 de 52 ES109-1634750-40 IFU
Información de compatibilidad electromagnética
Los productos sanitarios eléctricos como Endomed 182 están sujetos a precauciones especiales
respecto a la compatibilidad electromagnética (EMC) y deben instalarse y ponerse en servicio
de acuerdo con los consejos relativos a EMC indicados en las instrucciones de uso.
Debe evitarse el uso de este equipo junto a otro o encima de otro, ya que podría producirse
un funcionamiento incorrecto. Si tal uso es necesario, deberá observar ambos equipos para
verificar que funcionan normalmente.
El uso de accesorios, transductores y cables diferentes de los especificados o proporcionados
por el fabricante de este equipo podría provocar el aumento de las emisiones
electromagnéticas o la disminución de la inmunidad electromagnética de este equipo y, por
tanto, originar un funcionamiento inadecuado.
Los equipos portátiles de comunicación de radiofrecuencia (incluidos periféricos como cables
de antena y antenas externas) deben utilizarse a una distancia mínima de 30 cm de cualquier
componente de Endomed 182, incluidos los cables especificados por el fabricante. De lo
contrario, el rendimiento de este equipo podría verse afectado.
Endomed 182 solo debe utilizarse con el cable de alimentación original especificado en la
lista de contenido entregada. Si utiliza el producto con cualquier otro cable de alimentación,
puede generar un aumento de las emisiones o una disminución de la inmunidad a las
interferencias del producto.
Endomed 182 está clasificado como un dispositivo del Grupo 1, Clase B de acuerdo con CISPR 11.
Endomed 182 es adecuado para su uso en un entorno de centro de salud profesional. El dispositivo
utiliza energía de radiofrecuencia solamente para su funcionamiento interno. Por lo tanto, sus
emisiones de radiofrecuencia son muy bajas y no es probable que causen interferencias en los
equipos electrónicos cercanos.
Endomed 182 ha sido probado de conformidad con la norma 60601-1-2 por un laboratorio
acreditado, y se ha determinado su conformidad con todas las normas o ensayos de emisiones e
inmunidad.

Página 50 de 52 ES109-1634750-40 IFU
14 Contacto
Si necesita asistencia, visite nuestro sitio web http://www.enraf-nonius.com
La última versión (en formato electrónico o impreso) de estas Instrucciones de uso puede
obtenerse de manera gratuita en nuestro sitio web www.enraf-nonius.com, contactando con su
proveedor o llamando al número de teléfono: +31-(0)10-2030600. Le enviaremos las Instrucciones
de uso (sin cargo) en el plazo de 7 (siete) días naturales.
15 Responsabilidad del producto
En muchos países ha entrado en vigor una Ley de responsabilidad del producto. Esta Ley de
responsabilidad del producto implica, entre otras cosas, que una vez transcurrido un periodo de 10
años después de la puesta en circulación de un producto, el fabricante ya no puede ser
considerado responsable de posibles deficiencias del producto.
Hasta donde lo permita la legislación aplicable, en ningún caso Enraf-Nonius o sus proveedores o
distribuidores se harán responsables de cualquier daño indirecto, especial, incidental o consecuente
que surja del uso o la incapacidad de usar el producto, incluyendo, sin limitación, daños por
pérdidas de fondo de comercio, trabajo y productividad, errores o mal funcionamiento
informáticos, o cualquier otro daño o pérdida comercial, incluso si se hubiese advertido de la
posibilidad de dichos daños, y con independencia de la teoría legal o equitativa (contrato, agravio u
otro) en que se base la reclamación. La responsabilidad total de Enraf-Nonius en virtud de cualquier
disposición de este acuerdo no excederá en ningún caso en conjunto la suma de los honorarios
pagados por este producto y los honorarios por el soporte técnico para el producto recibidos por
Enraf-Nonius bajo un acuerdo de soporte técnico independiente (si lo hubiera), con excepción de la
muerte o las lesiones personales causadas por la negligencia de Enraf-Nonius en la medida en que
la legislación aplicable prohíba la limitación de daños en tales casos.
La parte contraria (el usuario del producto o su representante) exonerará a Enraf-Nonius de todas
las reclamaciones que surjan de terceros, cualquiera que sea su naturaleza o relación con la parte
contraria.

Página 51 de 52 ES109-1634750-40 IFU

ES109-1634750-40
Copyright:
Enraf-Nonius B.V.
Vareseweg 127 | 3047 AT | Rotterdam | Países Bajos
Tel: +31 (0)10-20 30 600 | [email protected]

Pagina 1 di 52 IT109-1634750-40 IFU
Endomed 182
IT109-1634750-40 IFU
21 Settembre, 2020
Istruzioni per l’uso

Pagina 2 di 52 IT109-1634750-40 IFU
Sommario
1 Introduzione ...................................................................................................................................................... 3
2 Simboli ................................................................................................................................................................ 7
3 Componenti del dispositivo ........................................................................................................................ 9
4 Contenuto della confezione ..................................................................................................................... 13
5 Installazione ................................................................................................................................................... 15
6 Uso previsto e destinatari previsti ......................................................................................................... 16
7 Indicazioni ....................................................................................................................................................... 17
8 Controindicazioni ......................................................................................................................................... 18
9 Istruzioni precauzionali .............................................................................................................................. 20
10 Funzionamento ............................................................................................................................................. 23
11 Informazioni sull'applicazione ................................................................................................................. 37
12 Manutenzione e risoluzione dei problemi .......................................................................................... 44
13 Specifiche ........................................................................................................................................................ 48
14 Contatti ............................................................................................................................................................ 51
15 Responsabilità per il prodotto ................................................................................................................ 51

Pagina 3 di 52 IT109-1634750-40 IFU
1 Introduzione
Prefazione
Grazie per aver scelto Endomed 182.
Endomed 182, progettato e realizzato da Enraf-Nonius B.V., offre una nuova dimensione per
l'elettroterapia, grazie al design avanzato del hardware e software. Il risultato è un dispositivo
estremamente versatile, dal funzionamento semplicissimo.
Il presente manuale è destinato ai proprietari e agli operatori di Endomed 182. Al fine di ottimizzare
l'utilizzo, l'efficienza e la durata dell'unità, leggere accuratamente il presente manuale per acquisire
familiarità con i comandi e gli accessori prima di utilizzare il dispositivo.
Descrizione del dispositivo
Endomed 182 è un elettrostimolatore ad alimentazione di rete dotato di un touchscreen a colori.
L'interfaccia utente grafica garantisce all'operatore la massima praticità.
Sono disponibili tre versioni di Endomed 182:
Endomed 182 Tipo 1 è un elettrostimolatore ad alimentazione di rete a canale singolo per l'elettrolisi
percutanea (PE) somministrata tramite corrente continua (c.c.) a bassa intensità.
Endomed 182 versioni
Nome:
Endomed 182 Tipo 1
Endomed 182 Tipo 2
Endomed 182 Tipo 3
Numero
articolo:
1634903
1634901
1634902
Numero
articolo unità
base:
1634910
1634900
1634900
Forme
d'onda
corrente:
Corrente continua
TENS
• corrente pulsata bifasica
continua (modo TENS
convenzionale)
• treni di corrente pulsata bifasica
(modo Burst TENS)
Corrente interferenziale (IFC)
• Interferenziale 2 poli
(bipolare) modalità
• Interferenziale 4 poli
(quadripolare) modalità
• Interferenziale 4 poli
(quadripolare) con vettore
isoplanare
TENS
• corrente pulsata bifasica
continua (modo TENS
convenzionale)
• treni di corrente pulsata bifasica
(modo Burst TENS)
Corrente interferenziale (IFC)
• Interferenziale 2 poli
(bipolare) modalità
• Interferenziale 4 poli
(quadripolare) modalità
• Interferenziale 4 poli
(quadripolare) con vettore
isoplanare
Vuoto
Canali:
1
2
2
Protocolli di
trattamento
pre-
programmati:
-
16
16

Pagina 4 di 52 IT109-1634750-40 IFU
Nell'elettrolisi percutanea, la corrente continua ((detta anche corrente Galvanica) viene applicata
tramite un ago inserito nell'apposito alloggiamento di un manipolo ("applicatore" o catodo).
L'elettrodo di ritorno (o anodo) è un elettrodo tenuto in mano dal paziente o un altro ago, a seconda
del trattamento previsto.
L'alloggiamento del manipolo (applicatore) consente di fissare aghi per l'agopuntura (sterili,
monouso e usa e getta) di diverse lunghezze e diametri, necessari per assicurare il corretto
posizionamento nelle diverse aree sottoposte alla terapia, a seconda della patologia da trattare.
Il manipolo dispone di un pulsante di avvio/arresto per avviare o interrompere manualmente il
passaggio di corrente.
Il dispositivo eroga una corrente continua con un'uscita di massimo 15 mA.
L'interfaccia utente grafica mostra i seguenti parametri: livello di uscita della corrente (mA), tempo
impostato per l'applicazione, corrente erogata effettiva (mC).
L'utente può impostare e regolare il livello di uscita della corrente (mA) e il tempo di applicazione, a
seconda del tipo di terapia.
Il dispositivo non offre protocolli clinici preimpostati, ma è possibile impostare e salvare come preferiti
dei parametri di trattamento (impostazioni personalizzate) da utilizzare come riferimento per future
sedute di terapia.
Il dispositivo è un'unità compatta dotata dei seguenti accessori: cavi di alimentazione e collegamento,
manipolo (applicatore), elettrodo di ritorno, interruttore a pedale (facoltativo) e documentazione
relativa al prodotto. Gli elementi consumabili, come gli aghi per l'agopuntura usa e getta, non sono
forniti insieme al prodotto.
Enraf-Nonius B.V. non fornisce elettrodi percutanei o aghi per l'agopuntura usa e getta.
Endomed 182 Tipo 2 e 3 includono 16 protocolli clinici preimpostati per terapie TENS e corrente
interferenziale. I parametri di trattamento individuali possono anche essere impostati manualmente
e regolati dall'operatore. Tutti i parametri di trattamento possono essere impostati e salvati come
preferiti (impostazioni personalizzate) da utilizzare come riferimento per future sedute di terapia.
Endomed 182 Tipo 3 presenta una configurazione impilata, formata da un modulo di aspirazione
per il vuoto e di un elettrostimolatore Endomed 182 Tipo 2. Il modulo di aspirazione per il vuoto
viene posto sotto allo stimolatore e collegato a questo. Lo scopo del modulo è generare un vuoto
per consentire al terapista di fissare rapidamente e con maggiore facilità gli elettrodi per la
stimolazione al paziente. L'operazione di fissaggio viene effettuata tramite ventose. Le ventose
dispongono di superfici per la stimolazione integrate capaci di trasferire l'elettrostimolazione al
tessuto desiderato tramite spugne inumidite.
Per Endomed 182 Tipo 2 e 3 la stimolazione elettrica viene quindi applicata alla pelle tramite
elettrodi di superficie: elettrodi in gomma flessibile, autoadesivi o a vuoto (solo Tipo 3), con
l'obiettivo di stimolare determinati tipi di fibre nervose. Enraf-Nonius offre elettrodi di varie
tipologie e dimensioni (dall'elettrodo a punta con una superficie di 0,3 cm2 agli elettrodi di
superficie pari a 96 cm2) per adeguarsi alle dimensioni dell'area di trattamento o all'obiettivo di
trattamento previsto.

Pagina 5 di 52 IT109-1634750-40 IFU
Descrizione dell'onda corrente
TENS
Il profilo d’onda a corrente impulsata bifase asimmetrica viene spesso utilizzato per le applicazioni
TENS (Transcutaneous Electrical Nerve Stimulation, stimolazione nervosa elettrica transcutanea).
Questo profilo d’onda è caratterizzato da una durata di fase e da una frequenza d’impulsi ambedue
variabili. I suoi fattori tipici, ampiezza, durata e velocità di ascesa e di caduta sono disuguali per
ciascuna fase, rispetto alla linea di base. Questo profilo d’onda è interamente equilibrato, vale a dire
che i carichi di ciascuna fase sono uguali
Per prevenire un’eventuale assuefazione alla
stimolazione, o per migliorare la tolleranza del
paziente, la frequenza degli impulsi può essere
variata tramite la modulazione di frequenza.
Corrente pulsata bifasica asimmetrica (TENS)
Burst TENS
Se la terapia TENS convenzionale si dimostra inefficace, può essere adottata una terapia TENS Burst,
particolarmente adatta al trattamento di regioni dolenti più profonde e casi di dolore cronico. La
terapia TENS Burst utilizza una durata di fase relativamente grande (150-200 μs), una frequenza di
impulso bassa (1-5 Hz) e una frequenza elevata.
Nei muscoli la cui innervazione corrisponde a quella della regione dolente dovrebbero verificarsi
delle contrazioni intense e visibili.
L'effetto analgesico in genere non si riscontra prima di 20 o 30 minuti, a differenza della terapia
TENS convenzionale, dove è piuttosto rapido. Tuttavia, al termine della stimolazione, l'effetto dura
molto più a lungo che nella terapia TENS convenzionale. L'effetto analgesico della terapia TENS
Burst è dovuto al rilascio di endorfine sia a livello spinale che sopraspinale.
Se la terapia TENS convenzionale o Burst non danno alcun sollievo o non offrono un sollievo
sufficiente, è possibile ricorrere alla modulazione di frequenza. La modulazione di frequenza può
inoltre prevenire l'accomodazione.
Corrente interferenziale (Interferential current, IFC)
Nel caso del tipo di corrente interferenziale, una frequenza a frequenza portante media viene
utilizzata per far transitare la frequenza di stimolazione a bassa frequenza (battimento) attraverso la
pelle. La relativamente bassa resistenza della pelle alla frequenza portante contribuisce a quel
confort del paziente che viene spesso associato a questo tipo di corrente. Le correnti interferenziali
sono tutte correnti alternate, senza alcun componente residuo di corrente continua. Si conoscono
diverse varianti del tipo di corrente interferenziale, di cui sono disponibili, nel Endomed 182 Typo 2
e 3: a 2 poli, 4 poli e 4 poli con vettore isoplanare.
Il metodo bipolare
In questo metodo vengono utilizzati due elettrodi e la
sovrapposizione delle due correnti alternate avviene
all'interno dell'apparecchiatura. La corrente che esce
dall'apparecchiatura è una corrente alternata
completamente modulata. Nel metodo bipolare la
profondità di modulazione è sempre del 100%.
Terapia interferenziale bipolare

Pagina 6 di 52 IT109-1634750-40 IFU
Il metodo a quadripolare (Interferenziale classico)
Con questa metodologia terapeutica, si utilizzano
quattro elettrodi e due correnti non modulate. La
frequenza di un canale viene fissata alla frequenza
portante, mentre l’altro canale presenta una
frequenza variabile, basata sulle impostazioni della
frequenza pulsazione e della modulazione di
frequenza. L’interferenza insorge allorché le due
correnti si intersecano nel tessuto. La profondità di
modulazione (che determina l’ampiezza di corrente
della stimolazione) dipende dalla direzione delle
correnti, e può variare dallo 0 al 100%. La profondità di
modulazione al 100% si verifica lungo le diagonali (e da
questo punto all’intersezione) delle due correnti. Si
tratta naturalmente di una situazione teorica, basata
sull’assunzione che il tessuto sia omogeneo. In realtà, il
tessuto è eterogeneo, per cui si deve utilizzare il
bilanciamento di corrente tra i due canali per ottenere
la profondità di modulazione del 100%. Si può pure
utilizzare il bilanciamento di corrente per compensare
le differenze nella sensazione che insorge sotto le
coppie di elettrodi.
Nel metodo a quadripolare, la profondità
di modulazione è solo del 100% in
corrispondenza delle diagonali.
Il metodo a quadripolare con vettore isoplanare
Con il vettore isoplanare l'area totale tra i 4 elettrodi è
stimolata in modo ottimale. Il posizionamento degli
elettrodi può essere effettuato in modo semplice e
veloce. La profondità di modulazione è del 100%
ovunque.
Isoplanar Interferenziale può essere utilizzato per il
trattamento di problemi che si trovano in una vasta
area e che sono molto difficili da localizzare. Isoplanar
Interferential è anche usato come leggero
pretrattamento. Dopo questa applicazione il
trattamento viene continuato con un focus su un'area
più piccola e locale.
Vettore isoplanare
Corrente continua
La corrente continua (c.c.) è stata utilizzata in medicina a numerosi scopi terapeutici. Il suo nome fa
riferimento al continuo flusso di corrente attraverso un conduttore tra due punti (elettrodi) con
potenziale differente (polarità), con il flusso che non cambia direzione nel corso del tempo. In
contrasto con la corrente alternata, le cariche elettriche si spostano sempre nella stessa direzione

Pagina 7 di 52 IT109-1634750-40 IFU
2 Simboli
Simbolo usato
Descrizione
Seguire le istruzioni contenute in Istruzioni per l'uso.
È importante leggere, comprendere e rispettare le istruzioni precauzionali e
operative.
Avviso generico di divieto.
Il divieto significa “Non bisogna…”
Avviso o avvertenza.
Indica una situazione pericolosa che, se non evitata, potrebbe provocare:
a. La morte o gravi lesioni al paziente (o)
b. Lesioni minori o moderate al paziente (o)
c. Danni all'apparecchiatura
Avvertimento generico di obbligo.
Intervento obbligatorio significa “Obbligo di…”
Parte applicata di tipo conforme ai requisiti specificati per garantire un livello
di protezione contro le scosse elettriche superiore a quello assicurato dalle
parti applicate di tipo B.
Intervallo di temperatura.
Indica l'intervallo di temperatura accettabile.
Limiti di umidità.
Indica l'umidità relativa accettabile.
Pressione atmosferica.
Indica l'intervallo di pressione atmosferica al quale è possibile esporre il
dispositivo medico in modo sicuro.
Rifiuti elettrici che possono essere riciclati.
Indica i componenti elettrici ed elettronici dell’apparecchio che sono riciclabili
e che devono essere smaltiti separatamente.
Tenere asciutto l'apparecchio
Nome e indirizzo del produttore e data di fabbricazione.
Numero di riferimento o codice parte
Numero di serie
Indica il numero di serie che consente di identificare un dispositivo medico
specifico.

Pagina 8 di 52 IT109-1634750-40 IFU
Corrente alternata
Collegamento cavo elettrodi elettroterapia
Collegamenti cavi vacuum elettroterapia
“Acceso” (Potenza)
“Spento” (Potenza)
Il marchio CE con il numero indica la conformità alla Direttiva del Consiglio
Europeo sui dispositivi medici e indica che questo dispositivo è soggetto alla
supervisione diretta dell'organismo notificato.

Pagina 9 di 52 IT109-1634750-40 IFU
3 Componenti del dispositivo
Endomed 182 Tipo 1
Endomed 182 Tipo 2
7
8
1
9
1
2
1
3
1
1
4
1
6
1
5
1
10
11

Pagina 10 di 52 IT109-1634750-40 IFU
Endomed 182 Tipo 3
12
13
16
15
14
17
18
19
21
20

Pagina 11 di 52 IT109-1634750-40 IFU
Descrizione delle parti
Parte
numerata
Descrizione
Obiettivo
[1]
Touchscreen LCD
Display TFT a colori da 4.3" con touchscreen.
Interfaccia utente che consente all'operatore di
controllare il dispositivo e modificare i parametri
dei protocolli di trattamento.
[2]
Collegamento Porta elettrodi
Collegamento Porta elettrodi
[3]
Collagemento Elettrodo di terra
vergine
Connection for DC reference cable which connects
to the blank earth electrode Collagemento per il
cavo di riferimento c.c. che si college al elettrodo di
terra vergine
[4]
Elettrodo di terra vergine
Elettrodo di riferimento
[5]
Cavo di riferimento c.c.
Cavo di collegamento dell'elettrodo di ritorno
[6]
Porta elettrodi
Manipolo per il supporto dell'ago
[7]
Collegamento A
Connessione per modulo vuoto (Endomed 182
Tipo 3 / Interruttore a pedale (Endomed 182 Tipo
1)
[8]
Collegamento B
Connessione per il Modulo di corrente
[9]
Modulo di corrente
Modulo di corrente con connessione per elettrodi
adesivi e di gomma.
[10]
Collegamento 1 Modulo di
corrente
Canale di connessione 1 per cavo paziente per
elettrodi adesivi o in gomma sul Modulo di
corrente Endomed 182.
[11]
Collegamento 2 Modulo di
corrente
Canale di connessione 2 per cavo paziente per
elettrodi adesivi o in gomma sul Modulo di
corrente Endomed 182.
[12]
Porta elettrodo per vuoto
Supporto per elettrodi del vuoto.
[13]
Modulo del vuoto
Modulo del vuoto integrato con Endomed 182 con
attacchi per elettrodi adesivi o in gomma ed
elettrodi per vuoto.
[14]
Cavi per elettrodi del Modulo
del vuoto
I cavi dell' elettrodo del Modulo del vuoto devono
essere collegati al collegamento del Modulo di
corrente [7] e [8] per il corretto funzionamento dei
collegamenti del Modulo del vuoto.
[15]
Connessioni superiori Modulo
del vuoto
Connessioni canale 1 e 2 per il cavo paziente per gli
elettrodi adesivi o di gomma sul Modulo del vuoto.
[16]
Connessioni inferiori Modulo
del vuoto
Connessioni canale 1 e 2 per il tubo flessibile di
piombo per elettrodi per vuoto sul Modulo del
vuoto.
[17]
Interruttore principale
Consente di accendere e spegnere l'unità.
Quando spegnere l'esposizione rimane visibile per
alcuni secondi (metodo a bassa energia).
[18]
Etichetta di riferimento
Fornisce informazioni sul dispositivo, come il tipo e
il numero di serie.
[19]
Connettore per cavo di rete
Collegare qui il cavo di rete fornito in dotazione
per alimentare il dispositivo.
[20]
Uscita aria
Uscita aria per il Modulo del vuoto.

Pagina 12 di 52 IT109-1634750-40 IFU
Descrizione delle parti
Parte
numerata
Descrizione
Obiettivo
[21]
Collegamento per il serbatoio
dell'acqua
Questo collegamento serve per il collegamento del
serbatoio dell'acqua. Non si può creare il vuoto se
non si collega il serbatoio dell'acqua. Il serbatoio
dell'acqua assicura che l'acqua in eccesso dalle
spugne venga raccolta e non possa essere espulsa
attraverso la pompa. Il serbatoio deve essere
svuotato ogni giorno. Fare riferimento alla sezione
sulla manutenzione.

Pagina 13 di 52 IT109-1634750-40 IFU
4 Contenuto della confezione
Dispositivo
Il contenuto della confezione dipende dal modello di dispositivo ordinato. Sono disponibili i
seguenti modelli:
Numero art.
Descrizione
1634903
Endomed 182 Tipo 1
1634901
Endomed 182 Tipo 2
1634902
Endomed 182 Tipo 3 (include il modulo del vuoto integrato)
Accessori standard Endomed 182 Tipo 1
1634750
CD-ROM con Istruzioni per l'uso (PDF su CD-ROM)
1634751
Opuscolo informativo
3444357
Cavo alimentazione 250V/2,5 A, L=2,5 m, nero
3444080
Porta elettrodi
3444582
Elettrodo di terra vergine
3444677
Cavo di riferimento c.c.
Accessori standard Endomed 182 Tipo 2 e Endomed 182 Tipo 3
1634750
CD-ROM con Istruzioni per l'uso (PDF su CD-ROM)
1634751
Opuscolo informativo
3444357
Cavo alimentazione 250V/2,5 A, L=2,5 m, nero
3444021
Fascia 250x3 cm
3444020
Fascia 100x3 cm
3444129
Elettrodi in gomma 6x8 cm, femmina da 2 mm set da 2
1460266
Cuscinetti idratabili per elettrodi in gomma 6x8 cm, set da 4
3444211
(2x) Cavo paziente, nero, 2 poli con connettori maschi da 2 mm e clip colorate
Ulteriori accessori standard Endomed 182 Tipo 3
3444503
(2x) Elettrodo vacuum Ø 60 mm, 2 pz.
3444505
Spugne elettrodo vacuum, Ø 65 mm, 4 pz. (per elettrodo vacuum Ø 60 mm)
3444507
(2x) Cavo elettrodo vacuum rosso
3444508
(2x) Cavo elettrodo vacuum nero
Accessori opzionali Endomed 182 Tipo 1
1634810
Interruttore a pedale
Acessori opzionali Endomed 182 Tipo 2 e Endomed 182 Tipo 3
Elettrodi adesivi
3444056
EN-Trode Ø 3,2 cm, femmina da 2 mm, confezione di 10 fogli da 4 pz.
3444135
EN-Trode Ø 5,0 cm, femmina da 2 mm, confezione di 10 fogli da 4 pz.
3444057
EN-Trode 5x5 cm, femmina da 2 mm, confezione di 10 fogli da 4 pz.
3444058
EN-Trode 5x9 cm, femmina da 2 mm, confezione di 10 fogli da 4 pz.
3444222
Elettrodi adesivi Ø 2,0 cm, 2 mm spinotto, 10 fogli da 8 pz.
Elettrodi in gomma
3444128
Elettrodi in gomma 4x6 cm, 2 mm spinotto, 2 pz.
3444129
Elettrodi in gomma 6x8 cm, 2 mm spinotto, 2 pz.
3444130
Elettrodi in gomma 8x12 cm, 2 mm spinotto, 2 pz.
3444380
Elettrodo in silicone 5x5 cm

Pagina 14 di 52 IT109-1634750-40 IFU
Cuscinetti idratabili per elettrodi in gomma
1460273
Cuscinetti idratabili per elettrodi in gomma 4x6 cm, set da 4
1460266
Cuscinetti idratabili per elettrodi in gomma 6x8 cm, set da 4
1460275
Cuscinetti idratabili per elettrodi in gomma 8x12 cm, set da 4
Fasce di fissaggio
3444020
Fascia 100x3 cm
3444021
Fascia 250x3 cm
3444022
Fascia 100x5 cm
3444023
Fascia 250x5 cm
Elettrodo a punta
3444180
Elettrodo a punta, connettore femmina da 2 mm, contenitore trasparente, incl. 10
tappi conduttivi in silicone
Adattatori
2523523
Adattatore, femmina da 2 mm/maschio da 4 mm, nero
2523524
Adattatore, femmina da 2 mm/maschio da 4 mm, rosso
Cavo paziente
3444211
Cavo paziente, nero, 2 poli con connettori maschi da 2 mm e clip colorate
Ulteriori accessori opzionali Endomed 182 Tipo 3
Elettrodo vacuum
3444503
Elettrodo vacuum Ø 60 mm, 2 pz.
3444504
Elettrodo vacuum Ø 90 mm, 2 pz.
3444509
Elettrodo vacuum Ø 30 mm, 2 pz.
Spunge
3444505
Spunge elettrodo vacuum, Ø 65 mm, 4 pz. (for vacuum electrodes Ø 60 mm)
3444506
Spunge elettrodo vacuum, Ø 95 mm, 4 pz. (per elettrodo vacuum Ø 90 mm)
3444516
Spugne elettrodo vacuum, Ø 30 mm, 4 pz. (per elettrodo vacuum Ø 30 mm)
Cavo elettrodo vacuum
3444507
Cavo elettrodo vacuum, rosso
3444508
Cavo elettrodo vacuum, nero
Informazioni per gli ordini
Per informazioni relative agli ordini di Endomed 182 e degli accessori, consultare il sito Web
www.enraf-nonius.com.

Pagina 15 di 52 IT109-1634750-40 IFU
5 Installazione
Ispezione
Se si notano danni da trasporto, contattare il proprio distributore locale.
NON USARE il dispositivo!
L'unità deve essere installata in modo tale da poter liberare il proprio calore nell'ambiente.
Subito dopo avere disimballato il dispositivo, eseguire la procedura seguente:
• Verificare i documenti di consegna per accertarsi che la consegna sia completa.
• Verificare che la confezione contenga tutti i componenti indicati nell’elenco degli accessori
standard
(fare riferimento al capitolo 4 - Contenuto della confezione del presente manuale).
• Ispezionare i componenti e gli accessori esterni per verificare la presenza di eventuali danni
dovuti al trasporto.
Estrazione dalla confezione
L’Endomed 182 viene confezionata in modo apposito per il trasporto in un confezionamento
singolo completo di materiali di riempimento specificamente ideati per trasporto e conservazione
in sicurezza.
• Per rimuovere l'apparecchiatura dalla confezione, porre la scatola su una superficie piana e
liscia.
• Aprire la parte superiore della scatola e rimuovere il riempimento in polistirolo.
• Prestare molta attenzione quando si estrae il contenuto dalla confezione.
Configurazione del dispositivo
Endomed 182 Tipo 2:
• Collegare il cavo dal Modulo di corrente [9] al collegamento B [8].
Endomed 182 Tipo 3:
• Collegare il cavo dal Modulo di corrente [9] al collegamento B [8].
• Collegare il cavo dal Modulo vuoto [13] al collegamento A [7].
Consultare il capitolo 3 - Componenti del dispositivo in questo manuale.
Collegamento all’alimentazione di rete
L’utilizzo di un cavo diverso da quello fornito è strettamente VIETATO in quanto
compromette la sicurezza del paziente e il corretto funzionamento dell’apparecchio.
Prima di collegare l'unità all'alimentazione di rete, controllare che la tensione di rete e la
frequenza indicate sulla targhetta di identificazione dell'apparecchiatura corrispondano a
quelle dell'alimentazione di rete.
Per evitare il rischio di scosse elettriche, questo apparecchio deve essere collegato solo ad una
rete di alimentazione con messa a terra protetta.
Per collegare l’apparecchio, inserire il cavo di rete in una presa a muro.
• Inserire il cavo di rete nella presa [19] e collegarlo a una presa a muro.
Scollegamento dall'alimentazione di rete
• Al termine del trattamento, spegnere l'apparecchio spegnendo l'interruttore di rete su Spento.
L'apparecchio è ora scollegato dalla rete elettrica.
• Scollegare il cavo di alimentazione dalla presa di corrente.
• Scollegare il cavo di rete dalla presa [19].

Pagina 16 di 52 IT109-1634750-40 IFU
6 Uso previsto e destinatari previsti
Uso previsto
Endomed 182 Tipo 1
Endomed 182 Tipo 1 è un elettrostimolatore a canale singolo pensato e progettato per l'uso da parte
di operatori sanitari per l'elettrolisi percutanea (PE) somministrata tramite corrente continua (c.c.) a
bassa intensità.
Endomed 182 Tipo 2 e 3
Endomed 182 Tipo 2 e 3 sono elettrostimolatori a due canali pensati e progettati per l'uso da parte
di operatori sanitari per la Gestione del dolore tramite corrente interferenziale (IFC) e TENS.
Con l'espressione Gestione del dolore mediante elettrostimolazione si fa riferimento a:
- Sollievo sintomatico da dolore cronico, non trattabile
- Gestione del dolore associato a condizioni post-traumatiche o post-operatorie
- Sollievo da dolore associato all'artrite.
La stimolazione elettrica viene applicata alla pelle tramite elettrodi di superficie con l'obiettivo di
stimolare determinati tipi di fibre nervose. Il sollievo dal dolore (modulazione del dolore) può
essere ottenuto tramite:
1. Il blocco delle informazioni che passano attraverso le fibre nocicettive (es. quelle che generano
dolore) mediante la stimolazione delle fibre A afferenti di grande diametro
2. Il rilascio degli oppioidi endogeni del corpo mediante la stimolazione delle fibre motorie e
afferenti di piccolo diametro.
Destinatari previsti
L'Endomed 182 è destinato ad essere utilizzato, e deve essere utilizzato solo da, o sotto la
supervisione di, utenti professionali nel campo della medicina fisica e della riabilitazione presso
strutture sanitarie professionali.
Inoltre per Endomed 182 Tipo 1:
Se un operatore sanitario (fisioterapista, medico) è autorizzato e formato per l'uso della terapia di
elettrolisi a corrente continua guidata da ecografo, l'operatore sanitario è autorizzato e formato per:
-> Effettuare punture su un paziente
-> Utilizzare l'ecografia
-> Utilizzare la terapia di elettrolisi a corrente continua.

Pagina 17 di 52 IT109-1634750-40 IFU
7 Indicazioni
Indicazioni Endomed 182 Tipo 1
Elettrolisi percutanea
L'elettrolisi percutanea (PE) può essere impiegata nel trattamento di:
• Tendinopatia rotulea/tendinite rotulea ("ginocchio del saltatore")
• Tendinopatia laterale del gomito ("gomito del tennista")
• Tendinopatia mediale del gomito ("gomito del golfista")
• Sindrome da dolore miofasciale/trigger point
• Sindrome acuta da colpo di frusta (AWS)
• Patologie della spalla (tendinopatie della cuffia dei rotatori, sindrome da dolore
subacromiale)
• Pubalgia
• Tendinopatia degli ischiocrurali
• Tendinopatia del tendine di Achille
• Fascite plantare/tallonite
Indicazioni Endomed 182 Tipo 2 e 3
TENS
Sollievo da dolore acuto
• Dolore post-operatorio
o Abdominale
o Toracico
o Ortopedico
• Dolori del parto e post parto
• Dismenorrea
• Dolore orofacciale, inclusi interventi odontoiatrici
• Trauma fisico, inclusi costole fratturate e procedure mediche minori
Sollievo da dolore cronico
• Lombalgia
• Dolore artritico, tra cui osteoartrite, artrite reumatoide
• Dolore muscolare, inclusi dolore miofasciale, tensione muscolare, indolenzimento dopo
l'attività fisica
• Dolore neuropatico, tra cui nevralgia del trigemino, post-erpetica e post-amputazione
(dolore fantasma)
• Dolore oncologico, incluso dolore da malattia metastatica ossea
• Sindrome dolorosa regionale complessa
Corrente interferenziale (IFC)
Sollievo dal dolore acuto e cronico, come ad esempio:
• Dolore post-operatorio /dolore ortopedico
• Lombalgia
• Dolore al collo
• Dolore alla spalla
• Dolore artritico, tra cui osteoartrite, artrite reumatoide
• Dolore muscolare, inclusi dolore miofasciale, tensione muscolare, indolenzimento dopo
l'attività fisica, e fibromialgia
Stimolazione muscolare
• Rafforzamento muscolare (in generale)
• Incontinenza fecale e urinaria
Disfunzione intestinale
Incremento del circolo sanguigno locale (cutaneo).

Pagina 18 di 52 IT109-1634750-40 IFU
8 Controindicazioni
Endomed 182 NON DEVE essere usato per i sintomi o le condizioni mediche descritte di
seguito.
Controindicazioni Endomed 182 Tipo 1
Controindicazioni per l'uso
• Artrite infettiva
• Cardiopatia/aritmia
• Gravidanza
• Ulcerazioni cutanee o altre infezioni cutanee
• Endoprotesi e/o osteosintesi
• Pacemaker
• Processi oncologici
• Tromboflebiti/precedenti insufficienze vascolari negli arti inferiori
• Coagulopatia/assunzione di farmaci anticoagulanti
• Discrasia ematica
• Mestruazione
• Paura degli aghi (belonefobia)
• Paura della stimolazione elettrica
• Disturbi delle ghiandole endocrine
• Pazienti neuropatici
• Pazienti affetti da patologie del sistema nervoso centrale e periferico
• Pazienti con patologie neurovegetative
• Pazienti in età pediatrica
• Condizioni mediche complicate
• Disturbi cognitivi
• Abuso di sostanze alcoliche o stupefacenti.
Punti in cui non devono essere applicati i trattamenti:
• Vasi sanguigni
• Ghiandole endocrine
• Organi
• Nervi periferici (endonevrio)
• Testa, occhi, collo e torace o parte superiore della schiena che attraversi il cuore.
Precauzioni elettrolisi percutanea
Regioni che necessitano di particolare attenzione:
• Regione addominale
• Regione intercostale (per evitare casi di pneumotorace)
• Regione toracica (per evitare casi di pneumotorace)
• Egresso toracico (per evitare casi di pneumotorace)
• Regione inguinale, cavo polipteo (per evitare danni ai fasci neurovascolari).

Pagina 19 di 52 IT109-1634750-40 IFU
Controdindicazioni Endomed 182 Tipo 2 e 3
Controindicazioni assolute:
• Dolore non diagnosticato
• Impianti attivi (incl. pacemaker cardiaci e defibrillatori cardiaci impiantabili o ICD)
• Sanguinamento dei tessuti (emorragia)
• Pazienti che non sono in grado di comprendere le istruzioni dell'operatore/fisioterapista o che
non sono in grado di collaborare
Controindicazioni relative (= controindicazioni locali):
• Gravidanza (non applicare all'interno della regione addominale/pelvica)
• Tumori maligni (non applicare su malignità in fase attiva)
• Epilessia (non applicare su collo o testa)
• Alterazioni cardiache come aritmie (non applicare sul torace)
• Posizionamento di elettrodi attorno agli occhi
• Posizionamento di elettrodi sulla parte anteriore di collo o seno carotideo
• Posizionamento di elettrodi attraverso il torace (es. posizioni anteriore e posteriore degli
elettrodi)
• Posizionamento di elettrodi sui testicoli
• Posizionamento di elettrodi sulle regioni epifisarie attive nei bambini
• Posizionamento di elettrodi su pelle danneggiata o ferite aperte
• Posizionamento di elettrodi su lesioni dermatologiche, es. dermatiti, eczemi o su pelli fragili
• Posizionamento di elettrodi su aree interessate da tessuto ischemico e/o trombosi
Nota: Non sono noti effetti collaterali causati dalla somministrazione della IFC / TENS sulla pelle
situata sopra o in prossimità di impianti metallici. La terapia TENS / IFC può essere utilizzata sulla
pelle intatta che copre impianti contenenti metallo, plastica o cemento. Sono state sottoposte
all'elettrostimolazione persone con protesi articolari che includevano componenti in metallo e ne
hanno tratto dei benefici senza effetti collaterali.
Precauzioni TENS e Corrente interferenziale
É necessario prestare attenzione e adottare le dovute precauzioni in caso di:
• Aree con sensibilità anomala (disestesia)
o iperestesia (allodinia/iperalgesia)
o ipoestesia
• Dermatite da contatto
• Donne in gravidanza
• Pazienti sensibili alle reazioni autonomiche della TENS (es. nausea, capogiri e svenimento)
Potenziali effetti avversi
Ferite o irritazioni cutanee sotto gli elettrodi sono state segnalate in seguito all'uso
dell'elettrostimolazione.
Casi isolati di irritazione cutanea possono verificarsi nei pazienti con una pelle particolarmente
sensibile. In caso di reazioni allergiche al gel per elettrodi, sospendere il trattamento e contattare
uno specialista. Se durante il trattamento dovessero insorgere segni di tachicardia e extrasistole,
sospendere il trattamento e contattare il proprio medico.

Pagina 20 di 52 IT109-1634750-40 IFU
9 Istruzioni precauzionali
Se l'uso del dispositivo ha causato o contribuito a un evento imprevisto come il decesso o
lesioni gravi dell'utente, è OBBLIGATORIO avvisare immediatamente il produttore E le
autorità competenti dello stato membro!
Tenere l’apparecchio lontano dalla portata dei bambini.
Il paziente e l’apparecchio devono essere costantemente monitorati dal terapista.
Non utilizzare l’apparecchio nei cosiddetti “ambienti umidi” (locali per idroterapia).
Quest'apparecchio non è idoneo per l'uso in presenza di miscele anestetiche infiammabili
con aria, ossigeno o ossido di azoto.
Non esporre il dispositivo alla luce diretta del sole, al calore emesso da un calorifero, a
quantità eccessive di polvere, umidità, vibrazioni e urti meccanici.
Questo dispositivo deve essere utilizzato solo sotto la continua supervisione di un medico o
di un professionista autorizzato.
Se si notano danni da trasporto, contattare il proprio distributore locale.
NON USARE il dispositivo!
L'unità deve essere installata in modo tale da poter liberare il proprio calore nell'ambiente.
L’utilizzo di un cavo diverso da quello fornito è strettamente VIETATO in quanto
compromette la sicurezza del paziente e il corretto funzionamento dell’apparecchio.
Prima di collegare l'unità all'alimentazione di rete, controllare che la tensione di rete e la
frequenza indicate sulla targhetta di identificazione dell'apparecchiatura corrispondano a
quelle dell'alimentazione di rete.
Per evitare il rischio di scosse elettriche, questo apparecchio deve essere collegato solo ad una
rete di alimentazione con messa a terra protetta.
Non utilizzare l’apparecchio dopo che è stato esposto a variazioni estreme di temperatura!
Prima di iniziare il trattamento, accertarsi: Di avere letto e compreso il contenuto del presente
manual.
Prima di iniziare il trattamento, accertarsi: Di osservare strettamente i messaggi di AVVERTENZA
e PRUDENZA riportati nelle istruzioni precauzionali.
Prima di iniziare il trattamento, accertarsi: Verificare che il paziente non presenti eventuali
controindicazioni.
Il collegamento degli accessori diversi da quelli specificati dal produttore può pregiudicare la
sicurezza del paziente e compromettere il corretto funzionamento dell’apparecchiatura e di
conseguenza non è consentito.
Per evitare possibili infezioni, gli elettrodi e i cuscinetti spugnosi non devono essere utilizzati
su una pelle che presenta lesioni.
Durante il trattamento, è possibile che il paziente avverta le sensazioni sgradevoli che
corrispondono a vero e proprio dolore. È consentito provare una leggera sensazione di
eccitazione.
Se, in seguito al trattamento si manifestano mal di testa, vertigini, stanchezza e/o altre
reazioni (relative al sistema nervoso centrale), il trattamento successivo dovrà essere
somministrato a un’intensità minore.
Si consiglia di tenere i macchinari per diatermia (quali dispositivi a onde corte e microonde) a
una distanza di almeno un metro dai dispositivi di elettrostimolazione, poiché il rendimento
di questi ultimi potrebbe essere compromesso dalla vicinanza a un macchinario a onde corte
e microonde (pulsate) in funzione.
La stimolazione non deve essere applicata attraverso la testa, direttamente sugli occhi, a
copertura della bocca, sulla parte anteriore del collo (soprattutto sul seno carotideo), da
elettrodi posizionati sul torace o sulla parte alta della schiena o attraverso il cuore.
L'applicazione di elettrodi vicino al torace potrebbe aumentare il rischio di fibrillazione
cardiaca.

Pagina 21 di 52 IT109-1634750-40 IFU
Il collegamento simultaneo di un paziente a un dispositivo elettromedicale chirurgico ad alta
frequenza può causare ustioni in corrispondenza degli elettrodi dello stimolatore e possibili
danni allo stimolatore.
Eventuali elettrodi con densità di corrente superiore a 2 mA/cm² possono richiedere
un'attenzione particolare da parte dell'operatore.
L’uso ripetuto di elettrodi pregellati comporta una rapida perdita di conducibilità e il
deterioramento delle proprietà di adesività.
Gli effetti della perdita di aderenza e dell’essiccatura del gel saranno visibili sui bordi che
inizieranno a sollevarsi, cosa che potrà far crescere notevolmente la densità di corrente; tali
effetti inoltre comporteranno la distribuzione non uniforme della corrente per tutta la
superficie degli elettrodi, causandone il possibile movimento e aumentando il rischio di
ustioni.
I cambiamenti subiti nel tempo dagli elettrodi autoadesivi producono come conseguenza una
situazione non sicura, in cui è possibile che si manifestino irritazioni cutanee e situazioni di
disagio per il paziente.
Gli elettrodi autoadesivi non devono mai essere condivisi dai pazienti.
Pulire regolarmente il dispositivo e i suoi accessori per mantenere la sicurezza igienica.
Prima di procedere a qualsiasi intervento di manutenzione, spegnere l’apparecchio e scollegare
la spina dall’alimentazione di rete.
Non spruzzare il detergente direttamente sul pannello in vetro.
Non usare agenti per la pulizia contenenti alcali forti, soda caustica, acido, detergenti con
fluoruro o con ammoniaca.
Evitare che eventuali liquidi penetrino nel dispositivo o nei suoi accessori durante la pulizia e la
disinfezione!
Asciugare tutte le prese di corrente e i connettori che si sono bagnati prima di qualsiasi ulteriore
utilizzo!
È NECESSARIO evitare urti meccanici o vibrazioni durante la pulizia del dispositivo
Non fare cadere il dispositivo.
Il dispositivo non deve essere utilizzato quando si notano danni meccanici. Ciò include
l'isolamento del cavo danneggiato.
Nel caso in cui compaia un messaggio di errore o un’avvertenza, interrompere
immediatamente qualsiasi utilizzo del dispositivo. Spegnere e riaccendere il dispositivo. Se il
problema persiste, contattare il fornitore Enraf-Nonius B.V. per l’assistenza. Gli errori e le
avvertenze indicano un problema interno al dispositivo che deve essere verificato da un
tecnico dell’assistenza certificato da Enraf-Nonius B.V prima di qualsiasi successivo utilizzo o
funzionamento del sistema.
L’utilizzo di un dispositivo indicante un errore o un’avvertenza può comportare rischi di
lesioni al paziente e all’utente oppure danni interni di notevole entità al sistema.
In caso di guasto allo schermo o altri difetti ovvi, scollegare immediatamente il dispositivo e
contattare un tecnico dell’assistenza certificato.
In caso di ingresso di liquidi, scollegare il dispositivo dalla rete elettrica e farlo controllare da
una persona autorizzata.
L’apertura dell’apparecchio da parte di agenzie non autorizzate non è consentita e porrà fine
a qualsiasi diritto di garanzia.
Il produttore declina ogni responsabilità per le conseguenze di interventi di riparazione o di
manutenzione svolti da personale non autorizzato!
Solo i tecnici del servizio assistenza autorizzati da Enraf-Nonius possono eseguire la
manutenzione o modificare questo apparecchio secondo le informazioni indicate dal servizio
assistenza.
Non si deve effettuare alcuna manutenzione sul dispositivo quando esso è in uso o è
collegato a un paziente.

Pagina 22 di 52 IT109-1634750-40 IFU
Si raccomanda di far controllare annualmente l'Endomed 182 da personale autorizzato di
Enraf-Nonius o dal suo distributore autorizzato.
I dispositivi elettromedicali come Endomed 182 sono soggetti a speciali misure precauzionali
per quanto riguarda la compatibilità elettromagnetica (EMC) e devono essere installati e messi
in funzione in conformità alle istruzioni EMC fornite nelle istruzioni per l’uso.
Evitare l’uso di questo apparecchio vicino o accatastato su altri apparecchi, per non
comprometterne il funzionamento. Se tale utilizzo è necessario, osservare questo apparecchio
e l’altro apparecchio per verificare che funzionino normalmente.
L'uso di accessori, trasduttori e cavi diversi da quelli specificati o forniti dal produttore potrebbe
determinare un aumento delle emissioni elettromagnetiche o una ridotta immunità
elettromagnetica dell’apparecchio e comprometterne il funzionamento.
Sistemi di comunicazione RF portatili (ad esempio periferiche come i cavi dell’antenna e le
antenne esterne) non devono essere utilizzati a una distanza minore di 30 cm da qualsiasi
componente di Endomed 182, inclusi i cavi specificati dal produttore. In caso contrario è
possibile che si verifichino anomalie nelle prestazioni di questo apparecchio.
Il dispositivo Endomed 182 deve essere utilizzato solo con il cavo di alimentazione originale
specificato nell’elenco dei contenuti forniti. L’utilizzo del dispositivo con un qualsiasi altro
cavo di alimentazione può causare l’aumento delle emissioni o la riduzione dell’immunità alle
interferenze del dispositivo.

Pagina 23 di 52 IT109-1634750-40 IFU
10 Funzionamento
Preparazione
Non utilizzare l’apparecchio dopo che è stato esposto a variazioni estreme di temperatura!
Funzioni di uso frequente
Selezione dei Protocolli Clinici (vale solo per gli Endomed 182 Tipo 2 e 3), dei Favoriti e dei tasti di
Funzionamento manuale sul touch screen.
Accensione
• Accendere l'unità premendo il pulsante Acceso/Spento sul retro dell'unità.
• Dopo l'accensione l'apparecchio si inizializza e viene visualizzata una schermata di benvenuto
mentre l'apparecchio esegue un autotest.
• Al termine dell'autotest il dispositivo entra nella schermata di Codice Chiave.
Quando l'unità viene attivata, tutte le funzioni fondamentali sono controllate da un
microprocessore interno. Durante il funzionamento dell'unità il livello di uscita effettivo della
corrente viene misurato costantemente e confrontato con quello richiesto. Se viene rilevata una
situazione anomala, l'unità interrompe immediatamente l'erogazione di corrente.
Navigazione
Menu Home
Il Menu Home dà accesso a tutte le funzioni dell'unità. E garantisce inoltre un accesso strutturato a
tutte le terapie presenti al suo interno, con adeguate impostazioni predefinite dei parametri. Il
dispositivo Endomed 182 è dotato di tecnologia touchscreen. Selezionare una voce di menu
premendo il pulsante per passare alla schermata seguente. È possibile tornare alla schermata
precedente toccando il pulsante posteriore nella parte superiore dello schermo.
• Selezionare "Protocolli
Clinici" per iniziare a
lavorare con i protocolli
preimpostati. Questo non
si applica all'Endomed 182
Tipo 1.
• Selezionare "Favoriti" per
utilizzare un protocollo
salvato manualmente
• Selezionare
"Funzionamento manuale"
per impostare tutti i
parametri manualmente
• Selezionare "Impostazioni
sistema" per accedere al
menu delle impostazioni
Endomed 182 Tipo 1 menu
home
Endomed 182 Tipo 2 e 3 menu
home

Pagina 24 di 52 IT109-1634750-40 IFU
Impostazioni di Sistema
Selezionare Impostazioni Sistema nel Menu Home, per regolare le varie impostazioni, controllare la
versione del software o ripristinare le impostazioni di fabbrica del dispositivo. Le opzioni Acoustic
Feedback, Tono del cicalino e Durata del cicalino sono disponibili solo nelle Endomed 182 Tipo 2 e
3.
Impostazione della Lingua
1) Selezionare "Impostazioni
sistema"
2) Selezionare “Linguaggio”
3) Selezionare la lingua
preferita con i tasti .
4) Premere OK per confermare
e tornare al menu precedente.
Impostazione del Luminosità LCD
Per cambiare la luminosità dello
schermo:
1) Selezionare “Luminosità”
2) Regolare la luminosità
tramite i tasti .
Gamma: 10 – 100%
3) Premere OK per confermare e
tornare al menu precedente.

Pagina 25 di 52 IT109-1634750-40 IFU
Informazioni di sistema
1) Selezionare “Informazioni di
sistema”
Nella schermata successiva si
possono trovare informazioni
sull'unità.
Viene mostrata la versione del
software attualmente installata.
2) Premere “Indietro” per
tornare al menu precedente
Feedback acustico
Endomed 182 Tipo 2 e 3:
Selezionare questa opzione
per attivare o disattivare i
segnali audio alla fine del
trattamento.
1) Selezionare “Feedback
acustico”
2) Attivare o disattivare il
feedback acustico
3) Premere “Indietro” per
tornare al menu precedente

Pagina 26 di 52 IT109-1634750-40 IFU
Tono del cicalino e Durata del cicalino
Endomed 182 Tipo 2 e 3:
1) Selezionare “Tono del
cicalino” o “Durata del cicalino”
Tono del cicalino fornisce
l'accesso a 7 diverse melodie
per segnalare la fine di un
trattamento.
La durata del cicalino consente
di accedere a 7 diversi intervalli
per segnalare la fine di un
trattamento.
Manutenzione
Ripristina le impostazioni
predefinite di fabbrica
cancellerà tutti i preferiti
memorizzati sul dispositivo e
cancellerà tutte le
impostazioni di sistema,
restituendo il dispositivo nel
suo stato originale di fabbrica.
Il Menu di servizio è destinato
alle organizzazioni di servizio
qualificate Enraf-Nonius e
può essere inserito solo con
un codice di accesso.
Pulizia serbatoio attiverà la
pompa. Vedi capitolo 12
Manutenzione e risoluzione
dei problemi. (applicabile solo
all'Endomed 182 Tipo 3)
1) Selezionare “Manutenzione”
(Applicabile per Endomed 182
Tipo 2 e 3)

Pagina 27 di 52 IT109-1634750-40 IFU
Funzionamento manuale Endomed 182 Tipo 1
L'Endomed 182 Tipo 1 ha un canale di uscita. Per il collegamento degli elettrodi vedi capitolo 11.
1) Selezionare "Funzionamento
manuale" nella Menu Home
Selezionare (K) per impostare il
tempo di trattamento
Selezionare (L) per impostare
l'intensità
2) Impostare il tempo di
trattamento
Opzione: 3 s / 10 s / 60 s
O tramite i tasti
3) Impostare l'intensità
Opzione: 1 mA / 3 mA / 5 mA
O tramite i tasti
4) Premere il pulsante Start (o
l'interruttore a pedale quando
è collegato) per avviare il
trattamento
5) Premere il pulsante Stop (o
l'interruttore a pedale quando
è collegato) per interrompere il
trattamento.
Il trattamento si interrompe
automaticamente allo scadere del
tempo di trattamento.
K
L

Pagina 28 di 52 IT109-1634750-40 IFU
Protocolli clinici
Per gli Endomed 182 Tipo 2 e 3, una lista di trattamenti elettroterapici comunisi trova alla voce
Protocolli Clinici. Questi protocolli basati sull'evidenza sono stati creati da operatori professionali ed
esperti dopo anni di esperienza nel settore.
I protocolli clinici preimpostati sono regolabili e riscrivibili. Per il collegamento degli elettrodi vedi
capitolo 11.
1) Selezionare "Protocolli
Clinici" nella Menu Home per
attivare la lista.
2) Selezionare il pulsante
per scorrere l'elenco.
3) Selezionare l'icona per
ulteriori informazioni sul
protocollo.
4) Selezionare il Protocollo
Clinico scelto per andare alla
schermata dei parametri
Schermata di informazioni sul
protocollo
5) Toccare i tasti per
scorrere le pagine
6) Selezionare OK per andare
alla schermata dei parametri o
Indietro per tornare al menu
dei Protocolli Clinici

Pagina 29 di 52 IT109-1634750-40 IFU
7) La schermata dei parametri
mostra tutti i parametri a colpo
d'occhio
8) I parametri del protocollo
clinico preimpostato possono
essere regolati
9) Premere la linguetta del
canale 1 o 2 nella parte
inferiore dello schermo per
modificare il livello di intensità
10) Regolare il livello di
intensità tramite i tasti
11) Premere OK per
confermare e tornare alla
schermata precedente
12) Il protocollo inizierà dopo
aver impostato il livello di
intensità
13) Il protocollo può essere
fermato premendo l'icona di
arresto (A) sul touchscreen. Il
protocollo si arresta
automaticamente allo scadere
del tempo di trattamento.
A

Pagina 30 di 52 IT109-1634750-40 IFU
Funzionamento Manuale Endomed 182 Tipo 2 e Tipo 3
Con il Funzionamento Manuale è possibile definire parametri personali per l'elettroterapia.
L'Endomed 182 Tipo 2 e 3 ha due canali di uscita indipendenti. Per selezionare il canale di uscita,
toccare la scheda del canale nella parte inferiore dello schermo. Vedere il capitolo 11 per il
collegamento degli elettrodi.
1) Selezionare "Funzionamento
manuale" nella Menu Home
2) Selezionare la Forma d'onda
corrente desiderata; apparirà la
schermata dei parametri
3) A seconda della Forma
d'onda corrente selezionata si
possono impostare diversi
parametri.
Impostazione dei parametri: Frequenza
1) Selezionare Frequeza (B)
2) Regolare la frequenza
tramite i tasti
Intervallo: 1 Hz – 200 Hz
3) Premere OK per
confermare e tornare alla
schermata dei parametri
B

Pagina 31 di 52 IT109-1634750-40 IFU
Impostazione dei parametri: Frequenza burst
1) Selezionare Frequenza
burst (C)
2) Impostare la Frequenza
burst
Opzione: 1 Hz / 2 Hz / 4 Hz
3) Premere OK per
confermare e tornare alla
schermata dei parametri
Impostazione dei parametri: Frequenza di modulazione
1) Selezionare Frequenza di
modulazione (D)
2) Regolare la frequenza di
modulazione tramite i tasti
Intervallo: 1 Hz- 180 Hz
3) Premere OK per
confermare e tornare alla
schermata dei parametri
D
C

Pagina 32 di 52 IT109-1634750-40 IFU
Impostazione dei parametri: Tempo modulazione
1) Selezionare Tempo
modulazione (E)
2) Impostare Tempo
modulazione
Opzione:
1-1 secondi
6-6 secondi
1-30 secondi
3) Premere OK per
confermare e tornare alla
schermata dei parametri
Impostazione dei parametri: Tempo trattamento
1) Selezionare Tempo
trattamento (F)
2) Impostare il Tempo
trattamento tramite i tasti
Intervallo: Da 0 a 60 minuti
3) Premere OK per
confermare e tornare alla
schermata dei parametri
E
F

Pagina 33 di 52 IT109-1634750-40 IFU
Impostazione dei parametri: Modulo del vuoto
Con l'Endomed 182 Tipo 3 è
possibile utilizzare elettrodi
per il vuoto
1) Selezionare Vuoto (G)
2) Impostare i parametri del
vuoto
Opzione: modo pulsato 1 Hz /
modo pulsato 2 Hz / continuo
3) Regolare la pressione delle
ventose a vuoto tramite i tasti
Le ventose a vuoto vengono
selezionate automaticamente
quando la pompa inizia a
funzionare
Impostazione dei parametri: Intensità
1) Premere la linguetta del
canale 1 o 2 (H) nella parte
inferiore dello schermo per
impostare il livello di intensità
(dopo aver impostato il tempo
di trattamento)
2) Regolare il livello di intensità
tramite i tasti
3) Premere OK per confermare
e tornare alla schermata
precedente
4) Il programma si avvia dopo
aver impostato il livello di
intensità
5) Il programma può essere
fermato premendo l'icona di
stop sul touchscreen. Il
programma si arresta
automaticamente allo scadere
del tempo di trattamento.
G
H

Pagina 34 di 52 IT109-1634750-40 IFU
Impostazione dei parametri: Controllo dell’equilibrio
Per Interferenziale 4P l'opzione
di controllo dell’equilibrio è
disponibile dopo
l'impostazione dell'Intensità.
Con il controllo dell'equilibrio
l'intensità del canale 1 rispetto
al canale 2 può essere
aumentata o diminuita. Un
aumento dell'intensità del
canale 1 diminuirà
automaticamente l'intensità
del canale 2 e viceversa.
1) Selezionare Controllo
dell’equilibrio (I)
2) Impostare I parametri di
controllo dell’equilibrio
3) Premere OK per confermare
e tornare alla schermata dei
parametri
Impostazione dei parametri: Vista Vettore
Per 4P Isoplanar Vector è
disponibile uno schermo Vista
Vettore dopo l'inizio del
trattamento.
1) Selezionare Vista Vettore (J)
In questo schermo si può
vedere un'animazione di anelli
ritmici che si restringono e si
gonfiano, così come il tempo
di trattamento rimanente e il
livello di intensità.
I
J

Pagina 35 di 52 IT109-1634750-40 IFU
Favoriti
Prima dell'esecuzione di un protocollo clinico modificato o di un'impostazione manuale, può essere
salvato per un uso successivo sotto la voce "Favoriti".
Quando tutti i parametri nella schermata del trattamento sono completamente impostati come
richiesto, è possibile scegliere di salvare le impostazioni come preferiti premendo il tasto store.
I favoriti possono essere memorizzati finché il trattamento non è stato avviato.
1) Premere Salva (M) per
salvare le impostazioni del
programma
2) Selezionare il numero di
programma tramite i tasti
Sono disponibili 20 posizioni di
archiviazione per l'Endomed
182
3) Premere OK per confermare
4) Inserite un nome per il
vostro preferito
5) Premere OK per salvare il
Favorito
M

Pagina 36 di 52 IT109-1634750-40 IFU
Caricamento e cancellazione dei favoriti
1) Selezionare “Favoriti” nel
menu Home
2) Per caricare un programma
selezionare un Favorito tramite
i tasti
Apparirà la schermata dei
parametri.
3) Per cancellare un Favorito
premere il tasto di
cancellazione (N) e selezionare
il Favorito da rimuovere tramite
i tasti
4) Premere OK per cancellare
definitivamente il Favorito.
N

Pagina 37 di 52 IT109-1634750-40 IFU
11 Informazioni sull'applicazione
Prima di iniziare il trattamento, accertarsi: Di avere letto e compreso il contenuto del presente
manual.
Prima di iniziare il trattamento, accertarsi: Di osservare strettamente i messaggi di
AVVERTENZA e PRUDENZA riportati nelle istruzioni precauzionali.
Prima di iniziare il trattamento, accertarsi: Verificare che il paziente non presenti eventuali
controindicazioni.
Il collegamento degli accessori diversi da quelli specificati dal produttore può pregiudicare la
sicurezza del paziente e compromettere il corretto funzionamento dell’apparecchiatura e di
conseguenza non è consentito.
Per evitare possibili infezioni, gli elettrodi e i cuscinetti spugnosi non devono essere utilizzati
su una pelle che presenta lesioni.
Durante il trattamento, è possibile che il paziente avverta le sensazioni sgradevoli che
corrispondono a vero e proprio dolore. È consentito provare una leggera sensazione di
eccitazione.
Se, in seguito al trattamento si manifestano mal di testa, vertigini, stanchezza e/o altre
reazioni (relative al sistema nervoso centrale), il trattamento successivo dovrà essere
somministrato a un’intensità minore.
Si consiglia di tenere i macchinari per diatermia (quali dispositivi a onde corte e microonde) a
una distanza di almeno un metro dai dispositivi di elettrostimolazione, poiché il rendimento
di questi ultimi potrebbe essere compromesso dalla vicinanza a un macchinario a onde corte
e microonde (pulsate) in funzione.
La stimolazione non deve essere applicata attraverso la testa, direttamente sugli occhi, a
copertura della bocca, sulla parte anteriore del collo (soprattutto sul seno carotideo), da
elettrodi posizionati sul torace o sulla parte alta della schiena o attraverso il cuore.
L'applicazione di elettrodi vicino al torace potrebbe aumentare il rischio di fibrillazione
cardiaca.
Il collegamento simultaneo di un paziente a un dispositivo elettromedicale chirurgico ad alta
frequenza può causare ustioni in corrispondenza degli elettrodi dello stimolatore e possibili
danni allo stimolatore.
Eventuali elettrodi con densità di corrente superiore a 2 mA/cm² possono richiedere
un'attenzione particolare da parte dell'operatore.
Collegamento degli elettrodi
Per la descrizione delle parti numerate si veda il capitolo 3.
Endomed 182 Tipo 1
• Collegare il cavo di riferimento c.c. [5] all'apposito attacco [3]
• Collegare l'elettrodo di terra vergine [4] al cavo di riferimento c.c. [5]
• Utilizzo dell'elettrodo di terra vergine: durante la seduta, il paziente deve tenere in una mano
l'elettrodo di terra vergine

Pagina 38 di 52 IT109-1634750-40 IFU
• Collegare il cavo del manipolo [6] all'apposito attacco [2]
• Fissare l'ago (non incluso) nell'apposito alloggiamento tramite il sistema a filettatura, che
consente di aprire il manipolo, inserire l'ago e chiudere nuovamente il manipolo
• Il manipolo dispone di un pulsante di avvio/arresto per avviare o interrompere manualmente il
passaggio di corrente.
Endomed 182 Tipo 2
• Collegare i cavi del paziente all'attacco 1 [10] e/o all'attacco 2 [11] nel modulo che regola il
passaggio della corrente [9] (connettori rossi collegati agli attacchi rossi, connettori neri
collegati agli attacchi neri)
• Collegare gli elettrodi ai cavi del paziente.
Endomed 182 Tipo 3
• Nel caso in cui vengano impiegati elettrodi adesivi o in gomma: collegare i cavi del paziente
agli attacchi superiori [15] del modulo di aspirazione per il vuoto [13] e collegare gli elettrodi ai
cavi del paziente (connettori rossi collegati agli attacchi rossi, connettori neri collegati agli
attacchi neri)
• Nel caso in cui vengano impiegati elettrodi a vuoto: collegare i tubi principali per l'aspirazione
agli attacchi inferiori [16] del modulo di aspirazione per il vuoto [13] e collegare gli elettrodi a
vuoto ai tubi principali per l'aspirazione (connettori rossi collegati agli attacchi rossi, connettori
neri collegati agli attacchi neri).
Trattamento
Prima del trattamento
• L’area della pelle interessata viene pulita (eliminando il grasso) con sapone o alcool al 70%
• Si consiglia di depilare l’area se necessario
• Testare la sensibilità dell’area del trattamento
• Posizionare gli elettrodi e/o le spugne (non dimenticare di inumidirle)
• Seguire le istruzioni per l'uso del capitolo 10 su come regolare le impostazioni e avviare e
interrompere il trattamento
Durante il trattamento
• L’intensità viene impostata sul livello desiderato
• Al paziente viene chiesto con regolarità di riferire qualsiasi sensazione avvertita. Se necessario, il
trattamento viene modificato
Al termine del trattamento
• Il trattamento può essere interrotto premendo l’icona di arresto sul touchscreen o impostando
il timer a zero. Il trattamento si interrompe automaticamente una volta scaduto il tempo di
trattamento
Dopo il trattamento
• Rimuovere gli elettrodi e/o le spugne
• Pulire la pelle del paziente con un asciugamano o un fazzoletto
• Gli effetti attesi sono tenuti sotto controllo (ad es. dolori o effetti su circolazione e mobilità)
• Successivamente al paziente si chiede di annotare qualsiasi reazione eventualmente avvertita

Pagina 39 di 52 IT109-1634750-40 IFU
Endomed 182 Tipo 1:
Elettrolisi percutanea
L'elettrolisi percutanea (PE) è una tecnica di trattamento non farmacologica e a invasività minima
per le tendinopatie croniche e presenta pochi effetti collaterali rispetto all'intervento farmaceutico.
Si tratta di un trattamento ben tollerato dalla maggior parte dei pazienti, con complicazioni ed
effetti collaterali estremamente rari. Ciononostante, i pazienti devono essere informati dei potenziali
rischi associati alla somministrazione dell'elettrolisi percutanea:
• Il trattamento può causare lieve dolore che si protrae generalmente da 48 a 72 ore
Uno degli effetti collaterali più comuni di questa terapia è il disagio nell'area sottoposta al
trattamento, causato dall'inserimento dell'ago. Durante l'applicazione della corrente continua, i
pazienti potrebbero percepire un dolore moderato o intenso a seconda dell'intensità adoperata. In
genere non vengono iniettati degli anestetici locali prima dell'elettrolisi percutanea, in quanto la
procedura è solitamente ben tollerata dai pazienti (l'applicazione di corrente continua può essere
interrotta in qualsiasi momento nel caso in cui il dolore non sia sopportabile). Inoltre, l'impiego di
siringhe per l'inoculazione degli anestetici incrementerebbe di molto l'invasività dell'operazione.
Tuttavia, l'uso di anestetici rimane possibile
• Reazioni vasovagali durante e immediatamente a seguito dell'operazione
L'elettrolisi percutanea influenza il sistema nervoso autonomo. Come in tutte le procedure che
prevedono l'uso di aghi, sono state riportate delle reazioni vasovagali (come pallore, sudorazione,
piloerezione e freddezza della pelle) durante l'elettrolisi percutanea. Diversi studi includono
informazioni sul potenziale rischio di possibili reazioni vasovagali. Tali reazioni possono essere
largamente giustificate dall'effetto dell'uso degli aghi e non solo dalla corrente
• Sanguinamento nell'area di inserimento dell'ago
A seguito del trattamento, è possibile applicare un bendaggio compressivo, ma in genere ciò non è
necessario.
L'uso di ghiaccio o l'assunzione di qualsiasi farmaco antinfiammatorio (FANS) 72 ore dopo il
trattamento è sconsigliato, in quanto contrasterebbe l'effetto terapeutico anticipato, ossia originare
un processo infiammatorio controllato.
Ago per l'agopuntura
Si raccomanda l'uso di aghi per agopuntura sterili di alta qualità, monouso e sterili, che hanno
l'approvazione medica CE, compreso il numero di Corpo Notificato. Enraf-Nonius non fornisce alcun
ago. L'ago deve essere compatibile con la somministrazione di elettrolisi guidata da ecografo. Per
quanto riguarda le dimensioni dell'ago, assicurarsi sempre di selezionare lo spessore e la lunghezza
adeguati per il tipo di lesione da trattare.
• Diametro dell'ago: 0,30 mm - 0,35 mm
• Diametro esterno del manipolo: 1,25 mm - 1,45 mm
• Lunghezza del corpo dell'ago: 20 mm - 100 mm
• Lunghezza del manipolo: 25 mm - 30 mm

Pagina 40 di 52 IT109-1634750-40 IFU
Interruttore a pedale
Endomed 182 Tipo 1 dispone di un interruttore a pedale facoltativo che può essere collegato
all'attacco A [7] (vedere capitolo 3).
Posizionare l'interruttore a pedale in modo che sia facilmente
raggiungibile durante il trattamento. L'unità di controllo a pedale
è multidirezionale: non è necessario allineare con precisione
l'interruttore a pedale.
Per evitare danni all'apparecchiatura, tenere a mente che è
necessario esercitare una pressione minima sull'interruttore.
Utilizzare la parte anteriore del piede per attivare l'interruttore,
non il tallone.
Premere l'interruttore a pedale per iniziare il trattamento. Premere nuovamente l'interruttore per
interrompere il trattamento.
Endomed 182 Tipo 2 e 3:
TENS / IFC
Protocollo per l’applicazione sicura di TENS / IFC
• Verificare le controindicazioni con il paziente
• Testare la pelle per la normale sensazione con il test di smussamento/affilatura
• Il dispositivo deve essere spento e i cavi elettrici devono essere scollegati
• Impostare le caratteristiche elettriche di TENS / IFC quando il dispositivo è spento
• Collegare gli elettrodi agli spinotti del cavo principale e posizionarli sulla pelle del paziente
• Assicurarsi che il dispositivo sia ancora spento e collegare il cavo degli elettrodi al dispositivo
• Accendere il dispositivo
• Aumentare gradualmente (lentamente) l’intensità ulteriormente fino a quando il paziente non
avvertirà una sensazione di “formicolio” forte ma piacevole
• Tale intensità non deve essere dolorosa né deve provocare contrazioni muscolari
Protocollo per l’interruzione sicura di TENS / IFC
• Diminuire gradualmente (lentamente) l’intensità fino a quando il paziente non avvertirà alcuna
sensazione di “formicolio”
• Spegnere il dispositivo
• Scollegare il cavo degli elettrodi dal dispositivo
• Staccare gli elettrodi dagli spinotti del cavo principale
• Rimuovere gli elettrodi dalla pelle del paziente

Pagina 41 di 52 IT109-1634750-40 IFU
Endomed 182 Tipo 2 e 3:
Elettrodi flessibili in gomma
Si consiglia di utilizzare elettrodi flessibili in gomma in combinazione con i cuscinetti spugnosi in
dotazione. Se correttamente inumiditi, nel corso del trattamento i cuscinetti spugnosi garantiscono
una bassa impedenza tra la pelle e lo stimolatore e al termine si puliscono facilmente. Per l’utilizzo
di tali elettrodi seguire le linee guida riportate sotto.
• Prima del primo utilizzo sciacquare bene i cuscinetti spugnosi con acqua di rubinetto calda per
rimuovere l’agente impregnante.
• Prima dell’applicazione, bagnare i cuscinetti spugnosi con acqua di rubinetto. Se tuttavia si
desidera aumentare la conduzione elettrica, si consiglia di utilizzare una soluzione salina.
• I cuscinetti spugnosi in dotazione presentano tre strati. Con le correnti CA, applicare uno strato
di spugna tra la pelle e l’elettrodo per una resistenza minima.
• Sistemare l’insieme composto da cuscinetto spugnoso ed elettrodo adesivo sul paziente
utilizzando le fasce per il fissaggio. In base alle dimensioni degli elettrodi, utilizzare due o tre
fasce per aumentare al massimo la superficie di contatto. Vedere le immagini di seguito.
• È importante che nel corso del trattamento gli elettrodi aderiscano completamente e che i
bordi non si sollevino.
• La modalità di uscita Endomed 182 è a Corrente Costante (CC). In questo modo si garantirà
l’ampiezza di corrente configurata, anche quando l’impedenza dei cuscinetti spugnosi aumenta
durante il trattamento a causa dell’evaporazione dell’acqua.
• Mantenere i cuscinetti spugnosi ben idratati (devono quasi gocciolare se leggermente strizzati)
durante il trattamento. Inumidire di nuovo se il trattamento supera i 10 minuti.
• Dopo l’uso pulire i cuscinetti spugnosi come descritto in “Pulizia e disinfezione”.
Applicazione errata delle fasce di fissaggio, che
produce una scarsa conducibilità elettrica.
Applicazione corretta delle fasce di fissaggio, che
produce una buona conducibilità elettrica.

Pagina 42 di 52 IT109-1634750-40 IFU
Endomed 182 Tipo 2 e 3:
Elettrodi autoadesivi
L’uso ripetuto di elettrodi pregellati comporta una rapida perdita di conducibilità e il
deterioramento delle proprietà di adesività.
Gli effetti della perdita di aderenza e dell’essiccatura del gel saranno visibili sui bordi che
inizieranno a sollevarsi, cosa che potrà far crescere notevolmente la densità di corrente; tali
effetti inoltre comporteranno la distribuzione non uniforme della corrente per tutta la
superficie degli elettrodi, causandone il possibile movimento e aumentando il rischio di
ustioni.
I cambiamenti subiti nel tempo dagli elettrodi autoadesivi producono come conseguenza una
situazione non sicura, in cui è possibile che si manifestino irritazioni cutanee e situazioni di
disagio per il paziente.
Gli elettrodi autoadesivi non devono mai essere condivisi dai pazienti.
Gli elettrodi autoadesivi presentano un’impedenza in serie più alta rispetto agli elettrodi flessibili in
gomma. In conseguenza di ciò è possibile che lo stimolatore termini il trattamento ad ampiezze di
corrente maggiori. Quando ciò si verifica, si consiglia di continuare il trattamento con gli elettrodi
flessibili in gomma, in combinazione con i cuscinetti spugnosi correttamente inumiditi.
Endomed 182 Tipo 3:
Elettrodi d’aspirazione
Vi è una scelta di elettrodi grandi e piccoli. Le aree degli elettrodi corrispondono a quelle degli
elettrodi di gomma flessibile da 4 x 6 cm, 6 x 8 cm e da 8 x 12 cm. Gli elettrodi d’aspirazione sono
sufficientemente flessibili per assicurare un contatto ottimale con la pelle, ma abbastanza rigidi per
prevenire qualsiasi cambiamento nel contorno della parte sotto trattamento, consentendo di trarre
pieno vantaggio dall‘effetto di massaggio dell’aspirazione impulsata.
L'effetto massaggio risultante dal vuoto pulsato assicura un buon flusso di sangue attraverso la
pelle sotto gli elettrodi. Questo riduce la resistenza della pelle e aumenta l'efficacia della corrente di
stimolazione.
• Scegliere la dimensione appropriata dell'elettrodo per la parte del corpo da trattare
• Inumidire le spugne. Spremerle leggermente per rimuovere l'acqua in eccesso e metterle negli
elettrodi per il vuoto
• Selezionare il vuoto costante, questo faciliterà il posizionamento degli elettrodi
• Posizionare gli elettrodi per il vuoto su una superficie liscia (ad es. su un tavolo)
• Alzare un po' l'intensità del vuoto, in modo da creare un vuoto negli elettrodi
• Ora spostare gli elettrodi uno ad uno dalla superficie liscia al corpo del paziente
• Impostare l'intensità del vuoto al valore desiderato
• Seguire le istruzioni per l'uso del capitolo 10 su come regolare le impostazioni e avviare e
interrompere il trattamento
• Correggere l'intensità del vuoto se necessario; è sufficiente un vuoto basso
• Se necessario, selezionare il vuoto pulsato
Mantenere i cuscinetti spugnosi ben idratati (devono quasi gocciolare se leggermente strizzati)
durante il trattamento. Inumidire di nuovo se il trattamento supera i 10 minuti. Dopo l’impiego,
ripulire i cuscinetti spugnosi come descritto dalle istruzioni di pulizia e disinfezione.
• Quando si utilizza un solo canale di vuoto, chiudere l'altro canale con uno dei cavi di vuoto non
in uso.

Pagina 43 di 52 IT109-1634750-40 IFU
Vuoto continuo o pulsato
Quando si utilizza un vuoto continuo, l'impulso di vuoto si spegne non appena viene raggiunta la
pressione di vuoto selezionata, rendendo il modulo del vuoto praticamente silenzioso nel
funzionamento. Un sistema di controllo assicura che il vuoto rimanga costante. La pompa si
accende per brevi intervalli durante il trattamento per mantenere il vuoto.
Quando si utilizza il vuoto pulsato, la pompa si accende e si spegne ad intermittenza. Il ritmo
pulsante del massaggio a vuoto è regolabile in modo continuo o pulsante (due possibilità). Il vuoto
pulsante è molto utile per i pazienti sensibili alla corrente elettrica, poiché la sensazione della
corrente tende ad essere soppressa.
Densità di corrente
Nella particolare norma relativa agli stimolatori elettrici neuromuscolari IEC 60601-2-10, si consiglia
di non superare la densità di corrente di 2 mA r.m.s./cm², altrimenti potrebbero manifestarsi
irritazioni cutanee o ferite.
Per trovare l’ampiezza di corrente massima consigliata in mA per i profili d’onda delle correnti di
stimolazione Interferenziale, moltiplicare la superfici dell’elettrodo in cm² per 2. Per tutte le altre
forme d’onda di corrente, la corrente in uscita dello stimolatore non può mai superare 50 mA r.m.s.
Ciò significa che con la superficie di un elettrodo di 25 cm² la densità di corrente non può mai
superare 2 mA r.m.s./cm². Come regola generale per gli elettrodi di dimensioni minori, come quelli
autoadesivi da 3,2 mm, la configurazione di corrente massima a disposizione nello stimolatore per
una data forma d’onda di corrente deve essere proporzionalmente ridotta.
Per un calcolo preciso del valore r.m.s. di una forma d’onda di corrente pulsata è possibile utilizzare
la formula seguente:
Si noti che gli elettrodi devono essere posizionati con cura, garantendo un buon contatto elettrico
su tutta la superficie dell'elettrodo, e che l'uso di piccoli elettrodi in combinazione con alte intensità
può causare irritazioni cutanee o ferite.
Reazioni di connessione e sconnessione
Le caratteristiche d’uscita a corrente continua (c.c.) possono provocare spiacevoli reazioni di
connessione e sconnessione, se gli elettrodi non sono predisposti in maniera ferma, o se perdono
contatto con la pelle. Assicurarsi che l’ampiezza di corrente sia predisposta a 0 mA quando si
applicano o rimuovono gli elettrodi.

Pagina 44 di 52 IT109-1634750-40 IFU
12 Manutenzione e risoluzione dei problemi
Pulizia e disinfezione
Pulire regolarmente il dispositivo e i suoi accessori per mantenere la sicurezza igienica.
Prima di procedere a qualsiasi intervento di manutenzione, spegnere l’apparecchio e scollegare
la spina dall’alimentazione di rete.
Non spruzzare il detergente direttamente sul pannello in vetro.
Non usare agenti per la pulizia contenenti alcali forti, soda caustica, acido, detergenti con
fluoruro o con ammoniaca.
Evitare che eventuali liquidi penetrino nel dispositivo o nei suoi accessori durante la pulizia e la
disinfezione!
Asciugare tutte le prese di corrente e i connettori che si sono bagnati prima di qualsiasi ulteriore
utilizzo!
È NECESSARIO evitare urti meccanici o vibrazioni durante la pulizia del dispositivo
Non fare cadere il dispositivo.
Dispositivo
Per pulire l’apparecchio, spegnerlo e staccarlo dall’alimentazione di rete. Pulire
l’apparecchio mediante un panno inumidito. Non impiegare agenti abrasivi di
pulitura. Se necessario, si potrà utilizzare una ridotta quantità di blando
detergente domestico.
Pannello del
display
Il pannello del display include un rivestimento antiriflesso che necessita di
particolare cura durante la pulizia. Utilizzare un panno asciutto in cotone
morbido o un tessuto in microfibra per pulire il pannello. Per rimuovere
impronte di dita o grasso, utilizzare un detergente per vetri non abrasivo.
Applicare una piccola quantità di detergente su un panno in cotone morbido e
pulire con cura il pannello.
Elettrodi, porta
elletrodi, spugne
e accessori
Tra un utilizzo e l’altro, gli elettrodi in gomma devono essere puliti con acqua
tiepida. Per disinfettare gli elettrodi o rimuovere le macchie più tenaci, utilizzare
una soluzione alcolica al 70%. La soluzione alcolica può far comparire macchie
nere, che però non pregiudicano il funzionamento degli elettrodi.
Tra un utilizzo e l’altro, i cuscinetti spugnosi devono essere lavati con acqua
corrente, scolati perfettamente e quindi asciugati. I cuscinetti spugnosi
danneggiati devono essere sostituiti.
Si consiglia di dotarsi di una quantità sufficiente di spugne in modo tale da
garantirne la completa asciugatura prima di poterle riutilizzare, limitando così la
proliferazione di batteri di origine idrica.
Quando gli elettrodi non vengono utilizzati, i tamponi di spugna devono essere
rimossi. Ciò aumenta la vita operativa degli elettrodi di gomma. Si consiglia di
tenere un set extra di tamponi di spugna in magazzino.
L'elettrodo di terra vergine può essere pulito con un panno umido. Utilizzare
sapone e acqua tiepida o una soluzione alcolica.
Il porta elettrodi può essere pulito con un panno umido. Utilizzare acqua tiepida
e un detergente domestico non abrasivo e non invasivo o una soluzione alcolica.
Non mettere in autoclave.

Pagina 45 di 52 IT109-1634750-40 IFU
Cavo paziente e
Cavo di
riferimento c.c.
Pulire il cavo del paziente mediante un panno inumidito. Utilizzare acqua tiepida
e un agente non abrasivo per pulizie domestiche. Non impiegare una soluzione
alcolica. Verificare regolarmente il cavo per rilevare danni e/o un cattivo contatto
elettrico. Consigliamo di tenere a disposizione un cavo del paziente di ricambio.
Elettrodi sotto
vuoto e spugne
Gli elettrodi di aspirazione e le spugne devono essere puliti con acqua tiepida.
In caso di sporco persistente e per la disinfezione si può usare una soluzione
alcolica al 70%.
Le spugnette devono essere sostituite con frequenza. Si consiglia di disporre di
spugnette e di un elettrodo di ricambio.
Depositi di calcare possono accumularsi sulle superfici metalliche degli
elettrodi. Tali depositi avranno un effetto isolante. Al fine di mantenere una
conducibilità ottimale, queste superfici devono essere pulite e lucidate
regolarmente.
Cavi vuoto
Pulire il cavo del vuoto con un panno umido. Non usare una soluzione alcolica.
Controllare regolarmente che il cavo non sia danneggiato e/o abbia un
contatto elettrico staccato. Vi consigliamo di tenere a magazzino un cavo del
vuoto di riserva.
Pulire il
serbatoio
dell'acqua e le
tubazioni
• Staccare le coppe sotto vuoto dai cavi del vuoto.
• Mettere un contenitore riempito di liquido di pulizia (*) sotto al sistema.
• Mettere i terminali periferici dei cavi nel contenitore.
• Andare alle Impostazioni di sistema e selezionare Pulizia serbatoio.
• Il serbatoio dell'acqua verrà riempito con il liquido di pulizia fino a quando
il serbatoio dell'acqua non sarà pieno.
• Svuotare il serbatoio dell'acqua come descritto di seguito (serbatoio
dell'acqua pieno).
(*) I seguenti prodotti registrati possono essere usati per disinfettare il serbatoio dell'acqua:
BAKTONIL, BAKTOLAN al 5%, CHINOSOL all’1%, CHLORAMIN soluzione, DETTOL, ELMOCID Gamma
al 2%, PERODIN, ZEPHIROL al 5%.
Osservare le informazioni di applicazione del produttore corrispondente.
Risoluzione dei problemi
Il dispositivo non deve essere utilizzato quando si notano danni meccanici. Ciò include
l'isolamento del cavo danneggiato.
Nel caso in cui compaia un messaggio di errore o un’avvertenza, interrompere
immediatamente qualsiasi utilizzo del dispositivo. Spegnere e riaccendere il dispositivo. Se il
problema persiste, contattare il fornitore Enraf-Nonius B.V. per l’assistenza. Gli errori e le
avvertenze indicano un problema interno al dispositivo che deve essere verificato da un
tecnico dell’assistenza certificato da Enraf-Nonius B.V prima di qualsiasi successivo utilizzo o
funzionamento del sistema.
L’utilizzo di un dispositivo indicante un errore o un’avvertenza può comportare rischi di
lesioni al paziente e all’utente oppure danni interni di notevole entità al sistema.
In caso di guasto allo schermo o altri difetti ovvi, scollegare immediatamente il dispositivo e
contattare un tecnico dell’assistenza certificato.
In caso di ingresso di liquidi, scollegare il dispositivo dalla rete elettrica e farlo controllare da
una persona autorizzata.

Pagina 46 di 52 IT109-1634750-40 IFU
Messaggi di errore
All'accensione, il dispositivo esegue prima un autotest. Quando viene rilevato un errore, sia durante
l'autotest che durante il normale funzionamento, sul display apparirà una schermata pop-up.
Quando viene visualizzato l'errore, tutte le uscite saranno disabilitate. Quando si verifica questa
situazione, spegnere l'unità e scollegare tutti gli accessori. Attendere circa 15 secondi e riaccendere
l'unità.
Quando l'errore ricompare, interrompere l'uso dell'apparecchio e contattare il fornitore.
Il dispositivo deve raffreddarsi prima di procedere
La temperatura del dispositivo è troppo elevata per iniziare il trattamento. Rimuovere il dispositivo
da qualsiasi potenziale fonte di calore (come la luce solare diretta) e farlo raffreddare. Riavviare il
dispositivo per continuare.
Insufficienza o mancanza di corrente d’uscita
• Controllare che il cavo del paziente non sia rotto o non abbia un cattivo contatto.
• Assicurarsi che le spugne siano sufficientemente umide.
• Pulire gli elettrodi
• Controllare se il contatto è insufficiente
• Nelle zone in cui l'acqua è dolce, è possibile che l'acqua conduca male, con conseguenti
correnti anormalmente basse. In questo caso è possibile utilizzare una soluzione salina per
migliorare la conducibilità dell'acqua.
Serbatoio dell'acqua pieno
Il serbatoio di separazione dell'acqua del modulo vuoto è pieno. Continuare il trattamento con gli
elettrodi standard o svuotare il serbatoio come segue:
• Impostare l'interruttore della linea di alimentazione [17] Spento (0).
• Scollegare il tubo flessibile dal raccordo più esterno [21] e svuotare il serbatoio.
• Riattaccare il tubo al raccordo.
• Impostare l'interruttore della linea di alimentazione [17] Acceso (1).
Perdita del vuoto
C'è probabilmente una perdita nel sistema del vuoto. Questo errore è di solito preceduto da una
pompa che gira di continuo cercando di raggiungere il vuoto impostato. Per proteggere il sistema
la pompa viene fermata automaticamente dopo un certo periodo di tempo. Ispezionare i cavi del
vuoto e gli elettrodi, reimpostare il vuoto sullo zero e riprovare. Se l'errore persiste, sospendere
l'utilizzo del dispositivo e contattare il proprio fornitore.

Pagina 47 di 52 IT109-1634750-40 IFU
Si consiglia inoltre di tenere un registro degli interventi. In alcuni paesi questa pratica è obbligatoria.
Su richiesta è possibile mettere a disposizione un manuale di manutenzione contenente: l’elenco
delle parti di ricambio, le istruzioni sulla calibrazione e altre informazioni che assisteranno il
personale tecnico qualificato dell’utente nelle operazioni di riparazione di quelle parti
dell’apparecchio che sono state concepite dal produttore per essere riparate.
Vita utile prevista
Questo dispositivo sarà adeguato all’utilizzo previsto fino a quando sarà sottoposto a manutenzione
annuale da parte di un tecnico qualificato del servizio assistenza, come descritto nel manuale di
manutenzione. Il tecnico del servizio assistenza deciderà se il dispositivo è idoneo ad essere utilizzato
in base alle specifiche.
Fine durata
Il dispositivo contiene materiali riciclabili e/o dannosi per l'ambiente.
Manutenzione tecnica
L’apertura dell’apparecchio da parte di agenzie non autorizzate non è consentita e porrà fine
a qualsiasi diritto di garanzia.
Il produttore declina ogni responsabilità per le conseguenze di interventi di riparazione o di
manutenzione svolti da personale non autorizzato!
Solo i tecnici del servizio assistenza autorizzati da Enraf-Nonius possono eseguire la
manutenzione o modificare questo apparecchio secondo le informazioni indicate dal servizio
assistenza.
Non si deve effettuare alcuna manutenzione sul dispositivo quando esso è in uso o è
collegato a un paziente.
Si raccomanda di far controllare annualmente l'Endomed 182 da personale autorizzato di
Enraf-Nonius o dal suo distributore autorizzato.
Informarsi debitamente sulle leggi e sulle norme locali relative allo smaltimento di
apparecchiature e accessori.

Pagina 48 di 52 IT109-1634750-40 IFU
13 Specifiche
Dati technici
Dati elettrici
Alimentazione
100 - 240 Volt
Frequenza
50/60 Hz
Potenza massima in uscita
50 VA
Dimensioni (larghezza x lunghezza x
altezza)
Endomed 182 Tipo 1
14,5 x 17 x 9 cm
Endomed 182 Tipo 2
14 x 16 x 14 cm
Endomed 182 Tipo 3
14 x 22,5 x 17,5 cm
Questi valori rappresentano le dimensioni delle
custodie senza cavi di comunicazione, elettrodi o tubi
flessibili.
Peso unità
Endomed 182 Tipo 1
710 grammi
Endomed 182 Tipo 2
1460 grammi
Endomed 182 Tipo 3
2750 grammi
Questi valori rappresentano il peso delle custodie
senza elettrodi e cavi di alimentazione.
Specifiche Tipo 1
Canali
1
Uscita
Corrente costante
Corrente continua
Polarità
Negativo
Intensità
0 – 15 mA
Tempo di trattamento
0 – 300 secondi
Specifiche Tipo 2 e 3
Canali
2
Uscita
Corrente costante
Intensità
0 -100 mA
Timer
0 – 60 min (a passi di 1 min.)
Interferenziale bipolare
Onda portante
4 kHz
Frequenza AMF
1 – 200 Hz
Frequenza di modulazione
0 – 180 Hz
Programmi di modulazione
1-1, 6-6, 1-30 secondi
Interferenziale quadripolare e Vettore
isoplanare
Onda portante
4 kHz
Frequenza AMF
1 – 200 Hz
Frequenza di modulazione
0 – 180 Hz
Programmi di modulazione
1-1, 6-6, 1-30 secondi

Pagina 49 di 52 IT109-1634750-40 IFU
Corrente pulsata bifasica asimmetrica (TENS)
Larghezza d'impulso
150 μs
Frequenza
1 – 200 Hz
Frequenza di modulazione
0 – 180 Hz
Programmi di modulazione
1-1, 6-6, 1-30 secondi
Frequenza di burst
1-2-4 Hz
Sono riservate modifiche tecniche
Sicurezza e standard delle prestazioni
Classificazione dispositivo medicale
IIa; Regola 9, Allegato IX della Direttiva 93/42/CEE
Questa apparecchiatura è conforme a tutti i requisiti
della Direttiva 93/42/CEE sui dispositivi medici.
Classe di sicurezza conforme a IEC
60601-1
Classe di sicurezza elettrica I
Modalità di funzionamento
Continuo
Parti applicate
Parte applicata di tipo BF per l’elettroterapia.
Prestazioni essenziali
Le prestazioni essenziali si basano sullo standard 60601-2-10, che specifica il livello massimo di
uscita della corrente e dell'energia dell'impulso. Considerando le diverse tipologie di terapia, le
prestazioni essenziali sono ricavate da cinque requisiti:
1) La radice della media quadratica della corrente TENS massima non deve essere superiore a
50 mA
2) La radice della media quadratica della corrente interferenziale massima non deve essere
superiore a 100 mA
3) L'energia dell'impulso TENS massimo non deve essere superiore a 300 mJ
4) L'energia dell'impulso interferenziale massimo non deve essere superiore a 300 mJ
5) La radice della media quadratica della corrente continua massima non deve essere
superiore a 80 mA.
Le uscite per l’elettroterapia rimarranno entro il 20% del valore impostato.
Poiché non si tratta di un dispositivo di sopravvivenza, è contemplato che possa passare a uno stato
di sicurezza (nessuna uscita), richiedendo l’intervento dell’operatore per il riavvio.
Condizioni ambientali
Condizioni ambientali per il trasporto e la conservazione
Temperatura ambiente:
da -10° a +70 °C
Umidità relativa:
da 10 a 90% (senza condensa)
Pressione atmosferica:
da 500 a 1060 hPa
Condizioni ambientali per il normale utilizzo
Temperatura ambiente:
da 10° a 40 °C
Umidità relativa:
da 10 a 90% (senza condensa)
Pressione atmosferica:
da 800 a 1060 hPa

Pagina 50 di 52 IT109-1634750-40 IFU
Dettagli sulla compatibilità elettromagnetica
I dispositivi elettromedicali come Endomed 182 sono soggetti a speciali misure precauzionali
per quanto riguarda la compatibilità elettromagnetica (EMC) e devono essere installati e messi
in funzione in conformità alle istruzioni EMC fornite nelle istruzioni per l’uso.
Evitare l’uso di questo apparecchio vicino o accatastato su altri apparecchi, per non
comprometterne il funzionamento. Se tale utilizzo è necessario, osservare questo apparecchio
e l’altro apparecchio per verificare che funzionino normalmente.
L'uso di accessori, trasduttori e cavi diversi da quelli specificati o forniti dal produttore potrebbe
determinare un aumento delle emissioni elettromagnetiche o una ridotta immunità
elettromagnetica dell’apparecchio e comprometterne il funzionamento.
Sistemi di comunicazione RF portatili (ad esempio periferiche come i cavi dell’antenna e le
antenne esterne) non devono essere utilizzati a una distanza minore di 30 cm da qualsiasi
componente di Endomed 182, inclusi i cavi specificati dal produttore. In caso contrario è
possibile che si verifichino anomalie nelle prestazioni di questo apparecchio.
Il dispositivo Endomed 182 deve essere utilizzato solo con il cavo di alimentazione originale
specificato nell’elenco dei contenuti forniti. L’utilizzo del dispositivo con un qualsiasi altro
cavo di alimentazione può causare l’aumento delle emissioni o la riduzione dell’immunità alle
interferenze del dispositivo.
Il dispositivo Endomed 182 è classificato come appartenente al Gruppo 1, Classe B ai sensi del
CISPR 11.
Il dispositivo Endomed 182 è idoneo per essere utilizzato in un ambiente di strutture sanitarie
professionali. Il dispositivo utilizza energia RF solo per le funzioni interne. Pertanto, le emissioni RF
sono molto basse ed è improbabile che causino interferenze ad apparecchi elettronici situati nelle
vicinanze.
Endomed 182 è stato testato ai sensi della norma 60601-1-2 da un laboratorio accreditato ed è
stato considerato conforme a qualsiasi norma o test su emissioni e immunità.

Pagina 51 di 52 IT109-1634750-40 IFU
14 Contatti
Per assistenza visitare il nostro sito Web http://www.enraf-nonius.com
La versione più aggiornata (in formato digitale o cartaceo) delle presenti istruzioni per l’uso è
disponibile gratuitamente visitando il nostro sito Web www.enraf-nonius.com, contattando il
distributore o chiamando il numero: +31-(0)10-2030600. Le istruzioni per l’uso verranno inviate
(gratuitamente) entro 7 (sette) giorni di calendario.
15 Responsabilità per il prodotto
In molti Paesi è in vigore una legge che disciplina la responsabilità per il prodotto. Tale legge sulla
responsabilità del prodotto implica, tra l'altro, che una volta trascorso un periodo di 10 anni
dall'immissione in commercio di un prodotto, il produttore non può più essere ritenuto
responsabile per eventuali carenze del prodotto.
Nella misura massima consentita dalla legge applicabile, Enraf-Nonius e i suoi fornitori o rivenditori
non saranno in alcun caso ritenuti responsabili per danni indiretti, speciali, accidentali o
consequenziali derivanti dall'uso o dall'impossibilità di utilizzare il prodotto, inclusi, senza
limitazione, i danni all'immagine e le perdite di lavoro e produttività, errori informatici o
malfunzionamenti o qualsiasi altro danno o perdita commerciale, anche se ne è stata notificata la
possibilità e indipendentemente dal principio legale o giuridico (contratto, infrazione o altro) su cui
si basa la richiesta. In ogni caso, l'intera responsabilità di Enraf-Nonius in virtù di qualsiasi
disposizione del presente accordo non deve superare complessivamente la somma dell'importo
pagato per questo prodotto e l'importo dell'assistenza per il prodotto ricevuta da Enraf-Nonius in
base ad un (eventuale) accordo di assistenza separato, ad eccezione di morte o lesioni personali
causate dalla negligenza di Enraf-Nonius nella misura in cui la legge applicabile vieti la limitazione
dei danni in tali casi.
La controparte (l’utente del prodotto o il suo rappresentante) esonererà Enraf-Nonius da qualsiasi
richiesta derivante da terzi, indipendentemente dalla natura o da qualsiasi rapporto con la
controparte.

IT109-1634750-40
Copyright:
Enraf-Nonius B.V.
Vareseweg 127 | 3047 AT | Rotterdam | Paesi Bassi
Tel: +31 (0)10-20 30 600 | [email protected]
-
 1
1
-
 2
2
-
 3
3
-
 4
4
-
 5
5
-
 6
6
-
 7
7
-
 8
8
-
 9
9
-
 10
10
-
 11
11
-
 12
12
-
 13
13
-
 14
14
-
 15
15
-
 16
16
-
 17
17
-
 18
18
-
 19
19
-
 20
20
-
 21
21
-
 22
22
-
 23
23
-
 24
24
-
 25
25
-
 26
26
-
 27
27
-
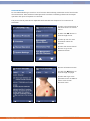 28
28
-
 29
29
-
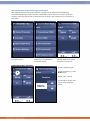 30
30
-
 31
31
-
 32
32
-
 33
33
-
 34
34
-
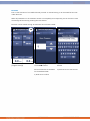 35
35
-
 36
36
-
 37
37
-
 38
38
-
 39
39
-
 40
40
-
 41
41
-
 42
42
-
 43
43
-
 44
44
-
 45
45
-
 46
46
-
 47
47
-
 48
48
-
 49
49
-
 50
50
-
 51
51
-
 52
52
-
 53
53
-
 54
54
-
 55
55
-
 56
56
-
 57
57
-
 58
58
-
 59
59
-
 60
60
-
 61
61
-
 62
62
-
 63
63
-
 64
64
-
 65
65
-
 66
66
-
 67
67
-
 68
68
-
 69
69
-
 70
70
-
 71
71
-
 72
72
-
 73
73
-
 74
74
-
 75
75
-
 76
76
-
 77
77
-
 78
78
-
 79
79
-
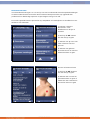 80
80
-
 81
81
-
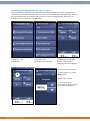 82
82
-
 83
83
-
 84
84
-
 85
85
-
 86
86
-
 87
87
-
 88
88
-
 89
89
-
 90
90
-
 91
91
-
 92
92
-
 93
93
-
 94
94
-
 95
95
-
 96
96
-
 97
97
-
 98
98
-
 99
99
-
 100
100
-
 101
101
-
 102
102
-
 103
103
-
 104
104
-
 105
105
-
 106
106
-
 107
107
-
 108
108
-
 109
109
-
 110
110
-
 111
111
-
 112
112
-
 113
113
-
 114
114
-
 115
115
-
 116
116
-
 117
117
-
 118
118
-
 119
119
-
 120
120
-
 121
121
-
 122
122
-
 123
123
-
 124
124
-
 125
125
-
 126
126
-
 127
127
-
 128
128
-
 129
129
-
 130
130
-
 131
131
-
 132
132
-
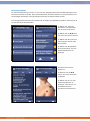 133
133
-
 134
134
-
 135
135
-
 136
136
-
 137
137
-
 138
138
-
 139
139
-
 140
140
-
 141
141
-
 142
142
-
 143
143
-
 144
144
-
 145
145
-
 146
146
-
 147
147
-
 148
148
-
 149
149
-
 150
150
-
 151
151
-
 152
152
-
 153
153
-
 154
154
-
 155
155
-
 156
156
-
 157
157
-
 158
158
-
 159
159
-
 160
160
-
 161
161
-
 162
162
-
 163
163
-
 164
164
-
 165
165
-
 166
166
-
 167
167
-
 168
168
-
 169
169
-
 170
170
-
 171
171
-
 172
172
-
 173
173
-
 174
174
-
 175
175
-
 176
176
-
 177
177
-
 178
178
-
 179
179
-
 180
180
-
 181
181
-
 182
182
-
 183
183
-
 184
184
-
 185
185
-
 186
186
-
 187
187
-
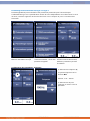 188
188
-
 189
189
-
 190
190
-
 191
191
-
 192
192
-
 193
193
-
 194
194
-
 195
195
-
 196
196
-
 197
197
-
 198
198
-
 199
199
-
 200
200
-
 201
201
-
 202
202
-
 203
203
-
 204
204
-
 205
205
-
 206
206
-
 207
207
-
 208
208
-
 209
209
-
 210
210
-
 211
211
-
 212
212
-
 213
213
-
 214
214
-
 215
215
-
 216
216
-
 217
217
-
 218
218
-
 219
219
-
 220
220
-
 221
221
-
 222
222
-
 223
223
-
 224
224
-
 225
225
-
 226
226
-
 227
227
-
 228
228
-
 229
229
-
 230
230
-
 231
231
-
 232
232
-
 233
233
-
 234
234
-
 235
235
-
 236
236
-
 237
237
-
 238
238
-
 239
239
-
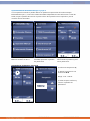 240
240
-
 241
241
-
 242
242
-
 243
243
-
 244
244
-
 245
245
-
 246
246
-
 247
247
-
 248
248
-
 249
249
-
 250
250
-
 251
251
-
 252
252
-
 253
253
-
 254
254
-
 255
255
-
 256
256
-
 257
257
-
 258
258
-
 259
259
-
 260
260
-
 261
261
-
 262
262
-
 263
263
-
 264
264
-
 265
265
-
 266
266
-
 267
267
-
 268
268
-
 269
269
-
 270
270
-
 271
271
-
 272
272
-
 273
273
-
 274
274
-
 275
275
-
 276
276
-
 277
277
-
 278
278
-
 279
279
-
 280
280
-
 281
281
-
 282
282
-
 283
283
-
 284
284
-
 285
285
-
 286
286
-
 287
287
-
 288
288
-
 289
289
-
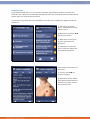 290
290
-
 291
291
-
 292
292
-
 293
293
-
 294
294
-
 295
295
-
 296
296
-
 297
297
-
 298
298
-
 299
299
-
 300
300
-
 301
301
-
 302
302
-
 303
303
-
 304
304
-
 305
305
-
 306
306
-
 307
307
-
 308
308
-
 309
309
-
 310
310
-
 311
311
-
 312
312
-
 313
313
-
 314
314
Enraf-Nonius CD-ROM Endomed 182 Manual de usuario
- Tipo
- Manual de usuario
en otros idiomas
Artículos relacionados
-
Enraf-Nonius CD-ROM Endomed 182 Manual de usuario
-
Enraf-Nonius CD-ROM Endomed 182 Manual de usuario
-
Enraf-Nonius CD-ROM COMPACT-II Manual de usuario
-
Enraf-Nonius Endomed 182 Manual de usuario
-
Enraf-Nonius Endomed 481/482/484 Manual de usuario
-
Enraf-Nonius Tecarpuls Manual de usuario
-
Enraf-Nonius Curapuls Manual de usuario
-
Enraf-Nonius Tree P Manual de usuario
-
Enraf-Nonius Tecarpuls-II Manual de usuario
-
Enraf-Nonius CD-ROM COMPACT-II Manual de usuario
Otros documentos
-
 TensCare TENS ONE Manual de usuario
TensCare TENS ONE Manual de usuario
-
Beurer EM44 El manual del propietario
-
Axion STIM-PRO T-400 Manual de usuario
-
Sharper Image Cordless T.E.N.S. Massager El manual del propietario
-
Drive Medical Padded Swivel Seat Cushion Manual de usuario
-
 TensCare Perfect EMS Manual de usuario
TensCare Perfect EMS Manual de usuario
-
 TensCare Sports TENS 2 Manual de usuario
TensCare Sports TENS 2 Manual de usuario
-
Medisana TDP El manual del propietario
-
Gima 33525 El manual del propietario
-
 Weelko U-Tech F803 El manual del propietario
Weelko U-Tech F803 El manual del propietario





























































































































































































































































































































