Roche uPath PD-L1 image analysis for NSCLC IVD Algorithm Manual de usuario
- Tipo
- Manual de usuario

Guía de algoritmos
del análisis de imagen uPath PD-L1
(SP263) para el cáncer pulmonar no
microcítico


Tabla de contenido
Introducción 1
Resumen y explicación del algoritmo 2
Uso previsto 3
Uso previsto del producto 3
Objetivo de la Guía de algoritmos 3
Importancia clínica 4
Principios de la prueba 5
Limitaciones 6
Seguridad de los datos 7
Flujo de trabajo para usar el algoritmo de análisis de imagen
uPath PD-L1 para NSCLC 8
Flujo de trabajo del anatomopatólogo 9
Análisis de imagen PD-L1 12
Evaluación de PD-L1 15
Evaluación de la tinción del algoritmo PD-L1 15
Características de la tinción 15
Características de rendimiento 26
Comparación de métodos 26
Estudios de reproducibilidad de anatomopatólogos 27
Estudios de reproducibilidad de los escáneres 28
Resolución de problemas 29
Bibliografía 33


Introducción
El Roche uPath enterprise software (uPath enterprise software)
junto con el algoritmo de análisis de imagen uPath PD-L1
(SP263) para el cáncer pulmonar no microcítico (NSCLC)
(algoritmo de análisis de imagen uPath PD-L1 (SP263) para
NSCLC) es un sistema de software diseñado para ayudar en la
evaluación cuantitativa de la expresión de proteínas en secciones
histológicas teñidas inmunohistoquímicamente (IHC) de tejidos
normales y neoplásicos fijados con formol y embebidos en
parafina (FFPE).
El uPath enterprise software es una solución integral de software
de patología digital que permite a los laboratorios de patología
adquirir, administrar, observar, analizar, compartir e informar sobre
imágenes digitales de muestras de patología. Usando el uPath
enterprise software, el anatomopatólogo puede ver imágenes
digitales con diferentes aumentos, añadir anotaciones, realizar
mediciones de secciones de tejido, realizar análisis de imágenes y
generar informes.
Nota: El algoritmo de análisis de imagen uPath PD-L1 (SP263)
para NSCLC es una metodología complementaria asistida por
ordenador para ayudar en la adquisición y medición de imágenes
procedentes de portaobjetos de vidrio para microscopio de
muestras de tejido teñidas con IHC para detectar la presencia de
la proteína PD-L1. Para garantizar la validez de las puntuaciones
del análisis de imágenes, es responsabilidad del anatomopatólogo
verificar la concordancia mediante el uso de los controles
apropiados como se especifica en la hoja de método de VENTANA
PD-L1 (SP263) Rabbit Monoclonal Primary Antibody
(disponible en www.ventana.com).
Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC) 1

2 Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC)
Resumen y explicación del algoritmo
Para las aplicaciones de análisis de imágenes, el
anatomopatólogo puede utilizar el uPath enterprise software para
seleccionar y destacar una o varias regiones de interés (ROI);
cada ROI se puede observar con varios aumentos y analizarse
después mediante el algoritmo de análisis de imagen uPath PD-L1
(SP263) para NSCLC. Se genera un recuento del número total de
TC en estudio y las células tumorales (TC) se estratifican según
estén teñidas o no. El algoritmo de análisis de imagen uPath
PD-L1 (SP263) para NSCLC divide las TC teñidas por el número
total de TC (teñidas y sin teñir) para generar la puntuación
de positividad de TC de PD-L1 en una escala del 0 al 100 %.
El algoritmo de análisis de imagen uPath PD-L1 (SP263) para
NSCLC puede generar una puntuación para un ROI particular
o una puntuación añadida para todas las ROI seleccionadas
en ese portaobjetos. Aunque el algoritmo detecta células no
tumorales como parte del análisis general, la superposición
y la salida solo muestran las TC utilizadas en el cálculo de la
puntuación de positividad de TC. El anatomopatólogo puede
aceptar la puntuación proporcionada por el algoritmo de análisis
de imagen uPath PD-L1 (SP263) para NSCLC, o bien puede
asignar una puntuación diferente. El anatomopatólogo debe
revisar cuidadosamente lo que el algoritmo ha marcado como
TC positivas y negativas, así como confirmar que el algoritmo es
correcto o bien realizar una asignación manual. El algoritmo de
análisis de imagen uPath PD-L1 (SP263) para NSCLC no realiza
interpretaciones independientes de los datos y, por lo tanto,
solo un anatomopatólogo con formación debe utilizarlo junto
con el examen histológico, la información clínica relevante y los
controles adecuados. Está diseñado e indicado como ayuda para
el anatomopatólogo en la evaluación de la expresión de PD-L1 al
50 %.

Uso previsto
Objetivo de la Guía de algoritmos
Esta Guía de algoritmos del análisis de imagen uPath PD-L1
(SP263) para NSCLC (Guía de algoritmos) se utiliza para:
• Proporcionar información básica sobre el uso previsto del
algoritmo de análisis de imagen uPath PD-L1 (SP263) para
NSCLC, principios de la prueba y limitaciones.
• Definir los materiales necesarios y los requisitos informáticos,
de seguridad de datos y de red.
• Mostrar las instrucciones paso a paso para ejecutar el
algoritmo de análisis de imagen uPath PD-L1 (SP263) para
NSCLC.
• Proporcionar imágenes fotográficas que ilustren cómo se debe
utilizar el algoritmo de análisis de imagen uPath PD-L1 (SP263)
para NSCLC.
• Proporcionar a los anatomopatólogos una herramienta para
facilitar el uso del algoritmo de análisis de imagen uPath PD-L1
(SP263) para NSCLC en secciones de NSCLC FFPE teñidas
con el VENTANA PD-L1 (SP263) Assay.
• Proporcionar imágenes de ejemplo de casos difíciles para
proporcionar orientación sobre cómo usar el algoritmo de
análisis de imagen uPath PD-L1 (SP263) para NSCLC en su
evaluación.
• Mostrar las características de rendimiento del algoritmo de
análisis de imagen uPath PD-L1 (SP263) para NSCLC.
Uso previsto del producto
El algoritmo de análisis de imagen uPath PD-L1 (SP263)
para NSCLC está previsto para su uso como ayuda para el
anatomopatólogo en la detección y medición semicuantitativa de
la proteína PD-L1 en tejido NSCLC fijado con formol y embebido
en parafina. Cuando se usa con el VENTANA PD-L1 (SP263)
Assay, está indicado para su uso como ayuda en la identificación
de pacientes con NSCLC para el tratamiento con terapias con
una línea de corte para la positividad de TC de PD-L1 ≥ 50 % de
acuerdo con la ficha técnica autorizada del producto terapéutico.
Nota: El análisis de imagen uPath PD-L1 (SP263) para NSCLC es
una metodología complementaria asistida por ordenador para
ayudar en la adquisición y medición de imágenes procedentes
de portaobjetos de vidrio para microscopio de muestras de tejido
teñidas con IHC para detectar la presencia de la proteína PD-L1.
Para garantizar la validez de las puntuaciones del análisis de
imágenes, es responsabilidad del anatomopatólogo verificar la
concordancia y usar controles apropiados como se especifica
en la hoja de método del VENTANA PD-L1 (SP263) Assay
(ref. 741-4905).
Este algoritmo es para uso diagnóstico in vitro (IVD).
Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC) 3

Importancia clínica
El cáncer de pulmón es, desde hace varias décadas, el cáncer
más común y la principal causa de muerte relacionada con esta
enfermedad a nivel mundial. Se estima que representa el 12,9 %
de todos los nuevos casos de cáncer y causa casi 1,76 millones de
muertes al año en todo el mundo o, lo que es lo mismo una de cada
cinco muertes relacionadas con el cáncer. El NSCLC es el tipo más
común de cáncer de pulmón y representa aproximadamente el 85 %
de todos los casos de cáncer de pulmón. La mayoría de los pacientes
con NSCLC presentan una enfermedad localmente avanzada e
inoperable (Estadio IIIB) o metastásica (Estadio IV). No existen
opciones de tratamiento curativo para ninguna de los dos. El índice de
supervivencia relativo a 5 años para el NSCLC avanzado es del 4,7%.
El ligando 1 de muerte programada (PD-L1) es una proteína
transmembran
a expresada en linfocitos T activados que regula por
disminución la respuesta inmunitaria mediante la unión a sus dos
receptores inhibidores de muerte programada-1 (PD-1) y B7-1 (CD80).
La unión de PD-L1 con PD-1 inhibe la proliferación de los linfocitos
T, la producción de citoquinas y la actividad citolítica, dando lugar a
la inactivación funcional o agotamiento de los linfocitos T. Además,
PD-L1 se une con CD80 en las células que presentan antígeno y en los
linfocitos T activados mediando en la regulación por disminución de la
respuesta inmunitaria, incluida la inhibición de la activación de linfocitos
T y la producción de citoquina. Se ha observado la expresión de PD-
L1 en células inmunitarias y TC. Se ha detectado que la expresión
aberrante de PD-L1 en TC obstaculiza la inmunidad antitumoral, dando
como resultado la evasión inmunitaria. Se ha demostrado que la
aparición de inmunoterapias que interrumpen la vía PD-L1/PD-1 mejora
las tasas de supervivencia de los pacientes diagnosticados con NSCLC.
Sin embargo, el pronóstico con el tratamiento depende del nivel de
expresión de PD-L1 y, por lo tanto, requiere la cuantificación de PD-L1
con tinción inmunohistoquímica.
La inmunohistoquímica se puede utilizar para detectar antígenos
específicos presentes en muestras de tejido, lo que la convierte en una
herramienta eficaz para que los anatomopatólogos la utilicen en su
diagnóstico y pronóstico de carcinomas. El VENTANA PD-L1 (SP 263)
Assay es un anticuerpo monoclonal de conejo previsto para su uso
en laboratorio para la detección semicuantitativa de la proteína PD-L1
en secciones de tejidos normales y neoplásicos FFPE. Una ventaja de
las preparaciones de tejido histológicas es que la morfología del tejido
intacto permite que contribuya a la interpretación de la positividad para
la PD-L1 de la muestra del paciente. Los análisis histológicos deben ser
interpretados por un especialista en morfología y/o patología del NSCLC.
Los resultados se deben complementar con estudios morfológicos y
controles adecuados y deben usarse junto con otros datos clínicos y de
laboratorio.
4 Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC)

Principios de la prueba
El uPath enterprise software con el algoritmo de análisis de imagen
uPath PD-L1 (SP263) para NSCLC emplea técnicas de análisis de
imagen para obtener una puntuación de positividad de TC.
El algoritmo de análisis de imagen uPath PD-L1 (SP263) para
NSCLC utiliza parámetros predefinidos para puntuar imágenes
del tejido teñido con el VENTANA PD-L1 (SP263) Assay.
Pasos implicados en el análisis de imágenes:
• Identificación de espacios en blanco y exclusión automática
del análisis.
• Detección de células en toda la imagen.
• Clasificación de células como TC u otros tipos de células.
• Identificación de TC teñidas frente a no teñidas.
• Cálculo de la puntuación de positividad de TC dividiendo el
número de TC teñidas por el número total de TC de acuerdo
con la hoja de método del VENTANA PD-L1 (SP263) Assay.
Cómo identifica las TC el algoritmo de análisis de imagen
uPath PD-L1 (SP263) para NSCLC y cómo se calcula la
puntuación:
• El algoritmo de análisis de imagen uPath PD-L1 (SP263) para
NSCLC identifica las TC usando color, intensidad, tamaño y
características morfológicas.
• Las TC identificadas se clasifican como teñidas usando la
membrana detectada y los umbrales preestablecidos que
están en sintonía con la hoja de método del VENTANA PD-L1
(SP263) Assay.
• Para calcular el porcentaje de TC teñidas, se divide el número
de TC teñidas por el número total de TC de acuerdo con la hoja
de método del VENTANA PD-L1 (SP263) Assay.
Determinación de espacios en blanco del algoritmo de
análisis de imagen uPath PD-L1 (SP263) para NSCLC:
• El algoritmo excluirá automáticamente los espacios en blanco.
Los artefactos tales como suciedad, arañazos o tinta no se
pueden excluir automáticamente.
• El usuario puede revisar las áreas determinadas por
el algoritmo como espacios en blanco utilizando una
superposición falsa de colores; consulte «Análisis de imagen
PD-L1: superposición falsa de colores».
Criterios del algoritmo de análisis de imagen uPath PD-
L1 (SP263) para NSCLC para generar la salida de la
puntuación de positividad de TC:
• El algoritmo de análisis de imagen uPath PD-L1 (SP263) para
NSCLC notificará una puntuación de un decimal, por ejemplo,
«4,8%».
• No se recomienda redondear la puntuación hacia arriba o
hacia abajo. Por ejemplo, «4,8%» no debe redondearse a 5%.
Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC) 5

El algoritmo de análisis de imagen uPath PD-L1 (SP263) para
NSCLC está diseñado para funcionar con el VENTANA PD-L1
(SP263) Assay. Los resultados de la prueba son tan buenos como
la calidad y precisión del portaobjetos IHC que se muestra en la
imagen, y la imagen posterior que se analiza.
El anatomopatólogo debe validar la sesión de tinción del
VENTANA PD-L1 (SP263) Assay realizado mediante un examen
microscópico manual de los portaobjetos de control PD-L1 para
verificar que se hayan obtenido los resultados esperados antes de
acceder a las imágenes de los portaobjetos en el uPath enterprise
software para su análisis.
Se deben seguir las recomendaciones del fabricante del
VENTANA PD-L1 (SP263) Assay, incluidos todos los materiales de
control de calidad positivo y negativo para cada sesión de tinción.
Si los portaobjetos de control no son aceptables con el examen
microscópico manual, vuelva a teñir el tejido con resultados
aceptables.
El anatomopatólogo debe seguir las recomendaciones para la
interpretación del VENTANA PD-L1 (SP263) Assay.
Consulte la hoja de método del VENTANA PD-L1 (SP263) Assay
(P/N 1014258ES) y la guía de interpretación (ref. 1015317EN)
(disponibles en www.ventana.com).
El algoritmo de análisis de imagen uPath PD-L1 (SP263) para
NSCLC está diseñado para que sea un anatomopatólogo con
formación el que lo use junto con un examen histológico,
información clínica importante y controles adecuados. No está
diseñado para ser una herramienta independiente; es necesaria
la intervención humana competente durante todo el proceso de
análisis.
El algoritmo de análisis de imagen uPath PD-L1 (SP263) para
NSCLC puede generar puntuaciones incorrectas si las imágenes
capturadas tienen una tinción anormal (nuclear, citoplasmática,
etc.).
El algoritmo de análisis de imagen uPath PD-L1 (SP263)
para NSCLC rechazará núcleos tumorales alargados
independientemente de la forma general de la célula. Por esta
razón, los que contienen grandes cantidades de células con
núcleos alargados pueden precisar su evaluación manual.
Limitaciones
El algoritmo de análisis de imagen uPath PD-L1 (SP263) para
NSCLC se ha preparado, desarrollado y validado en muestras de
tejido de NSCLC.
El algoritmo de análisis de imagen uPath PD-L1 (SP263) para
NSCLC no se ha probado, como tampoco se ha validado su
seguridad y eficacia, cuando se utiliza con un ordenador personal
(PC) desde casa.
El algoritmo de análisis de imagen uPath PD-L1 (SP263) está
indicado para su uso como ayuda en la identificación de
pacientes con NSCLC para el tratamiento con terapias con una
línea de corte para la positividad de TC de PD-L1 del 50% de
acuerdo con la ficha técnica autorizada del producto terapéutico.
El algoritmo de análisis de imagen uPath PD-L1 (SP263) para
NSCLC puede identificar incorrectamente las células debido
a la presencia de una tinción citoplasmática y/o membranosa
débil, una tinción fuerte de las células inmunitarias que se solapa
con la tinción de células tumorales donde hay una inflamación
entremezclada significativa, TC con rubor citoplasmático, y tinción
de no dianas. Esto puede suponer la identificación errónea de TC
como no TC, y de no TC como TC positivo.
Aunque es necesario que los macrófagos estén excluidos de
la región de análisis, no siempre es posible excluir todos los
macrófagos. Como resultado, la puntuación generada por el
algoritmo de análisis de imagen uPath PD-L1 (SP263) para NSCLC
puede verse influenciada por los macrófagos en la ROI que se
analiza. Esto es imprescindible cuando la puntuación de un
paciente está cerca de la línea de corte del 50%.
La tinción citoplasmática generalmente es difusa y algunos
casos presentan una calidad granular fina. Algunos casos
excepcionales han presentado una tinción de los cuerpos
puntiformes perinucleares con intensidad variable. El porcentaje
total de las intensidades de la señal de la membrana tumoral se
estima visualmente y se utiliza para generar el nivel de expresión
de PD-L1. La tinción citoplasmática de células tumorales no se
tiene en cuenta para determinar la expresión de PD-L1. Se utiliza
un anticuerpo de control negativo compatible con isotipo para
evaluar la presencia de fondo en las muestras de la prueba y
establecer una línea de base de la intensidad de tinción.
6 Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC)

Seguridad de los datos
La presencia de software malintencionado o un acceso no
autorizado al instrumento puede dar lugar a una pérdida de datos
o dejar el instrumento inutilizable.
Para evitar infecciones por un software malintencionado, así
como para impedir accesos no autorizados y usos indebidos
del instrumento, es fundamental seguir las recomendaciones
siguientes:
• No instale ni ejecute ningún otro software en el instrumento.
• Asegúrese de que el resto de ordenadores y servicios de
la red están suficientemente protegidos contra software
malintencionado y cualquier acceso no autorizado. Estos
comprenden, entre otros, el sistema de información de
laboratorio (LIS), la memoria compartida de archivos de
almacenamiento, la memoria compartida de copias de
seguridad y los servicios.
• Los clientes son responsables de la seguridad de su red de
área local, sobre todo a la hora de protegerla contra software
y ataques malintencionados. Esta protección puede incluir
medidas como un firewall, que sirve para separar el dispositivo
de redes no controladas. Por otro lado, la protección también
puede comprender medidas que garanticen que la red
conectada está libre de códigos malintencionados.
• Limite el acceso físico al instrumento y a toda la
infraestructura informática conectada (ordenadores, cables,
equipos de red, etc.)
• Asegúrese de que los archivos de almacenamiento y de
copia de seguridad del instrumento estén protegidos
contra cualquier acceso no autorizado y contra desastres
potenciales. Esta lista incluye la ubicación de almacenamiento
remoto, los sitios de detección de desastres y la transferencia
segura de archivos de copia de seguridad.
• En la medida de lo posible, utilice un firewall para restringir el
tráfico de la red.
• Las memorias USB se pueden usar para diversos tipos
de copias de seguridad y restauraciones. Una incorrecta
manipulación de una memoria USB puede provocar la pérdida
de datos o el mal funcionamiento del instrumento.
• Utilice solo las memorias USB que su representante de
servicio de Roche haya probado e instalado.
• En cada momento solo se puede utilizar un dispositivo USB.
Antes de insertar una memoria USB, verifique que no haya otro
dispositivo USB insertado.
• Antes de extraer una memoria USB, pulse el botón Expulsar de
Windows.
• No se debe modificar la configuración predeterminada del
sistema operativo (SO) proporcionada con el servidor, ya
que esto tiene implicaciones en las configuraciones de SO
reforzadas.
• Para evitar que un virus infecte el uPath enterprise software,
use la memoria USB exclusivamente en el instrumento. No
almacene otros datos en esta memoria USB.
Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC) 7

Flujo de trabajo para usar el algoritmo de análisis de imagen uPath PD-L1 para NSCLC
Materiales necesarios
• uPath enterprise software
• Algoritmo de análisis de imagen uPath PD-L1 (SP263) para NSCLC
• Portaobjetos de tejido de NSCLC teñidos con el VENTANA PD-L1 (SP263) Assay (usando el OptiView DAB IHC Detection Kit)
teñidos en el instrumento BenchMark ULTRA
• Escáner de portaobjetos VENTANA DP 200
Flujo de trabajo
1. Una muestra de tejido de NSCLC en un portaobjetos se tiñe con el VENTANA PD-L1 (SP263) Assay utilizando un instrumento
BenchMark ULTRA.
2. La adquisición de imágenes (escaneado completo del portaobjetos) se realiza con el escáner de portaobjetos VENTANA DP 200
con un aumento de 20 veces en un plano z.
3. Una vez que se adquieren las imágenes digitales, estas imágenes se transfieren desde el ordenador asociado con el escáner de
portaobjetos VENTANA DP 200 al sistema de administración de imágenes (IMS) en un servidor centralizado.
4. Después de la transferencia al servidor, se creará un caso en el uPath enterprise software. La creación de casos se puede producir
automáticamente a través de la comunicación con el sistema de información de laboratorio (LIS) utilizando la información de
identificación (es decir, tipo de tejido y anticuerpo primario) que se encuentra en la etiqueta del código de barras del portaobjetos o que
se introduce manualmente en el uPath enterprise software (consulte la Guía del usuario de uPath enterprise software (ref. 1018943ES)).
5. Si se instala el algoritmo de análisis de imagen uPath PD-L1 (SP263) para NSCLC (debe instalarse en un servidor distinto del usado
para el uPath enterprise software y el IMS) y se accede a una imagen de 20 aumentos con la tinción y el tipo de tejido adecuados,
después, el uPath enterprise software desencadena automáticamente el Análisis Completo del Portaobjetos (Whole Slide Analysis,
WSA).
6. WSA analiza automáticamente toda la imagen escaneada.
7. Una vez que WSA finaliza, se informa desde el uPath enterprise software al anatomopatólogo que “analysis is complete” («el
análisis ha finalizado»). Ahora, el anatomopatólogo puede seleccionar ROI específicos para puntuar. Un anatomopatólogo puede
seleccionar un único ROI de cualquier tamaño o múltiples ROI. Si se seleccionan múltiples ROI, se proporciona una puntuación
añadida, así como una puntuación individual para cada ROI.
Tinción
• La preparación y tinción del tejido debe seguir las recomendaciones que se proporcionan en la hoja de método del VENTANA PD-
L1 (SP263) Assay.
• Todos los controles adecuados deben revisarse y los portaobjetos deben volver a teñirse si la tinción no cumple las directrices
descritas en la hoja de método del VENTANA PD-L1 (SP263) Assay.
• El algoritmo de análisis de imagen uPath PD-L1 (SP263) para NSCLC requiere el uso del VENTANA PD-L1 (SP263) Assay, y
cualquier material o suministros adicionales indicados en la hoja de método del VENTANA PD-L1 (SP263) Assay, para teñir los
tejidos antes del análisis. El VENTANA PD-L1 (SP263) Assay detecta la proteína PD-L1 en el tejido de NSCLC FFPE teñido con el
OptiView DAB IHC Detection Kit en un instrumento BenchMark ULTRA. Aunque el VENTANA PD-L1 (SP263) Assay detecta la
proteína PD-L1 en el tejido de NSCLC FFPE teñido en los instrumentos BenchMark ULTRA, el algoritmo de análisis de imagen uPath
PD-L1 (SP263) para NSCLC se validó utilizando el OptiView DAB IHC Detection Kit teñido en el instrumento BenchMark ULTRA.
Captura de imágenes
Es necesario el uso del escáner de portaobjetos VENTANA DP 200 para escanear los portaobjetos. Las imágenes deben escanearse
con un aumento de 20x. Si hay grandes secciones de la imagen desenfocadas, se recomienda volver a escanear los portaobjetos.
Para obtener más información sobre el escaneado, consulte el manual de usuario del escáner de portaobjetos VENTANA DP 200
(ref. 1017149ES).
8 Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC)

Navegación general: uPath enterprise software
El uPath enterprise software está diseñado para adaptarse a las necesidades individuales y del sitio, incluidos, entre otros: configuración
de informes e interfaz de usuario. Esta Guía de algoritmos se centrará en las herramientas necesarias para usar solamente el algoritmo
de análisis de imagen uPath PD-L1 (SP263) para NSCLC. Para obtener más información sobre el uPath enterprise software, consulte la
Guía del usuario de uPath enterprise software.
Flujo de trabajo del anatomopatólogo
Abrir un caso
Se puede acceder a las imágenes de tejido de NSCLC teñido con el VENTANA PD-L1 (SP263) Assay haciendo doble clic en un caso o
seleccionando un caso y pulsando en la pestaña del visor dentro del uPath enterprise software (Figura 1).
Aparecerá una pantalla con todas las imágenes asociadas a un caso (Figura 2).
Figura 2
Figura 1
Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC) 9

Una vez escaneado un portaobjetos teñido con el VENTANA PD-L1 (SP263) Assay en un escáner de portaobjetos VENTANA DP 200 a
20x, la imagen se importa al uPath enterprise software y se asocia con un caso. El algoritmo de análisis de imagen uPath PD-L1 (SP263)
para NSCLC activará automáticamente el WSA. El tiempo necesario para finalizar el paso de precálculo del WSA dependerá de las
especificaciones del servidor, los tamaños de imagen y el número de imágenes en la cola. Cuando se muestra, “waiting to start auto-
analysis” («esperando para iniciar el autoanálisis») quiere decir que las imágenes están en la cola y aún no se han analizado, y aparecerá
“analyzing” («analizando») cuando se realiza el WSA (Figuras 3 y 4). Una vez que la imagen se analiza por completo a través del WSA
en el uPath enterprise software, se mostrará “analysis successful” («análisis correcto») debajo de la imagen del portaobjetos dentro del
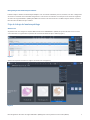
Viewer (Visor) en el uPath enterprise software (Figura 5). Las imágenes no se pueden puntuar antes de finalizar con éxito el WSA.
Dibujar el tumor completo (ROI): selección del área tumoral
Use el botón de la herramienta Freehand (Mano alzada) dentro del menú desplegable ROI (Figura 6) para seleccionar las áreas
tumorales en la imagen del portaobjetos IHC a analizar. La Figura 7 muestra una imagen que tiene una sola ROI dibujada. Se pueden
extraer ROI adicionales. Cada área seleccionada dará como resultado un ROI que aparecerá en el Slide Panel (Panel de portaobjetos)
(Figura 8).
Figura 6 Figura 7
Figura 8
Figura 5
Figura 4
Figura 3
10 Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC)

Dibujar la o las ROI del tumor completo: área de exclusión
Al dibujar la ROI, puede ser necesario excluir ciertas áreas; las áreas específicas que se deben evitar u omitir, así como los ejemplos, se
tratarán a continuación, en la sección de características de tinción. Use la herramienta de exclusión Freehand (Mano alzada) dentro
del menú desplegable Exclusion (Exclusión) (Figura 9) para excluir las áreas específicas (Figura 10). Si hay grandes áreas de la imagen
borrosas o desenfocadas, vuelva a escanear el portaobjetos.
Las áreas excluidas no se analizarán mediante el algoritmo, y las TC teñidas y no teñidas dentro de esta área se excluirán del área
de análisis total. Si ya se ha analizado la ROI y se realiza una exclusión, será necesario volver a analizar la ROI y la superposición y la
puntuación se actualizarán correctamente.
Dibujar una gran cantidad de exclusiones, especialmente las exclusiones Freehand (Mano alzada) complicadas, puede llevar mucho
tiempo y afectar la eficiencia del flujo de trabajo, aportando un impacto marginal a la puntuación final. Si un caso requiere una gran
cantidad de exclusiones, el anatomopatólogo debe hacer lo siguiente:
• Dibujar múltiples ROI y excluir porciones de tejido que considere irrecuperables con un uso mínimo de la herramienta de Exclusion
(Exclusión).
• Limitar las exclusiones y anular manualmente la puntuación con otra puntuación.
Dibujar la o las ROI del tumor completo: supresión
Si una ROI del tumor completo seleccionada no es óptima, se puede eliminar. Seleccione la ROI del tumor completo haciendo clic en
el centro de la ROI en la imagen y después haciendo clic en el botón Delete (Eliminar) dentro del Slide Panel (Panel de portaobjetos)
(Figura 11) o dentro de la imagen del portaobjetos junto a la ROI (Figura 12). Aparecerá una ventana de confirmación. Seleccione
Confirm (Confirmar) para eliminar la ROI seleccionada. Seleccione Cancel (Cancelar) para conservar la ROI.
Figura 10Figura 9
Figura 11 Figura 12
Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC) 11

Una vez que se han dibujado todas las áreas de exclusión y/o las ROI del tumor completo, la imagen está lista para ser analizada.
Seleccione la ROI del tumor completo haciendo clic en el centro de la ROI que se analizará o haciendo clic en la ROI en el Slide Panel
(Panel de portaobjetos). Para cada ROI, seleccione el botón Image Analysis (Análisis de la imagen) dentro del Slide Panel (Panel de
portaobjetos) (Figura 13) o al lado de la ROI (Figura 14).
Una vez que finaliza el Análisis PD-L1, el resultado aparecerá en el Slide Panel (Panel de portaobjetos) en dos ubicaciones: debajo de
Slide Score (puntuación de portaobjetos) y al lado del ROI (Figura 15). Slide Score (Puntuación de portaobjetos) se basa en una suma
del estado de positividad de la célula tumoral en todos los ROI seleccionados, que es la puntuación que aparecerá en el informe.
Análisis de imagen PD-L1
Figura 15
También puede ver información más detallada en el menú desplegable Slide Score (Puntuación de portaobjetos) y en el menú
desplegable Details (Detalles) de la ROI haciendo clic en el icono desplegable (Figura 16). Aparecerá el menú desplegable Slide Score
(Puntuación de portaobjetos) (Figura 17). Al hacer clic en el mismo icono desplegable también se ocultará esta información.
Figura 17
Figura 16
Figura 13 Figura 14
12 Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC)

Análisis de imagen PD-L1: superposición en colores falsos
Una vez que se ha pulsado el botón ROI(s) Analysis (Análisis de ROI) y se ha analizado el tejido, se mostrará una superposición de
colores en la ROI. En la imagen que aparece a continuación (Figura 18), los círculos rojos representan células que se determinaron
como teñidas positivamente para PD-L1 y los círculos azules representan células que se determinaron negativas para PD-L1. Al sujetar
la imagen (pulsando el botón izquierdo del ratón y moviendo la imagen) la superposición desaparecerá (Figura 19). Cuando se deja de
pulsar el botón del ratón, la superposición vuelve a aparecer (Figura 18).
Figura 18
Figura 19
Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC) 13

Anulación manual de la introducción de puntuación de portaobjetos
Las puntuaciones se pueden anular manualmente haciendo clic en el icono desplegable Slide Score (Puntuación de portaobjetos)
dentro del Slide Panel (Panel de portaobjetos) al lado de Slide Score (Puntuación de portaobjetos) (Figura 16). Aparecerá el menú
desplegable Slide Score (Puntuación de portaobjetos) (Figura 20). Al seleccionar el botón Edit (Editar) (Figura 20) en el menú
desplegable Slide Score (Puntuación de portaobjetos), el usuario podrá introducir manualmente la puntuación (Figura 21). El campo
Comments (Comentarios) permite introducir notas sobre el caso y/o la decisión de anular la puntuación automatizada. Se pueden
introducir manualmente puntuaciones de PD-L1 de 0-100%. Tras introducir una anulación manual de la puntuación, seleccione el
botón Confirm (Confirmación) (Figura 22). Aparecerá un mensaje de confirmación; haga clic en “Yes” («Sí»).
La puntuación que aparece dentro del Slide Panel (Panel de portaobjetos) reflejará ahora anulación manual de la puntuación.
La puntuación del análisis de imagen proporcionado junto a los ROI ya no aparecerá (Figura 23). El usuario tendrá la opción de volver
a analizar la imagen pulsando el botón del gráfico de barras (Figura 13, Figura 14).
Figura 21 Figura 22
Figura 20
Figura 23
14 Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC)

Consulte la hoja de método del VENTANA PD-L1 (SP263) Assay y la Guía de interpretación.
Evaluación de PD-L1
Las células neoplásicas de NSCLC marcadas con el VENTANA PD-L1 (SP263) Assay se evalúan para verificar la positividad del
porcentaje de TC con tinción de la membrana a cualquier intensidad. La tinción inmunohistoquímica en el NSCLC es membranosa y/o
cistoplasmática, y se puede expresar homogénea o heterogéneamente por todo el neoplasma. La tinción citoplasmática de células
tumorales no se incluye en la puntuación de positividad de TC. La tinción de la membrana puede presentar un patrón discontinuo,
circunferencial o basolateral. Se utiliza un anticuerpo de control negativo compatible con isotipo para evaluar la presencia de fondo en
las muestras de la prueba.
Evaluación de la tinción del algoritmo PD-L1
El anatomopatólogo, usando el algoritmo de análisis de imagen uPath PD-L1 (SP263) para NSCLC debe estar familiarizado con la
puntuación manual del VENTANA PD-L1 (SP263) Assay. El anatomopatólogo debe usar la herramienta Freehand (Mano alzada) para
rodear toda el área tumoral. El anatomopatólogo debe hacer referencia al portaobjetos de control negativo y la H&E asociada antes
de utilizar el algoritmo de análisis de imagen uPath PD-L1 (SP263) para NSCLC. Al seleccionar las áreas a analizar, tenga en cuenta
las limitaciones descritas en las secciones Limitaciones y Áreas a evitar. Si el anatomopatólogo no está de acuerdo con la puntuación
proporcionada por el algoritmo de análisis de imagen uPath PD-L1 (SP263) para NSCLC, el anatomopatólogo debe anular manualmente
la puntuación.
Entre los casos no evaluables se incluyen casos con tumor viable insuficiente, morfología inaceptable y antecedentes interferentes.
Los casos de NSCLC con suficientes TC viables (en función de la puntuación del anatomopatólogo) y sin interferencias del fondo en el
portaobjetos IHC de PD-L1 se aceptan para su evaluación.
Características de la tinción
Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC) 15

Figura 24: imágenes escaneadas de tejido de NSCLC teñido con IHC en el uPath enterprise software; antes del análisis
(arriba) y después del análisis (abajo). La superposición roja representa células determinadas como TC teñidas positivamente
y la superposición azul representa células determinadas como TC teñidas negativamente.
En las siguientes figuras (24-25) se proporcionan imágenes de diversos patrones de tinción y niveles de expresión de PD-L1.
La expresión de PD-L1 en TC se indica como porcentaje (0-100).
16 Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC)

Figura 25: imágenes escaneadas de tejido de NSCLC teñido con IHC en el uPath enterprise software; antes del análisis
(arriba) y después del análisis (abajo). La superposición roja representa células determinadas como TC teñidas positivamente
y la superposición azul representa células determinadas como TC teñidas negativamente.
Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC) 17

Figura 26: ejemplo de identificación de células tumorales pasadas por alto. Imágenes escaneadas de tejido de NSCLC teñido con
IHC en el uPath enterprise software; antes del análisis (arriba) y después del análisis (abajo). La superposición roja representa
células determinadas como células tumorales teñidas positivamente y la superposición azul representa células determinadas como
células tumorales teñidas negativamente.
Ejemplos de células tumorales pasadas por alto
En las siguientes figuras se proporcionan varios ejemplos de células tumorales pasadas por alto (26-28).
18 Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC)

Figura 27: ejemplo de identificación de células tumorales pasadas por alto. Imágenes escaneadas de tejido de NSCLC teñido con
IHC en el uPath enterprise software; antes del análisis (arriba) y después del análisis (abajo). La superposición roja representa células
determinadas como células tumorales teñidas positivamente y la superposición azul representa células determinadas como células
tumorales teñidas negativamente.
Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC) 19

Figura 28: ejemplo de identificación de células tumorales pasadas por alto. Imágenes escaneadas de tejido de NSCLC
teñido con IHC en el uPath enterprise software; antes del análisis (arriba) y después del análisis (abajo). La superposición roja
representa células determinadas como células tumorales teñidas positivamente y la superposición azul representa células
determinadas como células tumorales teñidas negativamente.
20 Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC)

Áreas a evitar al usar el algoritmo
Al dibujar la ROI, ciertas áreas se deben excluir de toda el área tumoral utilizando la herramienta Exclusion (Exclusión) como se describió anteriormente,
o se deben evitar al definir un área tumoral con una ROI. Cuando se utiliza el algoritmo de análisis de imagen uPath PD-L1 (SP263) para NSCLC, los
anatomopatólogos deben evitar puntuar cualquier región que normalmente se evita al puntuar manualmente. La puntuación general para PD-L1 se
puede anular si el usuario no está de acuerdo con la puntuación dada por el algoritmo de análisis de imagen uPath PD-L1 (SP263) para NSCLC.
Figura 29: ejemplo de tejido necrótico antes (arriba) y después del análisis (abajo). Los usuarios deben cumplir las directrices
de puntuación descritas en la hoja de método del VENTANA PD-L1 (SP263) Assay. Es importante excluir el tejido necrótico
porque puede afectar a la forma en la que el algoritmo puntúa la muestra de tejido y ocasiona una puntuación de positividad
de TC de PD-L1 inexacta.
Ejemplo de necrosis
Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC) 21

Ejemplo de pliegues de tejido
Figura 30: ejemplo de pliegues de tejido. Los usuarios deben cumplir las directrices de puntuación descritas en la hoja de
método del VENTANA PD-L1 (SP263) Assay. Es importante excluir los pliegues de tejido porque pueden afectar a la forma en
la que el algoritmo puntúa la muestra de tejido y ocasiona una puntuación de positividad de TC de PD-L1 inexacta.
22 Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC)

Ejemplo de tinción de fondo
Figura 31: ejemplo de tinción de fondo antes (arriba) y después del análisis (abajo). Los usuarios deben cumplir las directrices
de puntuación descritas en la hoja de método del VENTANA PD-L1 (SP263) Assay. Es importante excluir la tinción de fondo
porque puede afectar a la forma en la que el algoritmo puntúa la muestra de tejido y ocasiona una puntuación de positividad
de TC de PD-L1 inexacta.
Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC) 23

Ejemplo de suciedad
Figura 32: ejemplo de suciedad antes (arriba) y después del análisis (abajo). Los usuarios deben cumplir las directrices de
puntuación descritas en la hoja de método del VENTANA PD-L1 (SP263) Assay. Es importante excluir la suciedad porque
puede afectar a la forma en la que el algoritmo puntúa la muestra de tejido y ocasiona una puntuación de positividad de TC
de PD-L1 inexacta.
24 Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC)

Ejemplo de macrófagos
Figura 33: ejemplo de macrófagos antes (arriba) y después del análisis (abajo). Los usuarios deben cumplir las directrices
de puntuación descritas en la hoja de método del VENTANA PD-L1 (SP263) Assay. Es importante excluir los macrófagos
porque pueden afectar a la forma en la que el algoritmo puntúa la muestra de tejido y ocasiona una puntuación de positividad
de TC de PD-L1 inexacta.
Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC) 25

Se evaluó el rendimiento del algoritmo de análisis de imagen uPath PD-L1 (SP263) para NSCLC mediante estudios de concordancia
interlectores, concordancia intralectores, métodos de comparación, concordancia entre escáneres y concordancia intraescáner. Todos
los análisis se realizaron utilizando el algoritmo de análisis de imagen uPath PD-L1 para NSCLC en el uPath enterprise software. Los
anatomopatólogos participantes siguieron las pautas descritas en esta Guía de algoritmos en todos los estudios. Todas las muestras
de tejido se tiñeron con el VENTANA PD-L1 (SP263) Assay usando el OptiView DAB IHC Detection Kit en un instrumento BenchMark
ULTRA y se escanearon usando el escáner de portaobjetos VENTANA DP 200 a un nivel de aumento de 20X. Solo se usaron portaobjetos
o imágenes de portaobjetos que se consideraron aceptables según las pautas descritas en la hoja de método del VENTANA PD-L1
(SP263) Assay. Cualquier cantidad menor que el umbral se determinó negativa y cualquier cantidad igual o mayor que el umbral del
50% se consideró positiva.
Características de rendimiento
Comparación de métodos
El estudio de comparación del método PD-L1 (SP263) para el algoritmo de análisis de imagen uPath PD-L1 (SP263) para NSCLC y la
lectura manual (microscopio) estuvo formado por 180 secciones de NSCLC archivadas y anonimizadas. Las muestras de la prueba de
estudio abarcaron un intervalo de positividad del 0 al 100% y fueron interpretadas por tres anatomopatólogos cualificados diferentes.
Tabla 1. Concordancia: lectura manual frente a análisis de imagen (umbral del 50%)
Resultado LM Concordancia
Lector Resultado AI Positivo Negativo Total Medida [a] % (n/N) CI del 95 % [b]
Global
Positivo 174 25 199 PCP (%) 96,7 (174/180) (94,0, 98,9)
Negativo 6 335 341 PCN (%) 93,1 (335/360) (90,2, 95,6)
Total
180 360 540 PCG (%) 94,3 (509/540) (92,0, 96,1)
Lector 1
Positivo 59 11 70 PCP (%) 98,3 (59/60) (91,1, 99,7)
Negativo 1 109 110 PCN (%) 90,8 (109/120) (84,3, 94,8)
Total 60 120 180 PCG (%) 93,3 (168/180) (88,7, 96,1)
Lector 2
Positivo
56 9 65 PCP (%) 93,3 (56/60) (84,1, 97,4)
Negativo 4 111 115 PCN (%) 92,5 (111/120) (86,4, 96,0)
Total 60 120 180 PCG (%) 92,8 (167/180) (88,0, 95,7)
Lector 3
Positivo 59 5 64 PCP (%) 98,3 (59/60) (91,1, 99,7)
Negativo 1 115 116 PCN (%) 95,8 (115/120) (90,6, 98,2)
Total 60 120 180 PCG (%) 96,7 (174/180) (92,9, 98,5)
LM= Lectura manual, AI=análisis de imagen
[a] PCP = Porcentaje de concordancia positiva; PCN = Porcentaje de concordancia negativa; PCG = Porcentaje de concordancia global.
[b] En general, los intervalos de confianza se calcularon utilizando el método bootstrap percentil. Para cada resultado del lector, los intervalos de
confianza se calcularon utilizando el método de puntuación de Wilson.
Nota: en el análisis solo se incluyeron observaciones que fueran evaluaciones presentes.
Nota: las observaciones que se sitúan en el intervalo de clase de la puntuación clínica final <1 % o > = 1 % a <50 % fueron negativas. Las
observaciones que se sitúan en el intervalo de clase de la puntuación clínica final > = 50 % fueron positivas.
26 Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC)

Resultado modal Concordancia
Método Lectura Resultado del lector Positivo Negativo Total Medida [a] % (n/N) CI del 95 % [b]
AI TAT
Global
Positivo 62 0 62 PCP 98,4 (62/63) (95,7, 100,0)
Negativo 1 116 117 PCN 100,0 (116/116) (96,8, 100,0)
Total 63 116 179 PCG 99,4 (178/179) (98,3, 100,0)
Lectura 1
Positivo 21 0 21 PCP 100,0 (21/21) (84,5, 100,0)
Negativo 0 38 38 PCN 100,0 (38/38) (90,8, 100,0)
Total 21 38 59 PCG 100,0 (59/59) (93,9, 100,0)
Lectura 2
Positivo
20 0 20 PCP 95,2 (20/21) (77,3, 99,2)
Negativo 1 39 40 PCN 100,0 (39/39) (91,0, 100,0)
Total 21 39 60 PCG 98,3 (59/60) (91,1, 99,7)
Lectura 3
Positivo 21 0 21 PCP 100,0 (21/21) (84,5, 100,0)
Negativo 0 39 39 PCN 100,0 (39/39) (91,0, 100,0)
Total 21 39 60 PCG 100,0 (60/60) (94,0, 100,0)
Tabla 3. Concordancia intralectores del estado de PD-L1 (50%)
AI = análisis de imagen
[a] PCP = Porcentaje de concordancia positiva; PCN = Porcentaje de concordancia negativa; PCG = Porcentaje de concordancia global.
[b] En general, los intervalos de confianza se calcularon utilizando el método bootstrap percentil estratificado mediante intervalos de clase cribados. Para el resultado
de cada ronda, los intervalos de confianza se calcularon utilizando el método de puntuación de Wilson.
Nota: en el análisis solo se incluyeron observaciones que fueran evaluaciones presentes.
Nota: las observaciones que se sitúan en el intervalo de clase de la puntuación clínica final <1 % o > = 1 % a <50 % fueron negativas. Las observaciones que se sitúan
en el intervalo de clase de la puntuación clínica final > = 50 % fueron positivas.
Nota: La observación con el portaobjetos ID C103 se excluyó de este análisis por resultar irreconciliables los datos.
Estudios de reproducibilidad de anatomopatólogos
Los estudios de reproducibilidad de anatomopatólogos para el algoritmo de análisis de imagen uPath PD-L1 (SP263) para NSCLC
estuvieron formados por 180 secciones de NSCLC archivadas y anonimizadas para interlectores y 60 secciones de NSCLC archivadas y
anonimizadas. Las muestras de la prueba de estudio abarcaron un intervalo de positividad del 0 a 100% y fueron interpretadas por tres
anatomopatólogos cualificados diferentes.
Resultado modal Concordancia
Método Lector
Resultado del lector
Positivo Negativo Total Medida [a] % (n/N) CI del 95 % [b]
AI TAT
Global
Positivo 194 5 199 PCP 95,1 (194/204) (92,5, 97,5)
Negativo 10 331 341 PCN 98,5 (331/336) (97,1, 99,7)
Total 204 336 540 PCG 97,2 (525/540) (95,9, 98,5)
Lector 1
Positivo 68 2 70 PCP 100,0 (68/68) (94,7, 100,0)
Negativo 0 110 110 PCN 98,2 (110/112) (93,7, 99,5)
Total 68 112 180 PCG 98,9 (178/180) (96,0, 99,7)
Lector 2
Positivo
64 1 65 PCP 94,1 (64/68) (85,8, 97,7)
Negativo 4 111 115 PCN 99,1 (111/112) (95,1, 99,8)
Total 68 112 180 PCG 97,2 (175/180) (93,7, 98,8)
Lector 3
Positivo 62 2 64 PCP 91,2 (62/68) (82,1, 95,9)
Negativo 6 110 116 PCN 98,2 (110/112) (93,7, 99,5)
Total 68 112 180 PCG 95,6 (172/180) (91,5, 97,7)
AI = análisis de imagen
[a] PCP = Porcentaje de concordancia positiva; PCN = Porcentaje de concordancia negativa; PCG = Porcentaje de concordancia global.
[b] En general, los intervalos de confianza se calcularon utilizando el método bootstrap percentil. Para cada resultado del lector, los intervalos de confianza se
calcularon utilizando el método de puntuación de Wilson.
Nota: en el análisis solo se incluyeron observaciones que fueran evaluaciones presentes.
Nota: las observaciones que se sitúan en el intervalo de clase de la puntuación clínica final <1 % o > = 1 % a <50 % fueron negativas. Las observaciones que se sitúan
en el intervalo de clase de la puntuación clínica final > = 50 % fueron positivas.
Tabla 2. Concordancia interlectores del estado de PD-L1 (50%)
Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC) 27

Resultado modal Concordancia
Método Escáner Resultado del escáner Positivo Negativo Total Medida [a] % (n/N) CI del 95 % [b]
AI TAT
Global
Positivo 204 2 206 PCP 100,0 (204/204) (98,2, 100,0)
Negativo
0 334 334 PCN 99,4 (334/336) (98,5, 100,0)
Total 204 336 540 PCG 99,6 (538/540) (99,1, 100,0)
Escáner 1
Positivo 72 1 73 PCP 100,0 (72/72) (94,9, 100,0)
Negativo 0 107 107 PCN 99,1 (107/108) (97,1, 100,0)
Total 72 108 180 PCG 99,4 (179/180) (98,3, 100,0)
Escáner 2
Positivo
69 1 70 PCP 100,0 (69/69) (94,7, 100,0)
Negativo 0 110 110 PCN 99,1 (110/111) (97,5, 100,0)
Total 69 111 180 PCG 99,4 (179/180) (98,3, 100,0)
Escáner 3
Positivo 63 0 63 PCP 100,0 (63/63) (94,3, 100,0)
Negativo 0 117 117 PCN 100,0 (117/117) (96,8, 100,0)
Total 63 117 180 PCG 100,0 (180/180) (97,9, 100,0)
Tabla 5. Concordancia intraescáner del estado de PD-L1 (50%)
AI = análisis de imagen
[a] PCP = Porcentaje de concordancia positiva; PCN = Porcentaje de concordancia negativa; PCG = Porcentaje de concordancia global.
[b] Los intervalos de confianza se calcularon utilizando el método bootstrap percentil.
Nota: en el análisis solo se incluyeron observaciones que fueran evaluaciones presentes.
Nota: las observaciones que se sitúan en el intervalo de clase de la puntuación clínica <1% o > = 1% a <50% se consideran negativas. Las observaciones que se
sitúan en el intervalo de clase de la puntuación clínica final > = 50% se consideran positivas.
Estudios de reproducibilidad de los escáneres
Los estudios de reproducibilidad de los escáneres para el algoritmo de análisis de imagen uPath PD-L1 (SP263) para NSCLC, estuvieron
formados por 60 secciones de NSCLC archivadas y anonimizadas. Las muestras de la prueba del estudio abarcaron un intervalo de
positividad del 0 a 100% Un usuario formado los escaneó 3 veces en cada uno de los 3 escáneres de portaobjetos VENTANA DP
200 diferentes a 20X y los analizó usando el algoritmo de análisis de imagen uPath PD-L1 (SP263) para NSCLC. Las puntuaciones se
compararon entre escáneres.
Resultado modal Concordancia
Método Escáner Resultado del lector Positivo Negativo Total Medida [a] % (n/N) CI del 95 % [b]
AI TAT
Global
Positivo 201 5 206 PCP 97,1 (201/207) (95,2, 100,0)
Negativo 6 328 334 PCN 98,5 (328/333) (96,4, 100,0)
Total 207 333 540 PCG 98,0 (529/540) (96,5, 99,4)
Escáner 1
Positivo 69 4 73 PCP 100,0 (69/69) (94,7, 100,0)
Negativo 0 107 107 PCN 96,4 (107/111) (91,7, 100,0)
Total 69 111 180 PCG 97,8 (176/180) (94,4, 100,0)
Escáner 2
Positivo
69 1 70 PCP 100,0 (69/69) (94,7, 100,0)
Negativo 0 110 110 PCN 99,1 (110/111) (97,5, 100,0)
Total 69 111 180 PCG 99,4 (179/180) (98,3, 100,0)
Escáner 3
Positivo 63 0 63 PCP 91,3 (63/69) (85,7, 100,0)
Negativo 6 111 117 PCN 100,0 (111/111) (96,7, 100,0)
Total 69 111 180 PCG 96,7 (174/180) (95,0, 100,0)
AI = análisis de imagen
[a] PCP = Porcentaje de concordancia positiva; PCN = Porcentaje de concordancia negativa; PCG = Porcentaje de concordancia global.
[b] Los intervalos de confianza se calcularon utilizando el método bootstrap percentil.
Nota: en el análisis solo se incluyeron observaciones que fueran evaluaciones presentes.
Nota: las observaciones que se sitúan en el intervalo de clase de la puntuación clínica <1% o > = 1% a <50% se consideran negativas. Las observaciones que se
sitúan en el intervalo de clase de la puntuación clínica final > = 50% se consideran positivas.
Tabla 4. Concordancia entre escáneres del estado de PD-L1 (50%)
28 Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC)

Resolución de problemas
Volver a generar un análisis fallido
Si se produce un error al realizar el WSA en el uPath enterprise software, se mostrará “analysis error” («error en el análisis») debajo de la
imagen del portaobjetos en una barra de color rojo (Figura 34).
Para volver a generar un análisis dentro del uPath enterprise software, comience iniciando sesión como Administrator (Administrador)
(Figura 35).
Una vez dentro de Administrator Settings (Ajustes de administrador), haga clic en Job Queue (Cola de trabajos) (Figura 36).
Figura 34
Figura 35
Figura 36
Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC) 29

Al seleccionar la pestaña Failed (Fallido), se mostrarán todos los portaobjetos con análisis fallidos. Seleccione el portaobjetos que debe
analizarse para habilitar los botones Cancel Job (Cancelar trabajo) y Start Job (Iniciar trabajo) (Figura 37).
Figura 37
Figura 38
Al seleccionar Start Job (Iniciar trabajo), se iniciará el análisis y, si tiene éxito, se mostrará “Job scheduled successfully” («Trabajo
planificado correctamente») en la parte superior de la pantalla en una barra de color verde (Figura 38).
30 Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC)

La imagen del portaobjetos aparecerá ahora en la página Pending (Pendiente). Una vez en esta página, si hay varias imágenes en la cola,
es posible reorganizar los trabajos en orden de prioridad (Figura 39).
Después de unos segundos, la imagen superior del portaobjetos se moverá a la página In-Progress (En progreso) y mostrará una barra
de progreso. No es necesario permanecer en esta página para realizar el análisis (Figura 40).
Figura 40
Figura 39
Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC) 31

Cuando finaliza un análisis de portaobjetos, se moverá a la página Canceled/Complete (Cancelado/Completo) (Figura 41). En el uPath
Viewer (Visor de uPath), “analysis successful” («análisis correcto») se mostrará ahora debajo de la imagen del portaobjetos y todas las
funciones analíticas importantes para la diapositiva estarán disponibles (Figura 42).
Figura 42
Figura 41
32 Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC)

Bibliografía
1. Ferlay J, Soerjomataram I, Ervik M, et al. GLOBOCAN 2012 v1.0. Cancer Incidence and Mortality Worldwide: IARC
CancerBase No. 11. http://globocan.iarc.fr. Published 2013-12-12. Updated 2014-01-09. Accessed 2016-02-08.
2. Howlader N, Noone AM, Krapcho M, et al. (eds). SEER Cancer Statistics Review (CSR),1975-2012. National Cancer
Institute. http://seer.cancer.gov/csr/1975_2012/. Published 2015-04-23. Updated 2015-11-18. Accessed 2016-02-08.
3. Keir ME, Butte MJ, Freeman GJ, et al. PD-1 and its ligands in tolerance and immunity. Annu Rev Immunol 2008;26:677-704.
4. Blank C, Mackensen A. Contribution of the PD-L1/PD-1 pathway to T-cell exhaustion: an update on implications
for chronic infections and tumor evasion. Cancer Immunol Immunother. 2007;56(5):739-745.
5. Butte MJ, Keir ME, Phamduy TB, et al. Programmed death-1 ligand 1 interacts specifically with the
B7-1 costimulatory molecule to inhibit T-cell responses. Immunity. 2007;27(1):111-122.
6. Dong H, Zhu G, Tamada K, et al. B7-H1, a third member of the B7 family, co-stimulates T-cell
proliferation and interleukin-10 secretion. Nat Med. 1999;5(12):1365-1369.
7. Massard C, Gordon MS, Sharma S, et al. Safety and efficacy of durvalumab (MEDI4736), an anti-programmed cell death ligand-1
immune checkpoint inhibitor, in patients with advanced urothelial bladder cancer. J Clin Oncol. 2016;34(26):3119-3126.
Guía de algoritmos del análisis de imagen uPath PD-L1 (SP263) para el cáncer pulmonar no microcítico (NSCLC) 33

Roche Diagnostics GmbH
Sandhofer Strasse 116
D-68305 Mannheim
Germany
www.roche.com
www.ventana.com
© 2020 Ventana Medical Systems, Inc. y Roche Diagnostics
International, Inc. Todos los derechos reservados.
VENTANA, BENCHMARK, OPTIVIEW, UPATH y el logotipo de
VENTANA son marcas comerciales de Roche. Todas las demás
marcas comerciales pertenecen a sus respectivos propietarios.
1019285ES Rev A
2020-03-31
08764174001
-
 1
1
-
 2
2
-
 3
3
-
 4
4
-
 5
5
-
 6
6
-
 7
7
-
 8
8
-
 9
9
-
 10
10
-
 11
11
-
 12
12
-
 13
13
-
 14
14
-
 15
15
-
 16
16
-
 17
17
-
 18
18
-
 19
19
-
 20
20
-
 21
21
-
 22
22
-
 23
23
-
 24
24
-
 25
25
-
 26
26
-
 27
27
-
 28
28
-
 29
29
-
 30
30
-
 31
31
-
 32
32
-
 33
33
-
 34
34
-
 35
35
-
 36
36
-
 37
37
-
 38
38
Roche uPath PD-L1 image analysis for NSCLC IVD Algorithm Manual de usuario
- Tipo
- Manual de usuario
Artículos relacionados
-
Roche VENTANA PD-L1 (SP263) Assay, Universal, CE IVD, Predictive, NSCLC Interpretation Guide
-
Roche uPath IVD Manual de usuario
-
Roche VENTANA anti-ALK D5F3 Primary Antibody Manual de usuario
-
Roche uPath IVD Manual de usuario
-
Roche BenchMark XT/LT Interpretation Guide
-
Roche iScan HT RUO Manual de usuario








































